Сера — элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к
группе халькогенов — элементов VIa группы.
Сера — S — простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при
религиозных обрядах.

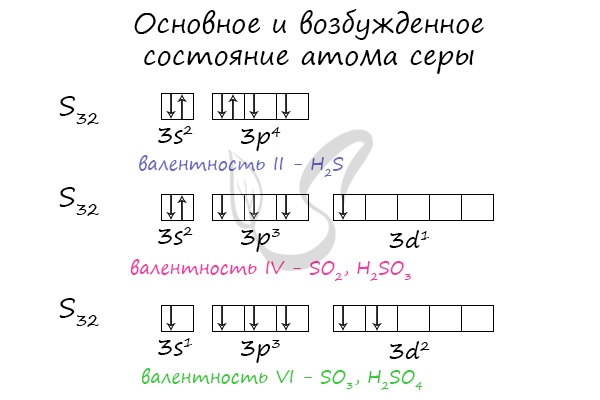
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных
электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 — пирит, колчедан
- ZnS — цинковая обманка
- PbS — свинцовый блеск (галенит), Sb2S3 — сурьмяный блеск, Bi2S3 — висмутовый блеск
- HgS — киноварь
- CuFeS2 — халькопирит
- Cu2S — халькозин
- CuS — ковеллин
- BaSO4 — барит, тяжелый шпат
- CaSO4 — гипс
В местах вулканической активности встречаются залежи самородной серы.

Получение
В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S,
SO2.
H2S + O2 = S + H2O (недостаток кислорода)
SO2 + C = (t) S + CO2
Серу можно получить разложением пирита
FeS2 = (t) FeS + S
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
H2S + H2SO4 = S + H2O (здесь может также выделяться SO2)
Химические свойства
- Реакции с неметаллами
- Реакции с металлами
- Реакции с кислотами
- Реакции с щелочами
- Реакции с солями
На воздухе сера окисляется, образуя сернистый газ — SO2. Реагирует со многими неметаллами, без нагревания —
только со фтором.
S + O2 = (t) SO2
S + F2 = SF6
S + Cl2 = (t) SCl2
S + C = (t) CS2

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
K + S = (t) K2S
Al + S = (t) Al2S3
Fe + S = (t) FeS
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
S + H2SO4 = (t) SO2 + H2O
S + HNO3 = (t) H2SO4 + NO2 + H2O
Сера вступает в реакции диспропорционирования с щелочами.
S + KOH = (t) K2S + K2SO3 + H2O
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
Na2SO3 + S → (t) Na2S2O3
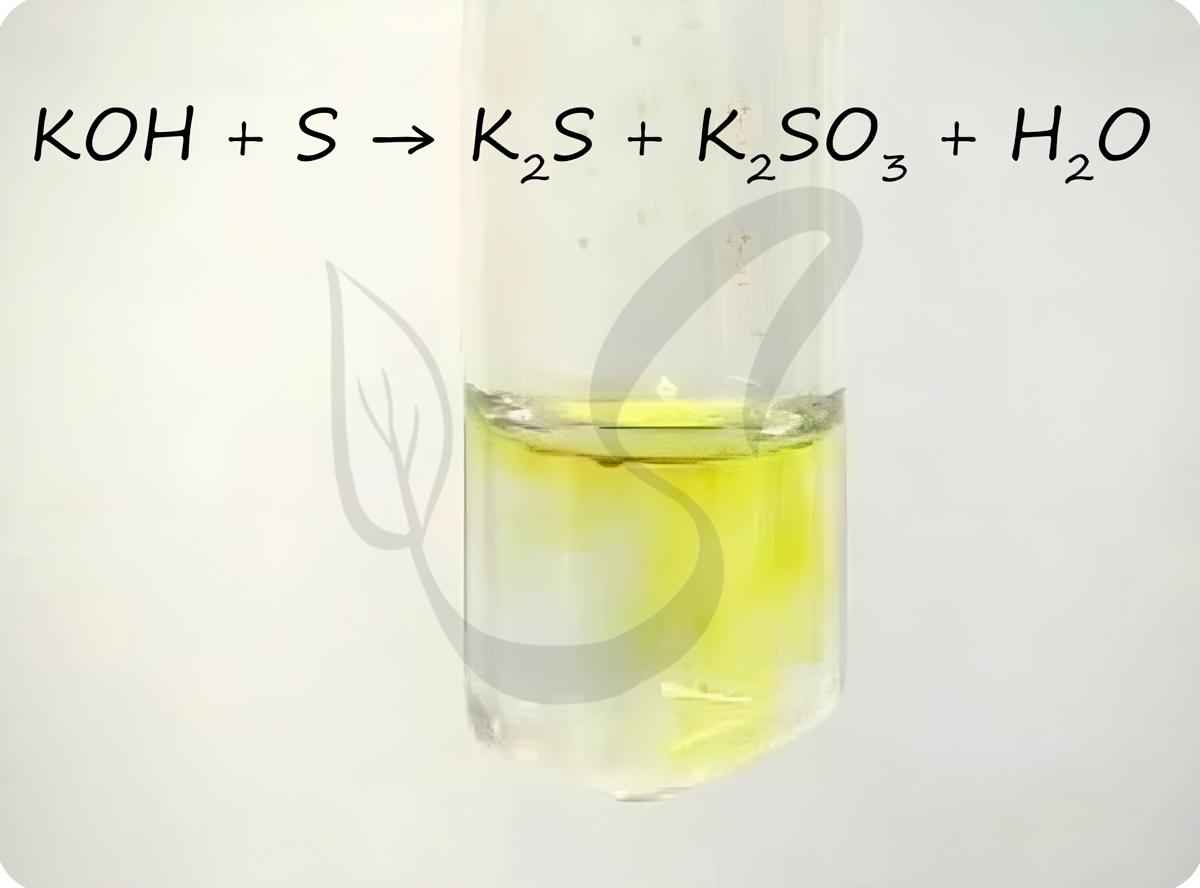
Сероводород — H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные
ванны).

Получение
Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.
Al2S3 + H2O = (t) Al(OH)3↓ + H2S↑
FeS + HCl = FeCl2 + H2S↑

Химические свойства
- Кислотные свойства
- Восстановительные свойства
- Качественная реакция
Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит
от соотношения основания и кислоты).
MgO + H2S = (t) MgS + H2O
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
2KOH + H2S = K2S + 2H2O
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Ca + H2S = (t) CaS + H2
Сероводород — сильный восстановитель (сера в минимальной степени окисления S2-). Горит в кислороде синим пламенем, реагирует с кислотами.
H2S + O2 = H2O + S (недостаток кислорода)
H2S + O2 = H2O + SO2 (избыток кислорода)
H2S + HClO3 = H2SO4 + HCl

Качественной реакцией на сероводород является реакция с солями свинца, в ходе которой образуется сульфид свинца.
H2S + Pb(NO3)2 = PbS↓ + HNO3
Оксид серы — SO2
Сернистый газ — SO2 — при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся
спички).

Получение
В промышленных условиях сернистый газ получают обжигом пирита.
FeS2 + O2 = (t) FeO + SO2
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота,
распадающаяся на сернистый газ и воду.
K2SO3 + H2SO4 = (t) K2SO4 + H2O + SO2↑
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
Cu + H2SO4(конц.) = (t) CuSO4 + SO2 + H2O
- Кислотные свойства
- Восстановительные свойства
- Как окислитель
С основными оксидами, основаниями образует соли сернистой кислоты — сульфиты.
K2O + SO2 = K2SO3
NaOH + SO2 = NaHSO3
2NaOH + SO2 = Na2SO3 + H2O

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
Fe2(SO4)3 + SO2 + H2O = FeSO4 + H2SO4
SO2 + O2 = (t, кат. — Pt) SO3
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
CO + SO2 = CO2 + S
H2S + SO2 = S + H2O
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Получение
SO2 + H2O ⇄ H2SO3
Химические свойства
- Диссоциация
- Кислотные свойства
- Окислительные свойства
- Восстановительные свойства
Диссоциирует в водном растворе ступенчато.
H2SO3 = H+ + HSO3—
HSO3— = H+ + SO32-
В реакциях с основными оксидами, основаниями образует соли — сульфиты и гидросульфиты.
CaO + H2SO3 = CaSO3 + H2O
H2SO3 + 2KOH = 2H2O + K2SO3 (соотношение кислота — основание, 1:2)
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота — основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
H2SO3 + H2S = S↓ + H 2O
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.
H2SO3 + Br2 = H2SO4 + HBr

Оксид серы VI — SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
Получение
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора
(оксид ванадия — Pr, V2O5).
SO2 + O2 = (кат) SO3
В лабораторных условиях разложением солей серной кислоты — сульфатов.
Fe2(SO4)3 = (t) SO3 + Fe2O3
Химические свойства
- Кислотные свойства
- Окислительные свойства
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли — сульфаты и
гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке — средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке — кислая соль)
SO3 + Ca(OH)2 = CaSO4 + H2O

SO3 + Li2O = Li2SO4
SO3 + H2O = H2SO4
SO3 — сильный окислитель. Чаще всего восстанавливается до SO2.
SO3 + P = SO2 + P2O5
SO3 + H2S = SO2 + H2O
SO3 + KI = SO2 + I2 + K2SO4

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Чтобы поделиться, нажимайте
Физические свойства
Газ, бесцветный, с запахом тухлых яиц, ядовит, растворим в воде (в одном объёме H2O растворяется 3 объёма H2S при н.у.); t°пл. = -86°C; t°кип. = -60°С.
Получение
1) H2 + S → H2S↑ (при t)
2) FeS + 2HCl → FeCl2 + H2S↑
Химические свойства
1) Раствор H2S в воде – слабая двухосновная кислота.
Диссоциация происходит в две ступени:
H2S → H+ + HS— (первая ступень, образуется гидросульфид — ион)
HS— → 2H+ + S2- (вторая ступень)
Сероводородная кислота образует два ряда солей — средние (сульфиды) и кислые (гидросульфиды):
Na2S – сульфид натрия;
CaS – сульфид кальция;
NaHS – гидросульфид натрия;
Ca(HS)2 – гидросульфид кальция.
2) Взаимодействует с основаниями:
H2S + 2NaOH(избыток) → Na2S + 2H2O
H2S (избыток) + NaOH → NaНS + H2O
3) H2S проявляет очень сильные восстановительные свойства:
H2S-2 + Br2 → S0 + 2HBr
H2S-2 + 2FeCl3 → 2FeCl2 + S0 + 2HCl
H2S-2 + 4Cl2 + 4H2O → H2S+6O4 + 8HCl
3H2S-2 + 8HNO3(конц) → 3H2S+6O4 + 8NO + 4H2O
H2S-2 + H2S+6O4(конц) → S0 + S+4O2 + 2H2O
(при нагревании реакция идет по — иному:
H2S-2 + 3H2S+6O4(конц) → 4S+4O2 + 4H2O
4) Сероводород окисляется:
при недостатке O2
2H2S-2 + O2 → 2S0 + 2H2O
при избытке O2
2H2S-2 + 3O2 → 2S+4O2 + 2H2O
5) Серебро при контакте с сероводородом чернеет:
4Ag + 2H2S + O2 → 2Ag2S↓ + 2H2O
Потемневшим предметам можно вернуть блеск. Для этого в эмалированной посуде их кипятят с раствором соды и алюминиевой фольгой. Алюминий восстанавливает серебро до металла, а раствор соды удерживает ионы серы.
6) Качественная реакция на сероводород и растворимые сульфиды — образование темно-коричневого (почти черного) осадка PbS:
H2S + Pb(NO3)2 → PbS↓ + 2HNO3
Na2S + Pb(NO3)2 → PbS↓ + 2NaNO3
Pb2+ + S2- → PbS↓
Загрязнение атмосферы вызывает почернение поверхности картин, написанных масляными красками, в состав которых входят свинцовые белила. Одной из основных причин потемнения художественных картин старых мастеров было использование свинцовых белил, которые за несколько веков, взаимодействуя со следами сероводорода в воздухе (образуются в небольших количествах при гниении белков; в атмосфере промышленных регионов и др.) превращаются в PbS. Свинцовые белила – это пигмент, представляющий собой карбонат свинца (II). Он реагирует с сероводородом, содержащимся в загрязнённой атмосфере, образуя сульфид свинца (II), соединение чёрного цвета:
PbCO3 + H2S = PbS↓ + CO2 + H2O
При обработке сульфида свинца (II) пероксидом водорода происходит реакция:
PbS + 4H2O2 = PbSO4 + 4H2O,
при этом образуется сульфат свинца (II), соединение белого цвета.
Таким образом реставрируют почерневшие масляные картины.
7) Реставрация:
PbS + 4H2O2 → PbSO4(белый) + 4H2O
Сульфиды
Получение сульфидов
1) Многие сульфиды получают нагреванием металла с серой:
Hg + S → HgS
2) Растворимые сульфиды получают действием сероводорода на щелочи:
H2S + 2KOH → K2S + 2H2O
3) Нерастворимые сульфиды получают обменными реакциями:
CdCl2 + Na2S → 2NaCl + CdS↓
Pb(NO3)2 + Na2S → 2NaNO3 + PbS↓
ZnSO4 + Na2S → Na2SO4 + ZnS↓
MnSO4 + Na2S → Na2SO4 + MnS↓
2SbCl3 + 3Na2S → 6NaCl + Sb2S3↓
SnCl2 + Na2S → 2NaCl + SnS↓
Химические свойства сульфидов
1) Растворимые сульфиды сильно гидролизованы, вследствие чего их водные растворы имеют щелочную реакцию:
K2S + H2O → KHS + KOH
S2- + H2O → HS— + OH—
2) Сульфиды металлов, стоящих в ряду напряжений левее железа (включительно), растворимы в сильных кислотах:
ZnS + H2SO4 → ZnSO4 + H2S
3) Нерастворимые сульфиды можно перевести в растворимое состояние действием концентрированной HNO3:
FeS2 + 8HNO3 → Fe(NO3)3 + 2H2SO4 + 5NO + 2H2O
Сероводород
Строение молекулы и физические свойства
Сероводород H2S – это бинарное соединение водорода с серой, относится к летучим водородным соединениям. Следовательно, сероводород бесцветный ядовитый газ, с запахом тухлых яиц. Образуется при гниении. В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода похожа на структуру воды — уголковая молекула. Но валентный угол H-S-H меньше, чем угол H-O-H в воде и составляет 92,1о.
Способы получения сероводорода
1. В лаборатории сероводород получают действием минеральных кислот на сульфиды металлов, расположенных в ряду напряжений левее железа.
Например, при действии соляной кислоты на сульфид железа (II):
FeS + 2HCl → FeCl2 + H2S↑
Еще один способ получения сероводорода – прямой синтез из водорода и серы:
S + H2 → H2S
Еще один лабораторный способ получения сероводорода – нагревание парафина с серой.
Видеоопыт получения и обнаружения сероводорода можно посмотреть здесь.
2. Также сероводород образуется при взаимодействии растворимых солей хрома (III) и алюминия с растворимыми сульфидами. Сульфиды хрома (III) и алюминия необратимо гидролизуются в водном растворе.
Например: хлорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
2CrCl3 + 3Na2S + 6H2O → 2Cr(OH)3 + 3H2S↑ + 6NaCl
Химические свойства сероводорода
1. В водном растворе сероводород проявляет слабые кислотные свойства. Взаимодействует с сильными основаниями, образуя сульфиды и гидросульфиды:
Например, сероводород реагирует с гидроксидом натрия:
H2S + 2NaOH → Na2S + 2H2O
H2S + NaOH → NaНS + H2O
2. Сероводород H2S – очень сильный восстановитель за счет серы в степени окисления -2. При недостатке кислорода и в растворе H2S окисляется до свободной серы (раствор мутнеет):
2H2S + O2 → 2S + 2H2O
В избытке кислорода:
2H2S + 3O2 → 2SO2 + 2H2O
3. Как сильный восстановитель, сероводород легко окисляется под действием окислителей.
Например, бром и хлор окисляют сероводород до молекулярной серы:
H2S + Br2 → 2HBr + S↓
H2S + Cl2 → 2HCl + S↓
Под действием избытка хлора в водном растворе сероводород окисляется до серной кислоты:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
Например, азотная кислота окисляет сероводород до молекулярной серы:
H2S + 2HNO3(конц.) → S + 2NO2 + 2H2O
При кипячении сера окисляется до серной кислоты:
H2S + 8HNO3(конц.) → H2SO4 + 8NO2 + 4H2O
Прочие окислители окисляют сероводород, как правило, до молекулярной серы.
Например, оксид серы (IV) окисляет сероводород:
2H2S + SO2 → 3S + 2H2O
Соединения железа (III) также окисляют сероводород:
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
Бихроматы, хроматы и прочие окислители также окисляют сероводород до молекулярной серы:
3H2S + K2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
2H2S + 4Ag + O2 → 2Ag2S + 2H2O
Серная кислота окисляет сероводород либо до молекулярной серы:
H2S + H2SO4(конц.) → S + SO2 + 2H2O
Либо до оксида серы (IV):
H2S + 3H2SO4(конц.) → 4SO2 + 4H2O
4. Сероводород в растворе реагирует с растворимыми солями тяжелых металлов: меди, серебра, свинца, ртути, образуя черные сульфиды, нерастворимые ни в воде, ни в минеральных кислотах.
Например, сероводород реагирует в растворе с нитратом свинца (II). при этом образуется темно-коричневый (почти черный) осадок, нерастворимый ни в воде, ни в минеральных кислотах:
H2S + Pb(NO3)2 → PbS + 2HNO3
Взаимодействие с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видеоопыт взаимодействия сероводорода с нитратом свинца можно посмотреть здесь.
Таблицы качественных реакций
21-Дек-2013 | комментариев 9 | Лолита Окольнова
Вопросы части С объединяют знание всех тем химии. В случае Задания С2 ЕГЭ по химии — знание всех классов неорганических веществ и их качественных реакции.
Дается конкретный химический эксперимент, ход которого нужно описать химическими реакциями.
Для таких реакции обычно предлагаются какие-то внешние проявления — выделения газа, выпадение осадка или изменение окраски раствора.
Таблица качественных реакций для газов
| Описание | Формула |
Реакции |
| Бурый газ |
NO2 |
1) N2 + 2O2 = 2NO2 2) взаимодействие металлов с азотной кислотой (концентрированной) 3) разложение нитратов |
| Запах тухлых яиц |
H2S |
Взаимодействие активных металлов с концентрированной серной кислотой: |
|
Газ с резким запахом. Растворимый в воде |
SO2 |
1) взаимодействие серасодежащих веществ с кислородом
2) взаимодействие некоторых металлов с концентрированной серной кислотой |
| Газ с резким характерным запахом, растворимый в воде |
NH3 |
1) N2 + 3H2 = 2NH3 2) обменные реакции солей аммония |
| Газ, не поддерживающий горение, малорастворимый в воде, не ядовитый |
N2 |
1) горение азотсодержащих веществ; NH4NO2 = N2 + 2H2O |
|
Газы, поддерживающие горение: (для NO2 – бурый цвет) |
O2 O3 NO2 |
3C + 2O3 = 3CO2 С + 2NO2 = CO2 + 2NO |
Таблица качественных реакций для щелочных металлов:
Т.к. все соединения щелочных металлов хорошо растворимы в воде, то их определяют по цвету пламени:
(указан так же цвет пламени некоторых щелочно-земельных металлов)
|
желто-зеленое |
фиолетовое |
кирпично-красное |
ярко-красное |
желтое |
карминово-красное |
|
Ba2+ |
K+ |
Са2+ |
Li+ |
Na+ |
Sr2+ |
Таблица качественных реакций
— цвета осадков
|
Осадки белого цвета |
Качественная реакция |
|
Белый творожистый нерастворимый в воде; нерастворимый в HNO3 |
Ag+ + Cl— → AgCl↓ качественная реакция на соли серебра; качественная реакция на хлорид-ионы; |
|
Белый осадок нерастворимый в кислотах |
Ba2+ + SO4 -2 → BaSO4↓ качественная реакция на соли бария; качественная реакция на сульфат-ионы; |
|
Белый осадок образуется при пропускании газа без цвета с резким запахом через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах |
Сa(OH)2 + SO2 = CaSO3↓ + H2O
|
|
Белый осадок образуется при добавлении щелочи; растворяется в избытке щелочи |
Al3+ + 3OH— = Al(OH)3↓ Zn2+ + 2OH— = Zn(OH)2↓
|
|
Белый осадок образуется при пропускании газа без цвета и запаха через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах |
Сa(OH)2 + CO2 = CaCO3↓ + H2O
CaCO3 + 2H+ → CO2↑ + H2O + Ca2+ |
|
Осадок светло-желтого цвета (осадок кремового цвета) образуется при приливании AgNO3; нерастворим в HNO3; |
Ag+ + Br— → AgBr↓ качественная реакция на бромид-ионы; (качественная реакция на соли серебра); |
|
Осадок желтого цвета образуется при приливании AgNO3; нерастворим в HNO3; |
Ag+ + I— → AgJ↓ качественная реакция на иодид-ионы; (качественная реакция на соли серебра); |
|
Осадок желтого цвета образуется при приливании AgNO3; растворим в кислотах; |
3Ag+ + PO43- → Ag3PO4↓ |
|
Осадки коричневых цветов |
Качественная реакция |
|
Осадок бурого цвета образуется при взаимодействии с растворами щелочей; |
Fe3+ +3OH— → Fe(OH)3↓ качественная реакция на соли железа |
|
Осадки синих и зеленых цветов |
Качественная реакция |
|
Осадки зеленого цвета |
Fe2+ +2OH— → Fe(OH)2↓ |
|
Осадок голубого цвета (осадок синего цвета) образуется при взаимодействии с растворами щелочей |
Cu2+ +2OH— → Cu(OH)2↓ качественная реакция на соли меди (II) |
|
Осадок синего цвета образуется при взаимодействии с раствором красной кровяной и желтой кровяной соли |
3Fe2+ + 2[Fe(CN)6]3- → Fe3[Fe(CN)6]2↓ качественная реакция на соли железа (II) — с красной кровяной солью; 4Fe3+ + 3[Fe(CN)6]-4 → Fe4[Fe(CN)6]3↓ качественная реакция на соли железа (III) — с желтой кровяной солью; |
|
Осадки черного цвета |
Качественная реакция |
|
Осадок черного цвета Образуется при взаимодействии с сульфидами или с H2S |
Fe2+ + S2- → FeS↓ Ni2+ + S2- → NiS↓ Cu2+ + S2- → CuS↓ Pb2+ + S2- → PbS↓ Hg2+ + S2- → HgS↓ Ag+ + S2- → Ag2S↓ качественная реакция на сульфид-ионы |
Обсуждение: «Таблицы качественных реакций»
(Правила комментирования)
…
Сероводород
Получение
сероводорода
- Получение из простых веществ:
S + Н2 = H2S
- Взаимодействие минеральных кислот и сульфидов металлов, расположенных в ряду напряжений левее железа:
FeS + 2HCI = H2S↑ + FeCl2
- Действие концентрированной H2SO4 (без избытка) на щелочные и щелочно-земельные металлы:
5H2SO4(конц.) + 8Na = H2S↑ + 4Na2SO4 + 4H2О
- Гидролиз некоторых сульфидов:
AI2S3 + 6Н2О = 3H2S↑ + 2Аl(ОН)3↓
- Нагревание парафина с серой:
C40H82 + 41S = 41Н2S+40С
Видео Получение и обнаружение сероводорода
Физические
свойства и строение сероводорода
Сероводород H2S – это бинарное летучее водородное соединение соединение с серой. H2S — бесцветный ядовитый газ, с неприятным удушливым
запахом тухлых яиц. При концентрации > 3 г/м3 вызывает смертельное отравление.
Сероводород тяжелее воздуха и легко конденсируется в бесцветную жидкость. Растворимость в воде H2S при обычной температуре составляет 2,5.
В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы сероводорода представляет собой сцепленные между собой атомы H-S-H с валентным углом 92,1о.
Качественная реакция для обнаружения сероводорода
Для
обнаружения анионов S2- и сероводорода используют
реакцию газообразного H2S с Pb(NO3)2:
H2S + Pb(NO3)2 = 2HNO3 + PbS↓ черный
осадок.
Влажная бумага, смоченная в растворе Pb(NO3)2 чернеет в присутствии H2S из-за получения черного осадка PbS.
Химические свойства серы
H2S является сильным восстановителем
При взаимодействии H2S с окислителями образуются различные вещества — S, SО2, H2SO4
- Окисление кислородом воздуха:
2H2S + 3О2(избыток) = 2SО2↑ + 2Н2О
2H2S + О2(недостаток) = 2S↓ + 2Н2О
- Окисление галогенами:
H2S + Br2 = S↓ + 2НВr
H2S + Cl2 → 2HCl + S↓
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
- Взаимодействие с кислотами-окислителями:
3H2S + 8HNО3(разб.) = 3H2SO4 + 8NO + 4Н2О
H2S + 8HNО3(конц.) = H2SO4 + 8NО2↑ + 4Н2О
H2S + H2SO4(конц.) = S↓ + SО2↑ + 2Н2О
- Взаимодействие со сложными окислителями:
5H2S + 2KMnO4 + 3H2SO4 = 5S↓ + 2MnSO4 + K2SO4 + 8Н2О
5H2S + 6KMnO4 + 9H2SO4 = 5SО2 + 6MnSO4 + 3K2SO4 + 14Н2О
H2S + 2FeCl3 = S↓ + 2FeCl2 + 2HCl
2H2S + SO2 = 2H2O + 3S
3H2S + K2Cr2O7 + 4H2SO4 → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
- Сероводородная кислота H2S двухосновная кислота и диссоциирует по двум ступеням:
1-я ступень:
H2S → Н+ + HS—
2-я ступень:
HS— → Н+ + S2-
H2S очень слабая
кислота, несмотря на это имеет характерные для кислот химические свойства. Взаимодействует:
- с активными металлами
H2S + Mg = Н2↑ + MgS
- с малоактивными металлами (Аg, Си, Нg) при совместном присутствии окислителей:
2H2S + 4Аg + O2 = 2Ag2S↓ + 2Н2O
- с основными оксидами:
H2S + ВаО = BaS + Н2O
- со щелочами:
H2S + NaOH(недостаток) = NaHS + Н2O
H2S + 2NaOH(избыток) → Na2S + 2H2O
- с аммиаком:
H2S + 2NH3(избыток) = (NH4)2S
- с некоторыми солями сильных кислот, если образующийся сульфид металла нерастворим в воде и в сильных кислотах:
CuSO4 + H2S = CuS↓ + H2SO4
H2S + Pb(NO3)2 → PbS↓ + 2HNO3
Реакция
с нитратом свинца в растворе – это качественная реакция на сероводород и сульфид-ионы.
Видео Взаимодействие сероводорода с нитратом свинца
Сульфиды
Получение сульфидов
- Непосредственно из простых веществ:
S + Fe → FeS
S + Mg → MgS
S + Ca → CaS
- Взаимодействие H2S с растворами щелочей:
H2S + 2NaOH = 2H2O + Na2S
H2S + NaOH = H2O + NaHS
- Взаимодействие H2S или (NH4)2S с растворами солей:
H2S + CuSO4 = CuS↓ + H2SO4
H2S + 2AgNO3 = Ag2S↓ + 2HNO3
Pb(NO3)2 + Н2S → PbS↓ + 2НNO3
ZnSO4 + Na2S → ZnS↓ + Na2SO4
- Восстановление сульфатов при прокаливании с углем:
Na2SO4 + 4С = Na2S + 4СО
Физические свойства сульфидов
Сульфиды – это бинарные соединения серы с элементами с меньшей электроотрицательностью, в том числе с некоторыми неметаллами (С, Si, Р, As и др.).
По растворимости
в воде и кислотах сульфиды классифицируют
на:
- растворимые в воде — сульфиды щелочных металлов и аммония;
- нерастворимые в воде, но растворимые в минеральных кислотах — сульфиды металлов, расположенных до железа в ряду активности (белые и цветные сульфиды ZnS, MnS, FeS, CdS);
- нерастворимые ни в воде, ни в минеральных кислотах — черные сульфиды (CuS, HgS, PbS, Ag2S, NiS, CoS)
- гидролизуемые водой — сульфиды трехвалентных металлов (алюминия и хрома (III))
По цвету сульфиды можно разделить на:
- Чёрные – HgS, Ag2S, PbS, CuS, FeS,
NiS; - Коричневые – SnS, Bi2S3;
- Оранжевые – Sb2S3, Sb2S5;
- Жёлтые – As2S3, As2S5,
SnS2, CdS; - Розовые — MnS
- Белые – ZnS, Al2S3, BaS,
CaS;
Химические свойства сульфидов
Обратимый гидролиз сульфидов
- Хорошо растворимыми в воде являются сульфиды щелочных металлов и аммония, но в водных растворах они в значительной степени подвергаются гидролизу. Реакция среды — сильнощелочная:
K2S + H2O ⇄ KHS + KOH
S2- + H2O → HS— + ОН—
- Сульфиды щелочно-земельных металлов и Mg, при взаимодействии с водой подвергаются полному гидролизу и переходят в растворимые кислые соли — гидросульфиды:
2CaS + 2НОН
= Ca(HS)2 + Са(ОН)2
При нагревании растворов сульфидов гидролиз протекает и по 2-й ступени:
HS— + H2O → H2S↑ + ОН—
Необратимый
гидролиз сульфидов
- Сульфиды некоторых металлов (Cr2S3, Fe2S3, Al2S3) подвергаются необратимому гидролизу, полностью разлагаясь в водных растворах:
Al2S3 + 6H2O = 3H2S↑ + 2AI(OH)3↓
Нерастворимые
сульфиды гидролизу не подвергаются
NiS + HСl ≠
- Некоторые из сульфидов растворяются в сильных кислотах:
FeS + 2HCI =
FeCl2 + H2S↑
ZnS + 2HCI =
ZnCl2 + H2S↑
CuS + 8HNO3 → CuSO4 + 8NO2 + 4H2O
CuS + 4H2SO4(конц. гор.) → CuSO4 + 4SO2 + 4H2O
MnS + 3HNO3 = MnSO4 + 8NO2 + 4H2O
- Сульфиды Ag2S, HgS, Hg2S, PbS, CuS не pacтворяются не только в воде, но и во многих кислотах.
- Сульфиды обладают восстановительными свойствами и вступают в реакции с окислителями:
PbS + 4H2O2 → PbSO4 + 4H2O
СuS + Cl2 → CuCl2 + S
- Окислительный обжиг сульфидов является
важной стадией переработки сульфидного сырья в различных производствах
2ZnS + 3O2 = 2ZnO + 2SO2
4FeS2 + 11O2 = 2Fe2O3 + 8SO2↑
2CuS + 3O2 → 2CuO + 2SO2
2Cr2S3 + 9O2 → 2Cr2O3 + 6SO2
Взаимодействия
сульфидов с растворимыми солями свинца, серебра, меди являются качественными на ион S2−:
Na2S + Pb(NO3)2 → PbS↓ + 2NaNO3
Na2S + 2AgNO3 → Ag2S↓ + 2NaNO3
Na2S + Cu(NO3)2 → CuS↓ + 2NaNO3
Оксид серы
(IV), диоксид серы, сернистый газ, сернистый ангидрид (SO2)
Способы получения сернистого газа
- Окисление серы, сероводорода и сульфидов кислородом воздуха:
S + O2 → SO2
2H2S + 3O2 → 2SO2 + 2H2O
2CuS + 3O2 → 2SO2 + 2CuO
- Действие высокой температуры на сульфиты (термическое разложение):
CaSO3 = СаО + SO2↑
- Действие сильных кислот на сульфиты:
Na2SO3 + 2HCl = SO2 + Н2O + 2NaCI
- Взаимодействие концентрированной H2SO4 с восстановителями, например с неактивными металлами:
2H2SO4 + Сu = SO2↑ + CuSO4 + 2Н2O
Физические
свойства сернистого газа
При обычной температуре SO2 — газ с резким запахом без цвета. В воде растворим хорошо — при 20°С в 1 л воды растворяется 40 л SO2.
Химические свойства сернистого газа
SO2 – типичный кислотный оксид. За счет того, что сера находится в промежуточной степени окисления (+4) SO2 может проявлять свойства как окислителя так и восстановителя.
- При растворении в воде SO2 частично соединяется с молекулами воды с образованием слабой сернистой кислоты.
SO2 + H2O ↔ H2SO3
- Как
кислотный оксид, SO2 вступает
в реакции с щелочами и оксидами щелочных и щелочноземельных металлов:
SO2 + СаО = CaSO3
SO2 + Na2O → Na2SO3
SO2 + NaOH = NaHSO3
SO2 + 2NaOH = Н2O + Na2SO3
- При взаимодействии с окислителями SO2 проявляет восстановительные свойства. При этом степень окисления серы повышается:
2SO2 + O2 ↔ 2SO3
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
SO2 + 2HNO3 → H2SO4 + 2NO2
SO2 + O3 → SO3 + O2
SO2 + PbO2 → PbSO4
5SO2 + 2H2O + 2KMnO4 → 2H2SO4 + 2MnSO4 + K2SO4
Обесцвечивание раствора перманганата калия KMnO4 является качественной реакцией для обнаружения сернистого газа и сульфит-иона
- SO2 проявляет окислительные свойства при взаимодействии с сильными восстановителями, восстанавливаясь чаще всего до свободной серы:
SO2 + 2Н2S → 3S↓ + 2H2O
SO2 + 2CO → S↓ +2СО2
SO2 + С → S↓ + СO2
Оксид серы (VI), триоксид серы, серный ангидрид (SO3)
Способы получения серного ангидрида
- SO3 можно получить из SO2 путем каталитического окисления последнего кислородом:
2SO2 + O2 ↔ 2SO3
- Окислением SO2 другими окислителями:
SO2 + O3 → SO3 + O2
SO2 + NO2 → SO3 + NO
- Разложением сульфата железа (III):
Fe2(SO4)3 → Fe2O3 + 3SO3
Физические
свойства серного ангидрида
При обычных условиях SO3 представляет собой бесцветную жидкость с характерным резким
запахом. На воздухе SO3 «дымит» и сильно
поглощает влагу.
SO3 – тяжелее
воздуха, хорошо растворим в воде.
SO3 ядовит!
Химические свойства серного
ангидрида
Оксид серы (VI) – это кислотный оксид.
- Хорошо поглощает влагу и реагирует с водой образуя серную кислоту:
SO3 + H2O → H2SO4
- Как кислотный оксид, SO3 взаимодействует с щелочами и
основными оксидами, образуются средние или кислые соли:
SO3 + 2NaOH(избыток) → Na2SO4 + H2O
SO3 + NaOH(избыток) → NaHSO4
SO3 + MgO → MgSO4 (при сплавлении):
SO3 + ZnO = ZnSO4
- SO3 проявляет сильные окислительные свойства, так
как сера в находится в максимальной степени окисления (+6).
Вступает в реакции с восстановителями:
SO3 + 2KI → I2 + K2SO3
3SO3 + H2S → 4SO2 + H2O
5SO3 + 2P → P2O5 + 5SO2
- При растворении в концентрированной
серной кислоте образует олеум (раствор
SO3 в H2SO4).
Сернистая кислота (H2SO3)
Способы
получения сернистой кислоты
При растворении в воде SO2 образует слабую сернистую кислоту, которая сразу частично разлагается:
SO2 + H2O ↔ H2SO3
Физические
свойства сернистой кислоты
Сернистая кислота H2SO3 – двухосновная кислородсодержащая кислота. При обычных условиях неустойчива.
Валентность серы
в сернистой кислоте равна IV, а степень окисления +4.
Химические свойства сернистой кислоты
Общие свойства
кислот
- Сернистая кислота – слабая кислота, диссоциирует в две стадии. Образует два типа солей:
- кислые – гидросульфиты
H2SO3 ↔ HSO3— + H+
- средние – сульфиты
HSO3—↔ SO32- + H+
- Сернистая кислота самопроизвольно распадается на SO2 и H2O:
H2SO3 ↔ SO2 + H2O
Соли сернистой кислоты, сульфиты и гидросульфиты
Способы
получения сульфитов
Соли сернистой кислоты получаются при взаимодействии SO2 с щелочами и оксидами щелочных и щелочноземельных металлов:
SO2 + СаО = CaSO3
SO2 + Na2O → Na2SO3
SO2 + NaOH = NaHSO3
SO2 + 2NaOH = Н2O + Na2SO3
Физические
свойства сульфитов
Сульфиты
щелочных металлов и аммония растворимы в воде, сульфиты остальных металлов — нерастворимы
или не существуют.
Гидросульфиты
металлов хорошо растворимы в Н2O, а некоторые из
них, такие как Ca(HSO3)2 существуют
только в растворе.
Химические свойства сульфитов
Cернистая кислота – двухосновная, образует нормальные (средние) соли — сульфиты Mex(SO3)y и кислые соли — гидросульфиты Me(HSO3)x.
- Водные растворы сульфитов подвергаются гидролизу. Реакция среды – щелочная (окрашивают лакмус в синий цвет):
SO3— + Н2O = HSO3— + ОН—
Na2SO3 + Н2O = NaHSO3 + NaOH
Реакции, протекающие без изменения степени окисления:
- Реакция с сильными кислотами:
Na2SO3 + 2HCl = 2NaCl +
SO2↑ + Н2O
NaHSO3 + HCl = NaCl + SO2↑ + Н2O
- Термическое разложение сульфитов:
CaSO3 = СаО + SO2↑
- Нормальные сульфиты в водных растворах, при избытке SO2, переходят в гидросульфиты:
CaSO3 + SO2 + Н2O = Ca(HSO3)2
- Ионно-обменные реакции с другими солями, протекающие с образованием нерастворимых сульфитов:
Na2SO3 + ZnCl2 = ZnSO3↓ + 2NaCl
Окислительно-восстановительные реакции
Сульфиты, также как и SO2, могут быть как восстановителями, так и окислителями, т.к. атомы серы в анионах находятся в промежуточной степени окисления +4
- Окисление водных растворов сульфитов, и гидросульфитов до сульфатов:
Na2SO3 + Вr2 + Н2O = Na2SO4 + 2НВr
5K2SO3 + 2КМnO4 + 3H2SO4 = 6K2SO4 + 2MnSO4 + 3Н2O
Na2SO3 + HNO3 = 2NaNO3 + SO2 + H2O
- Твердые сульфиты при хранении на воздухе также медленно окисляются до сульфатов:
2Na2SO3 + O2 = 2Na2SO4
- При нагревании сухих сульфитов с активными восстановителями (С, Mg, Al, Zn) сульфиты превращаются в сульфиды:
Na2SO3 + ЗС = Na2S + ЗСО
- При нагревании сухих сульфитов до высоких температур сульфиты диспропорционируют, превращаются в смесь сульфатов и сульфидов:
4K2SO3 = 3K2SO4 + K2S
Серная кислота (H2SO4)
Способы
получения серной кислоты
В промышленности серную кислоту производят из серы, сульфидов
металлов, сероводорода и др.
Наиболее часто серную кислоту получают из пирита FeS2.
Основные стадии получения серной кислоты включают:
1.Обжиг пирита в кислороде в печи для обжига с получением сернистого газа:
4FeS2 +
11O2 → 2Fe2O3 +
8SO2 + Q
2. Очистка полученного сернистого газа от примесей в циклоне, электрофильтре.
3. Осушка сернистого газа в сушильной башне
4. Нагрев очищенного газа в теплообменнике.
5. Окисление сернистого газа в серный ангидрид в контактном аппарате:
2SO2 + O2 ↔ 2SO3 + Q
6. Поглощение серного ангидрида серной кислотой в поглотительной башне – получение олеума.
Физические
свойства, строение серной кислоты
При обычных условиях серная кислота – тяжелая бесцветная маслянистая жидкость, хорошо растворимая в воде. Максимальная плотность равна 1,84 г/мл
При растворении серной кислоты в воде выделяется большое количество теплоты. Поэтому, по правилам безопасности в лаборатории при приготовлении разбавленного раствора серной кислоты во избежание разбрызгивания необходимо наливать серную кислоту в воду тонкой струйкой по стеклянной палочке при постоянном перемешивании. Но не наоборот!
Валентность серы в серной кислоте равна VI.
Качественные
реакции для обнаружения серной кислоты и сульфат ионов
Для обнаружения сульфат-ионов используют реакцию с растворимыми солями бария. В результате взаимодействия, образуется белый кристаллический осадок сульфата бария:
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
Видео Взаимодействие хлорида бария и сульфата натрия в растворе (качественная реакция на сульфат-ион).
Химические свойства серной кислоты
Серная кислота — сильная двухосновная кислота, образует два типа солей: средние – сульфаты, кислые – гидросульфаты.
- Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени и достаточно по второй ступени:
H2SO4 ⇄ H+ + HSO4–
HSO4– ⇄ H+ + SO42–
Характерны все свойства кислот:
- Реагирует с основными оксидами, основаниями, амфотерными оксидами, амфотерными гидроксидами и аммиаком:
H2SO4 + MgO → MgSO4 + H2O
H2SO4 + КОН → KHSО4 + H2O
H2SO4 + 2КОН → К2SО4 + 2H2O
3H2SO4 + 2Al(OH)3 → Al2(SO4)3 + 6H2O
H2SO4 + NH3 → NH4HSO4
- Вытесняет более слабые кислоты из их солей в растворе (карбонаты, сульфиды и др.) и летучие кислоты из их солей (кроме солей HBr и HI):
Н2SO4 + 2NaHCO3 → Na2SO4 + CO2 + H2O
H2SO4 + Na2SiO3 → Na2SO4 + H2SiO3
- Концентрированная серная кислота реагирует с твердыми солями, например нитратом натрия, хлорида натрия.
NaNO3(тв.) + H2SO4 → NaHSO4 + HNO3
NaCl(тв.) + H2SO4 → NaHSO4 + HCl
- Вступает в обменные реакции с солями:
H2SO4 + BaCl2 → BaSO4 + 2HCl
- Взаимодействует с металлами:
Разбавленная серная кислота взаимодействует с металлами, расположенными в ряду напряжения металлов до водорода. В результате реакции образуются соль и водород:
H2SO4(разб.) + Fe → FeSO4 + H2
H2SO4 + Zn = ZnSO4 + H2
Концентрированная серная кислота — сильный окислитель. Реакция с металлами протекает без вытеснения водорода из кислоты. В зависимости от активности металла образуются различные продукты реакции:
- Активные металлы и цинк при обычной температуре с концентрированной серной кислотой образуют соль, сероводород (или серу) и воду:
H2SO4 + Na = Na2SO4 + Н2S↑ + H2O
5H2SO4(конц.) + 4Zn → 4ZnSO4 + H2S↑ + 4H2O
- Металлы средней активности с концентрированной H2SO4 образуют соль, серу и воду:
4H2SO4 + 3Mg → 3MgSO4 + S + 4H2O
- Такие металлы, как железо Fe,
алюминий Al, хром Cr пассивируются концентрированной
серной кислотой на холоде. При нагревании,
при удалении оксидной пленки реакция возможна.
6H2SO4(конц.) + 2Fe → Fe2(SO4)3 + 3SO2 + 6H2O
6H2SO4(конц.) + 2Al → Al2 (SO4)3 + Н2S↑ + 6H2O
- Неактивные металлы восстанавливают концентрированную серную кислоту до сернистого газа:
2H2SO4(конц.) + Cu → CuSO4 + SO2 ↑ + 2H2O
2H2SO4(конц.) + Hg → HgSO4 + SO2 ↑ + 2H2O
2H2SO4(конц.) + 2Ag → Ag2SO4 + SO2↑+ 2H2O
- В реакциях с неметаллами концентрированная серная кислота также проявляет окислительные свойства:
5H2SO4(конц.) + 2P → 2H3PO4 + 5SO2↑ + 2H2O
2H2SO4(конц.) + С → СО2↑ + 2SO2↑ + 2H2O
2H2SO4(конц.) + S → 3SO2 ↑ + 2H2O
3H2SO4(конц.) + 2KBr → Br2↓ + SO2↑ + 2KHSO4 + 2H2O
5H2SO4(конц.) + 8KI → 4I2↓ + H2S↑ + K2SO4 + 4H2O
H2SO4(конц.) + 3H2S → 4S↓ + 4H2O (комнатная температура)
H2SO4(конц.) + H2S = S↓ + SО2↑ + 2Н2О (при нагревании)
H2SO4(конц.) + 2HBr = Br2 + SO2 + 2H2O
- Концентрированная серная кислота широко используется в химических процессах как водоотнимающий агент, т.к. проявляет сильное водоотнимающее действие. В органической химии ее используют при получении спиртов, простых и сложных эфиров, альдегидов и т.д.
Соли серной кислоты, сульфаты, гидросульфаты
Способы
получения солей серной кислоты
Сульфаты можно получить при взаимодействии серной кислоты с металлами,
оксидами, гидроксидами (см. Химические свойства серной кислоты). А также при
взаимодействии с другими солями, если продуктом реакции является нерастворимое
соединение.
Физические
свойства солей серной кислоты
Кристаллы разного цвета. Многие средние и кислые сульфаты растворимы
в воде. Плохо растворяются или не растворяются в воде сульфаты многозарядных
щёлочноземельных металлов (BaSO4, RaSO4), сульфаты лёгких
щёлочноземельных металлов (CaSO4, SrSO4) и сульфат свинца.
Средние сульфаты щелочных металлов термически устойчивы. Кислые
сульфаты щелочных металлов при нагревании разлагаются.
Многие средние сульфаты образуют устойчивые кристаллогидраты:
Na2SO4 ∙ 10H2O − глауберова
соль
CaSO4 ∙ 2H2O − гипс
2CaSO4 xH2O –
алебастр
CuSO4 ∙ 5H2O − медный купорос
FeSO4 ∙ 7H2O − железный купорос
ZnSO4 ∙ 7H2O − цинковый купорос
Na2CO3 ∙ 10H2O −
кристаллическая сода
KАl(SO4)2 x 12H2O
– алюмокалиевые квасцы.
Химические свойства солей серной кислоты
Разложение сульфатов на различные классы соединений в зависимости от металла, входящего в состав соли.
- Сульфаты щелочных металлов плавятся без разложения.
- Кислые сульфаты щелочных металлов разлагаются с отщеплением воды:
2KHSO4 → K2S2O7 + H2O↑.
- Сульфаты металлов средней активности разлагаются на соответствующие оксиды:
ZnSO4 = ZnO + SO3
FeSO4 = 2Fe2O3 + 4SO2 + O2
2CuSO4 → 2CuO + SO2 + O2 (SO3)
2Al2(SO4)3 → 2Al2O3 + 6SO2 + 3O2
2Cr2(SO4)3 → 2Cr2O3 + 6SO2 + 3O2
- Сульфаты тяжёлых или малоактивных металлов разлагаются с образованием металла и кислорода:
HgSO4 = Hg + SO2 + O2
- Некоторые сульфаты проявляют окислительные свойства и вступают в реакции с простыми веществами:
CaSO4 +
C = CaO + SO2 + CO
BaSO4 +
4C = BaS + 4CO



