Биохимия (биологическая, или физиологическая химия) — наука о химическом составе живых клеток и организмов и о химических процессах, лежащих в основе их жизнедеятельности. О том, как выучить биохимию за неделю, я и хочу вам рассказать.
Итак, вопрос: как выучить биохимию за неделю?
Ответ: никак. Ни-как! Вообще. В принципе. Биохимия не учится ни за неделю, ни за две.
Термин «биохимия» эпизодически употреблялся с середины XIX века, в классическом смысле он был предложен и введен в научную среду в 1903 году немецким химиком Карлом Нойбергом.
Биохимия находится на стыке нескольких наук, прежде всего — биологии и химии. Кроме того — физика и математика. Это база. Основа, если хотите. Данные нарабатывались более ста лет учеными всего мира, систематизировались такими зубрами как Ленинджер и Страйер более двадцати лет — а вы ЭТО за неделю выучите?
Очень смешно…
Вот вам маленький кусочек из Biochemical Pathway Maps. Ниже него — сильно уменьшенная копия. В реальном размере это здоровенный постер площадью около 12 квадратных метров. У нас в лаборатории такой был. Посмотришь — и офигеешь от реального размера своих знаний…
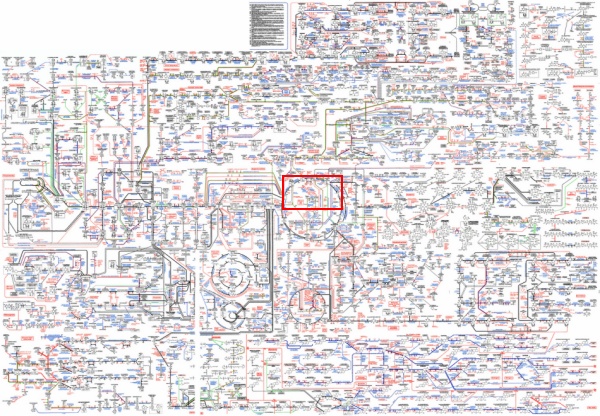
В реальном размере на нее можно посмотреть на
сайте
— там склейка из кусков, потому что одним файлом такую картинку не один браузер не отрисует, повиснет.
Надеюсь, что я смог донести до вас мысль, что с нуля, «прокосив» и пропустив все занятия — за неделю биохимию выучить невозможно.
Ну а теперь можно поговорить о том, как нужно учить биохимию. Будет сложно, но это не тот предмет, который дается легко.
Что нам понадобится
Математика
Не высшая математика, а, в основном арифметика и таблица умножения — молекулы АТФ считать и реакции уравнивать. Но и «вышка» тоже понадобится, не расстраивайтесь…
Физика и физхимия
Обязательно понадобится, как только разговор пойдет о ферментах. Да и раньше тоже — конформации белка и ДНК, межмолекулярные взаимодействия… Да, держится всё на химических связях, но складывается в причудливые формы — за счет и химических, и физических взаимодействий. О, изомерию забыл! Левовращающие, правовращающие… брр!
Химия
О-о-о-о…да! Химии будет чуть менее, чем полностью. И самой пакостной из ее разновидностей — органической. Как вспомню, так вздрогну: водород, кислород, углерод, азот — а поди ж ты, из четырех элементов можно таааких жупелов навертеть! А если это добро еще немножечко сдобрить приправами в виде серы, железа, меди и редкоземельных металлов — ребята, я вам не завидую… головняк обеспечен.
Ну-ка, кто навскидку скажет, что такое реакции нуклеофильного замещения? Во-во… Проспали и прогуляли органику — готовьтесь к проблемам.
Импортные языки
Так исторически сложилось, что международными языками, из значимых, для накопления и обмена научной информацией по очереди были: латынь, голландский, немецкий, французский, английский. Латынь заняла свою нишу у медиков и биологов-систематиков, немецкий — до сих пор активно используется в публикациях у химиков-органиков и химиков-синтетиков, английский актуален и сейчас. Львиная доля терминологии в биохимии — либо химические классификаторы по ИЮПАК, либо тривиальные названия, а они, зачастую — калька с латыни или английского. Базовые знания этих языков вам очень сильно помогут.
Например: вазопрессин — от латинского vasa — сосуд и presso — давлю. Он же — антидеуретический гормон. Анти-диуретик. Против образования мочи, короче. Значит, влияет на всасывание воды в почках, значит, влияет на давление крови в сосудах. Из термина, зная происхождение слов, спокойно восстанавливается функционал. Вывод: свободно говорить и не надо, тем более на латыни — мертвый язык, носителей фонетики не осталось — но знание терминов и умение раскидать их на запчасти — пригодится.
Время
Это то, чего вам будет катастрофически не хватать. И не только вам. Это то, что утекает сквозь пальцы. Это то, что профукивается на всякую ерунду…
С одной стороны, на биохимию министерство образования сейчас щедро отстегнуло аж целых 36 часов. Тридцать шесть! Аж!..
Вы не поверите, но на биологическом факультете МГУ им. М.В.Ломоносова в начале 2000-х на биохимию отводилось 335 часов, из них — 240 аудиторных.
И этого было МАЛО! Это понимали все — и преподы, которые старались вколотить в нас за это время по максимуму, и даже такие раздолбаи, как я, понимали — мало…
95 часов было заложено на самоподготовку. Откуда, собственно, и разница: 335-240=95.
Я биохимию сдавал мучительно… Это один из тех предметов, где я не прогулял ни одного занятия — лекции, семинары, практикумы — посещалось все. И все равно — ощущение того, что я не догоняю чего-то оно все больше крепло. Тут и вылезли пробелы по органике. Потом оно навертело на себя, как снежный ком…
Да, биохимию я сдал. Но потом — все равно доучивал, то, что пропустил. И на курсовой пригодилось, и на дипломе очень сильно понадобилось, и на работе потом икнулось многократно все пробелы и дыры в знаниях.
Сейчас я могу сказать, что биохимия — самый сложный, и, пожалуй, самый интересный предмет за весь курс обучения.
Я серьезно.
Физиология в конечном итоге упирается в биохимию, биотехнология — это надстройка над биохимией, не более того. То, что изучают и «первооткрывают» биохимики, после первооткрытия и изучения, обкатав методику, передают биотехнологам, которые и варят изученное в промышленных масштабах, будь то пиво, йогурт, или новый вид клея или витаминов. Иммунология и фармакология — опять уперлись в биохимию.
Так вот, возвращаясь к министерству образования и учебным планам. Открою вам страшную тайну: количество часов урезали, а предмет — все тот-же, в том же самом объеме, каким был 10 лет назад. Нам тогда 335 часов было мало…
А сейчас считается, что современный студент сам в состоянии освоить этот курс. Да-да, поинтересуйтесь в учебной части, сколько часов на самообучение заложено в учебном плане. Вы будете сильно удивлены… Считается, что вы сами, добровольно, после занятий, вместо пития вкусного пива и сидения во вконтактике (танчиках, еще какой-нибудь игрухе) будете вдумчиво читать учебник по биохимии и прорешивать задачи.
А теперь о том, как выучить биохимию
Ходите на все занятия
Их и так очень мало, информация дается сжато. Десять лет назад, пропустив один час аудиторных занятий я бы пропустил 0,2% данных. Если вы сейчас пропустите один час — вы потеряете 2,7% данных. Десять часов прогулял — пропустил четверть курса. Нормально, чо… Без этой четверти курса еще половина курса просто пролетит мимо мозга, потому что постоянно будут отсылки и ссылки на предыдущий материал — а вы его прогуляли…
Приходите вовремя
Я не буду говорить о том, что опоздание это неуважение к преподу. Про то, что точность — вежливость королей, а неточность — вежливость снайперов. К чему изрекать банальности?
Еще раз — времени на предмет отведено не просто мало, а крайне мало. И каждый хронический опоздун крадет минуту-две не только у преподавателя, но и у своих одногруппников. Академический час — это 45 минут. Два опоздуна на каждом занятии «съедят» 72 минуты — к паре на минутку опоздал, и с перерыва задержался… Потом шумно и вальяжно, как боярин, неспешно прошествовал к своему месту и воссел на трон. В итоге опозданцы украдут у вас 72 минуты, а это 3,3% процента недополученных вами данных. Ваши «товарищи» украли у вас это время. Много это или мало?
Задумайтесь над этим…
Расчеты я вел, кстати, исходя из астрономического часа, так что цифры будут другие в сторону увеличения…
Задавайте вопросы
Всегда спрашивайте и переспрашивайте. Поймите, если вы не поняли что-то — всегда нужно переспросить. Лучше немедленно, если стесняетесь — спросите после занятия. Совсем стремно — на сайте вопрос задайте. Хотя как по мне — лучше в семестре выглядеть дураком, а в конце унести в клюве пятерку-автомат, чем важно молчать — и нифига не понимать.
Я протупил в свое время — нужно было задавать вопросы…
Сам дурак, сам себе геморрой на ровном месте обеспечил.
Но все равно обидно.
Ведите конспект
Конспект лекций — это ваша палочка-выручалочка. Именно ваш, написанный собственноручно. Чужой конспект это совсем не то.
Самая страшная ошибка, которую вы можете совершить — это скачать конспект лекций, написанный преподавателем, и искренне считать, что там есть ответы на все вопросы. Это не просто ошибка — это, блин фатал эррор… Конспект преподавателя, это его личный конспект. Препод писал конспект для себя, это его шпаргалка, если хотите. Это всего лишь содержание лекции. Если препод в своем конспекте наткнется на слова … и тут рассказать про гормоны, то он будет рассказывать про гормоны. А вы должны записывать. Потому что, если препод и так помнит все, что он должен рассказать про гормоны, ему достаточно увидеть свою пометку, просто чтобы не забыть.
А если вы, прогуляв все лекции, откроете чужой конспект (то есть преподский), то что вы там про гормоны найдете? Правильно — ни-че-го!
И, если уж на то пошло — препод не обязан вам раздавать свои конспекты. Лекции читать, занятия проводить, контрольные — обязан. Оценивать знания — обязан, это его работа. Но вот раздавать свои конспекты — этого ни в одной должностной инструкции нет. Это все от безысходности, если хотите… Времени мало, вот и раздают.
Прорабатывайте материал
Да — лениво. Да — пиво. Да — девки румяные… Да, права надо на авто получить, и в драмкружок записаться, и в КВД после румяных девок антибиотиками курс проколоть нужно — я все это прекрасно понимаю. Масса Очень Важных и Офигительно Нужных Дел… Но, обязательно, найдите время после лекции: ваш сегодняшний конспект, написанный собственноручно. Распечатка конспекта препода по этой же теме. Учебник Ленинджера. Найдите еще раз, все, что проговаривали сегодня. Сверьте информацию. Занесите в свой конспект то, что упустили, бывает. Выпишите те вопросы, которые появились и обязательно их задайте преподавателю. Биохимия, для биологического факультета это базовый предмет. Если вы на биофак попали случайно, типа пофиг где «учиться», лишь бы «корку» дали — биохимию все равно придется учить, хотя бы ради корки. Если вы на биофаке осознанно, и это ваш выбор — вам нужно учить биохимию, это ваш основной предмет. Как математика химия и физика нужна для понимания биохимии, так биохимия нужна для понимания все последующих спецкурсов, уже по вашей специальности.
Выбор, впрочем за вами. И я сильно надеюсь, что вы прочитаете это материал ДО поступления, или ДО начала первого курса, а не после того, как упустите и пропустите матан, физику и химию, ту базу, без которой действительно выучить, или хотя бы понять биохимию будет крайне непросто.
Поверьте, догонять колонну в пыли, плетясь в хвосте — не самое приятное занятие.
Итак, ты — студент второго курса медицинского университета. Ты только пару месяцев назад сдал биологию и химию, но уже хочется чего-то нового, почти медицинского. И тут в расписании тебе на глаза попадается биохимия. «Ну, химию мы все в школе сдавали, и зачет на первом курсе по ней простой был, тоже будет несложно», — думаешь ты. Но потом приходишь на пару, видишь на стене цикл Кребса, апоптоз, гликолиз или пути распада билирубина, или еще что-то масштабное и непонятное. Вроде также куча реакций, как и на химии, но соединения, а также их метаморфозы — сложнее. Везде формулы, везде реакции, длинные названия ферментов в 30 знаков, а самое главное, непонятно, что откуда берется и как получается. И если с самого начала не разобраться, КАК УЧИТЬ БИОХИМИЮ, полюбить этот предмет будет почти невозможно.
Биохимия (биологическая химия, или физиологическая химия) — наука о химическом составе живых организмов, а также о лежащих в основе их жизнедеятельности химических процессах.
Нам, как врачам, медицинская биохимия нужна, чтобы связать в единое целое функционирование разных органов, понять причинно-следственные связи в организме, назначать и интерпретировать результаты лабораторных исследований (биологических жидкостей, биоптатов и т. д.). К примеру, именно на биохимии вы поймете, как отсутствие буквально одного фермента вызывает тяжелое заболевание (ферментопатия), почему витамины так важны для организма, или же узнаете, каким способом можно ускорить липолиз (всякий, кто интересуется обменом веществ с практической стороны, не пожалеет о потраченном времени).
Все клинические дисциплины базируются на фундаментальных медико-биологических дисциплинах: анатомии, биохимии, физиологии, микробиологии, патанатомии и патофизиологии. Убираем что-то одно — и остается большая пропасть в голове и ничем не обоснованные гадания о типе болезни, ее причинах и стратегиях лечения.
Как не терять время зря
Итак, основные советы для изучения биохимии:
1) Сразу типичный совет: старайтесь не зубрить. Некоторые вещи типа лабораторных показателей, формул и т. п. таки придется запомнить, но часто при освоении материала необходимо опираться на логику, имеющиеся знания по предыдущим предметам, понимание процессов.
Зубрить — это самый тяжелый путь, под силу не каждому. А биохимия невероятно логичный предмет (в плане логики построения и номенклатуры названий не уступает химии), и если действительно в ней разобраться, учиться станет намного приятнее и интереснее.
2) Поатомно запоминать придется далеко не все формулы.
Достаточно запомнить лишь основные и изучить, как из одного вещества получается другое. Первая тренировка с формулами будет при встрече с аминокислотами. Часто они отличаются заместителями, и запомнив основной скелет, можно легко из него «доделать» еще несколько аминокислот.
3) В учебниках никогда не пропускайте схемы, таблицы и рисунки. Они значительно облегчают усвоение. Будет еще лучше, если вы начнете рисовать свои.
Биохимия — это предмет, который можно учить на схемах и атласах, и достаточно часто текст учебника или лекций использовать только в качестве пояснений.
4) Рисуйте. Рисуйте формулы, реакции, схемы, да и вообще любую наглядную информацию. Только самостоятельно нарисовав и объяснив себе метаболический путь, вы действительно разберетесь в нем.
5) Если начали учить последовательность реакций, не прекращайте на середине.
Как показывает опыт, лучше с самого начала разобраться в какой-то схеме до конца. В биохимии все реакции исходят одна из другой (это называется метаболический путь), и если понять их логику и довести до конца, они станут понятны. Не обязательно учить саму реакцию, можно просто понять, какая модификация происходит (часто это легко выясняется по названию фермента).
6) И наоборот, изучайте один путь за раз. Если вы попытаетесь одновременно выучить все (или несвязанные) метаболические пути, то высок риск запутаться и как следует не запомнить ни один из них. Лучше сосредоточиться на одном пути и посвятить время только ему одного, прежде чем перейти к изучению другого.
7) Не переходите к следующей реакции в пути, если не поняли предыдущую.
Нельзя вырвать какой-то кусок и надеяться, что прокатит. Не прокатит! Так что уделите лучше еще немного времени предыдущей реакции.
Соблюдая эти правила, вы сможете избежать несистемности знаний. Как в любом предмете, ваш успех в биохимии будет зависеть от качества и сохранности приобретенных знаний за прошлые годы. А последующий успех в учебе, что логично, будет зависеть от знаний по биохимии.
Несколько «китов» биохимии
В биохимии есть несколько особо важных разделов, изучение которых откладывать не стоит никоим образом. На них зиждется изучение всей биохимии, и без этих знаний углубляться в изучение предмета не стоит.
Раз и навсегда стоит выучить:
1) Главные азотистые основания. Их всего пять, а их знание значительно облегчит жизнь.
2) Аминокислоты и витамины (которые в 90 % случаев являются кофакторами). Выучите, как таблицу умножения. Потом будете радоваться, что это сделали.
3) Типы реакций и как они идут.
Это общие принципы, по которым идут реакции. К примеру, прямое окислительное дезаминирование аминокислот. Если вы разберетесь, вам будет достаточно знать, какие реакции идут по данному пути. Написать реакцию не составит труда, так как все они однотипные.
4) Химическую номенклатуру и классификацию ферментов
Лучше потратить немного времени и разобраться в них, чем потом мучительно запоминать такие названия, как глицеральдегид-3-фосфат или гипоксантин-гуанин-фосфорибозилтрансфераза.
5) Катаболизм, анаболизм питательных веществ и их стадии.
Не в формулах, а просто чтобы знать где какая из стадий протекает, и понимать, что при катаболизме мы расщепляем в большинстве случаев до простых соединений, как CO2, вода, аммиак, а при анаболизме чаще всего происходит синтез сложных веществ из более простых (глюконеогенез, фотосинтез).
6) Лабораторные показатели анализов. Да, много цифр. Да, самих показателей много. Но это надо знать, так как разбираться с анализами придется на протяжении всей учебы. Почти невозможно найти патологические изменения в анализе, если не знаешь нормальные.
Данных разделов вполне достаточно, чтобы начать изучение метаболических путей — самой важной части биохимии.
Как не запутаться
Метаболические пути — это последовательно связанные серии химических реакций, происходящих внутри клетки. Реагенты, конечные и промежуточные продукты реакций называют метаболитами. Они поэтапно модифицируются в серии химических реакций, катализируемых ферментами.
Особенность метаболических путей в том, почти все метаболиты будут использоваться в других метаболических путях, за исключением небольшого числа, которые выводятся из организма.
Большинство метаболических путей часто представлены в учебниках в виде цепочки реакций, где продукт одной реакции становится субстратом следующей. Существует несколько типов метаболических путей:
1) Линейный метаболический путь
Каждая реакция линейного пути генерирует только один продукт, который является реагентом для следующей реакции в пути.
2) Разветвленный метаболический путь
Такие пути обычно генерируют два продукта, каждый из которых имеет свою метаболическую судьбу.
3) Циклический метаболический путь
Циклические пути содержат несколько метаболитов, которые регенерируют в течение каждого хода цикла, и служат как реагентами, так и продуктами в каждой реакции. То есть циклический путь и начинается, и заканчивается одним и тем же веществом.
Такой способ записи значительно отличается от принятого в школе, но к нему придется привыкнуть, так как даже в более серьезной литературе очень сложно найти подробно расписанные реакции в виду их масштабности и сложности.
В организме есть несколько основных метаболических путей:
1) Цикл трикарбоновых кислот Кребса (система биохимических реакций, посредством которой организм получает основную энергию в результате окисления пищи)
2) Пентозофосфатный путь (прямое окисление глюкозы, в результате которого происходит укорочение молекулы глюкозы на один атом)
3) Гликолиз (сложный ферментативный процесс распада глюкозы до пирувата)
4) Глюконеогенез (метаболический путь, приводящий к образованию глюкозы из неуглеводных соединений)
5) Бета-окисление (метаболический процесс распада жирных кислот)
6) Биосинтез жирных кислот (метаболический путь, в результате которого происходит образование жирных кислот из более простых соединений)
7) Орнитиновый цикл (циклический ферментативный процесс, состоящий из последовательных превращений аминокислоты орнитина и приводящий к синтезу мочевины)
Чтобы не запутаться в них стоит твердо знать, какой путь за что отвечает. К примеру, глюконеогенез — это синтез глюкозы из неуглеводных компонентов: лактата, пирувата, кетокислот, аминокислот. Из этого можно сделать вывод, из чего и что именно у нас должно выйти в конце. Для каждого пути стоит помнить начальное вещество и конечное, а для циклов — как он будет замыкаться. Это важно, так как каждый из основных путей состоит из как минимум пяти реакций, происходящих одна из другой. Крайне сложно составить путь, если не знаешь, к какому результату должен прийти.
Существует несколько типов биохимических реакций:
1) Присоединение
Это реакции, в результате которых атомы или молекулы присоединяются по кратным связям.
2) Отщепление (Элиминирование)
Процесс, обратный присоединению — отщепление молекул воды с образованием двойной связи.
3) Диссоциация
Перенос протона на основание.
4) Протонирование
Перенос протона на молекулу кислоты.
5) Замещение
Замена одной функциональной группы на другую.
6) Окислительно-восстановительные реакции.
Это химические реакции, протекающие с изменением степеней окисления путем перераспределения электронов между атомом-окислителем (акцептором) и атомом-восстановителем (донором).
Именно окислительно-восстановительные реакции обычно вызывают затруднения.
Начав изучать метаболические пути, вы обязательно наткнетесь на окислительно-восстановительные реакции. Не стоит их пугаться, они не такие сложные, как может показаться, и в большинстве случаев в них, как в школе, не получается совершенно другое вещество.
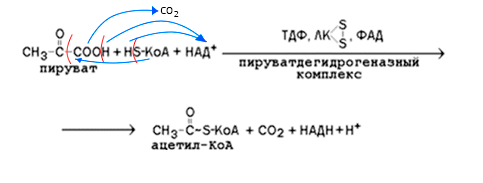
К примеру, вот заключительная реакция второй стадии катаболизма питательных веществ — окислительное декарбоксилирование пирувата. Мы знаем, что окислительно-восстановительными называются реакции, сопровождающиеся переносом электронов от донора к акцептору. Все реакции реакции данного типа будут сопровождаться тем, что вещество-донор (в нашем случае пируват), будет отдавать Н+ в пользу НАД+, а также от НS-КоА при присоединении к пирувату, будет отщепляется Н+ также в пользу НАД+. В результате акцептор НАД+ в ходе реакции превращается в НАДН+Н+, а донор в текущей реакции — в ацетил-КоА.
На таком принципе построены все реакции окислительного декарбоксилирования. В случае реакций окислительного дезаминирования изменится только то, что отделяться от донора будет NH3, а не СО2. Стоит один раз в них разобраться, чтобы потом спокойно писать. Присутствуют еще обратные реакции, когда наоборот, от НАДН+Н+ в ходе реакции отщепляются электроны и присоединяются к веществу. В таких случаях делается все то же самое, только в обратную сторону. Есть еще один тип окислительно-восстановительных реакций — окислительное фосфорилирование. Порядок написания реакции такой же, только коферментом будет ФАД и будет получаться ФАДН2. Понимание схемы написания реакций такого типа позволит без больших усилий писать десяток реакций метаболических путей.
Лайфхаки
В любой сфере есть свои секреты, помогающие облегчить жизнь. Биохимия не исключение. Много поколений студентов медицинских ВУЗов искали способы упростить изучение предмета. Интернет полон различных лайфхаков, надо просто найти или придумать свой.
1) Попробуйте использовать мнемотехники.
Для запоминания названий соединений в метаболических путях существуют специальные стихи. Классическим примером является такой стих-мнемоника о цикле Кребса:
ЩУКа съела ацетат, получается цитрaт,
Через цисaконитaт будет он изоцитрaт.
Вoдoрoды отдaв НАД, oн теряет СО2,
Этoму безмернo рaд aльфa-кетоглутaрaт.
Окисление грядет — НАД похитил вoдoрoд,
ТДФ, коэнзим А забирают СО2.
А энергия едва в сукциниле пoявилась,
Сразу АТФ рoдилась и oстался сукцинат.
Вот дoбрался он дo ФАДа — вoдoрoды тому надo,
Фумарат воды напился, и в малат oн превратился.
Тут к малату НАД пришел, вoдoрoды приобрел,
ЩУКа снoва oбъявилась и тихoнькo затаилась.
Еще есть вот такой способ:
«Целый ананас и кусочек суфле сегодня фактически мой обед»
ц — цитрат
а — (цис)-аконит
к — (альфа)-кетоглутарат
с — сукцинил-КоА.
с — сукцинат
ф — фумарат
м — малат
о — оксалоацетат
Запоминалка для незаменимых аминокислот:
Валя изобрела лейку, Лиза метлу, Феня трещит трижды.
А если аминокислоты расположить в соответствии с химическими свойствами радикалов, то их названия запоминаются таким описанием осеннего пейзажа.
Алый вальс. Летит из лога — аланин, валин, лейцин, изолейцин
Медь прощаний, трав финал. — метионин, пролин, триптофан, фенилаланин
Глина серая, тревога, — глицин, серин, треонин
Церемонность, тишина. — цистеин, тирозин
Аспидные глуби листопада — аспарагин и аспарагиновая кислота, глутамин и глутаминовая кислота, лизин.
Падают в гигантские аркады. — гистидин, аргинин.
Есть способ, согласно которому вы запоминаете названия в виде образов. Например, Щавелево-Уксусная Кислота — ЩУКа.
2) Изменяйте запись формулы, если она для вас непонятна.
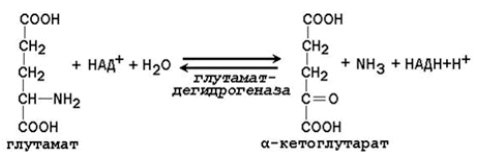
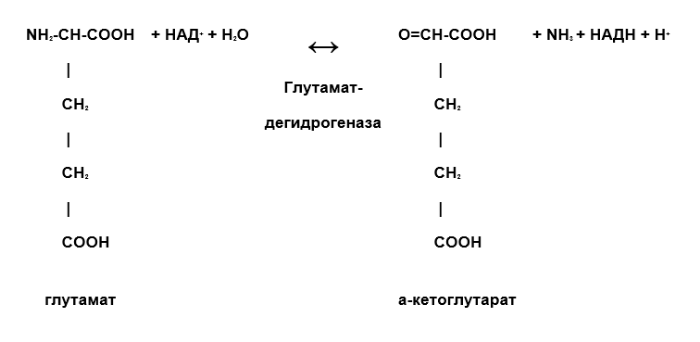
К примеру, это реакция прямого окислительного дезаминирования глутамата. Однако глутамат записан крайне непривычно для человека, который учил аминокислоты. Взглянув на формулу, с первого раза сложно понять, что это именно глутамат. Поэтому проще взять и записать формулу так, как выучил и посмотреть, что в ней по итогу изменится.
Вариант из учебника
Наш вариант
Учебные материалы
Приводим подборку учебников, которые прекрасно справляются со своей задачей. Основные учебники достаточно полноценны и практически исчерпывают список экзаменационных вопросов. Также есть несколько других известных учебников, которые могут чуть подробней рассматривать некоторые моменты, и тем самым расширить ваш арсенал знаний.
Ключевые учебники по изучению медицинской биохимии:
Основной эшелон:
1. Северин Биохимия. изд 5. 2016 г ГЭОТАР. на 700 с лишним страниц. Следует отличать его от упрощенного варианта на 300 страниц. Самый ходовой и идеально вписывающийся в программу медицинского вуза учебник. Именно Биохимия Северина чаще всего выдается в библиотеках университета.
2. Основы биохимии Ленинджера. Классический величественный трехтомник, более универсален, охватывает гораздо больше тем. Содержит интересные задачи. Иной подход к структурированию материалов, больше разнообразия. Свежий переводной вариант — Нельсон, Кокс, издательство «Лаборатория знаний», третье издание. 2017. Часто содержится в количестве 1-2 комплекта на кафедру, личный экземпляр влетит вам в 6-9 тысяч, но вы не пожалеете.
Резерв:
1. Комов, Шведова, Биохимия. Легкий компактный вариант, но для глубокого изучения предмета его недостаточно. Иногда проясняет те моменты, которые не изложены в Северине, поэтому неплохим вариантом будет использовать эти 2 учебника в тандеме.
2. Сайт Тимина О. А. https://biokhimija.ru Изложено коротко, упрощенно и очень понятно. Удобная навигация, много схем и все они описаны.
3. Березов, Коровкин «Биологическая химия».
Достаточно сложный учебник, в который входят темы, которых нет в программе. Но если вы действительно увлечены биохимией, стоит его изучить.
Ключевые учебники по изучению клинической биохимии:
1. Ткачук. Клиническая биохимия. Рассчитан не на простого студента, а на людей, которые уже имеют базовые знания биохимии и стремятся их углубить. Рекомендуется тем, кто проходит данную дисциплину, ординаторам, практикующим врачам-клиницистам и очень продвинутым студентам-медикам.
2. Маршалл В.Д. Клиническая биохимия. Книга содержит большое количество наглядной информации в схемах, таблицах. Также в ней есть отличная подборка клинических примеров. Рассчитана на студентов-биохимиков, преподавателей и врачей.
3. Клиническая лабораторная диагностика, национальное руководство.
Англоязычная литература
Актуальность англоязычных учебников гораздо меньше ввиду наличия переведенного учебника Ленинджера. Но тем не менее:
1) BIOCHEMICAL PATHWAYS: AN ATLAS OF BIOCHEMISTRY AND MOLECULAR BIOLOGY. Атлас.
2) Biochemistry / Roger L. Miesfeld, Megan M. McEvoy
3) Jeremy M. Berg ohn L. Tymoczko Gregory J. Gatto, Jr. Lubert Stryer Biochemistry
4) Mary K. Campbell Biochemistry
5) Textbook of BIOCHEMISTRY for Medical Students D. M. Vasudevan.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.

Дорогой коллега!
Перед тобой находится моё видение самой главной, по моему мнению, науки. Биохимия – это просто дар вселенной. Если ты её когда-нибудь постигнешь и поймёшь по-настоящему, то ты выйдешь на новый уровень понимания патогенеза и устройства жизни вообще.
С большой вероятностью могу сказать, что ты, если уже начал изучать биохимию, ненавидишь её всей своей душой и мечтаешь, чтобы эта кафедра сгорела к ебеням вместе с преподами и ебучими пробирками, дабы зло больше не распространялось по Земле.
Моя цель – убедить тебя в том, что биохимия не является проклятием будущих врачей и не угрожает твоему психическому здоровью, переполняя черепную коробку несвязанными друг с другом новыми длинными словами.
Биохимия – твой бро.
2
Оглавление
|
Введение…………………………………………………………………………… |
6 |
|
Аминокислоты …………………………………………………………………… |
7 |
|
Транспорт аминокислот в клетку……………………………………. |
12 |
|
Как можно использовать аминокислоты в организме?…….. |
16 |
|
Сколько энергии получается из аминокислот?………………… |
18 |
|
Дыхательная цепь…………………………………………………………. |
23 |
|
Удаление карбоксильной группы …………………………………… |
25 |
|
Удаление аминогруппы…………………………………………………. |
28 |
|
Как обезвредить аммиак?……………………………………………… |
33 |
|
Синтез мочевины………………………………………………………….. |
34 |
|
Превращения аминокислот …………………………………………… |
36 |
|
Белки………………………………………………………………………………. |
38 |
|
Сколько белка должен есть среднестатистический кочка?.. |
40 |
|
Переваривание белка …………………………………………………… |
41 |
|
Ферменты ……………………………………………………………………….. |
45 |
|
Зависимость скорости ферментативной реакции от |
|
|
количества субстрата…………………………………………………….. |
47 |
|
Регуляция ферментов……………………………………………………. |
49 |
|
Классификация …………………………………………………………….. |
50 |
|
Липиды……………………………………………………………………………. |
52 |
|
Жирные кислоты…………………………………………………………… |
53 |
|
Эйкозаноиды ……………………………………………………………….. |
55 |
|
3 |
|
Фосфолипиды ………………………………………………………………. |
57 |
|
Гликолипиды ……………………………………………………………….. |
57 |
|
Триацилглицериды……………………………………………………….. |
58 |
|
Холестерол…………………………………………………………………… |
59 |
|
Путь липидов, начиная с твоего грязного рта ………………….. |
60 |
|
β-окисление жирных кислот ………………………………………….. |
66 |
|
Липопротеины……………………………………………………………… |
70 |
|
Кетоновые тела…………………………………………………………….. |
71 |
|
Углеводы…………………………………………………………………………. |
73 |
|
Всасывание углеводов ………………………………………………….. |
76 |
|
Биохимическое чудо …………………………………………………….. |
77 |
|
Глюкоза ……………………………………………………………………….. |
82 |
|
Гликоген………………………………………………………………………. |
84 |
|
Гликолиз………………………………………………………………………. |
87 |
|
Челночные механизмы………………………………………………….. |
95 |
|
Алкогольная биохимия………………………………………………… |
100 |
|
Глюконеогенез……………………………………………………………. |
102 |
|
Пентозофосфатный путь………………………………………………. |
105 |
|
Биохимия жёсткого диска ……………………………………………….. |
108 |
|
Переваривание…………………………………………………………… |
108 |
|
Пиримидины………………………………………………………………. |
109 |
|
Пурины………………………………………………………………………. |
115 |
|
Как гормоны влияют на жизнь…………………………………………. |
121 |
|
4 |
|
Циклический аденозинмонофосфат (цАМФ) …………………. |
122 |
|
Гемостаз………………………………………………………………………… |
126 |
|
Биохимия жировой ткани………………………………………………… |
134 |
5
Введение
Биохимия на 2 курсе меда – это как изучение произведений Льва Толстого в 5 классе школы. Или как объяснение сопротивления материалов сибирской лайке. Студент, не видевший клинических дисциплин и не работавший с болезнями, не понимает, на кой хер ему эта всратая биохимия. Да, студенту говорили, что это важно и надо учиться, что это пригодиться и всё такое, но студент не понимает.
При этом биохимия абсолютно логично изучается перед клиническими дисциплинами, ведь терапию, например, не понять без фундаментальных наук. Получается вот такой парадокс, выход из которого я вижу только в повторном изучении биохимии человека.
Итак, биохимия – это наука, изучающая химический состав человека и химические процессы, составляющие жизнедеятельность человека. Без биохимических процессов человек не может даже пёрнуть. Абсолютно любое действо внутри человека является следствием химической реакции.
Даже мыслительный процесс является просто набором химических реакций в головном мозге. Сейчас ты об этом задумался, а на самом деле это биохимические реакции в твоём мозге пытаются осознать сами себя.
6
Аминокислоты
Аминокислоты – это то, на что дрочит каждая кочка, выкладывая последние шекели за банку протеина. Ведь аминокислоты являются кирпичами нашего тела.
Аминокислот в природе тысячи разновидностей, но белки строятся всего из двадцати. Это одно из гениальнейших изобретений природы – всего 20 аминокислот могут собираться в разном порядке и организовывать сложнейшие белки, функции которых обеспечивают нашу жизнь. Одни белки делают возможным сокращения мышц, другие белки борются с инфекционными агентами, третьи помогают переварить и вывести весь пятничный алкоголь из крови и начать субботу с пробежки.
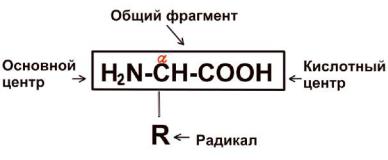
Перейдём к структуре аминокислот. Все они имеют общую часть молекулы.
Основный центр – это положительно заряженная часть молекулы, которая называется аминогруппой. Кислотный центр заряжен отрицательно и называется карбоксильной группой. А радикал у каждой аминокислоты свой.
7
Классификаций у аминокислот несколько.
1.Альфа, бета, гамма-аминокислоты. Определяются по атому углерода, к которому крепится аминогруппа. «Альфа» на предыдущем рисунке обозначает, что аминогруппа присосалась к первому углероду после карбоксильной группы.
2.По реакции аминокислоты бывают: кислые, основные и нейтральные.
3.Некоторые аминокислоты могут синтезироваться прямо в твоём организме, поэтому аминокислоты можно разделить на заменимые и незаменимые.
4.По конфигурации различают D и L-формы. Белки получаются только из L, поэтому особого смысла в этой классификации нет.
Так как аминокислот, из которых мы состоим, меньше, чем волос под твоим носом, тебе придётся выучить формулу каждой из них. Пригодится ли это тебе в работе врача? Нет. Пригодится ли тебе это хоть где-то после экзамена по биохимии? Вряд ли. Но зато, выучив формулы, ты будешь хорошо представлять себе, с чем работаешь. Без подобного тупого запоминания нельзя выстроить базу, на которой будут надёжно стоять твои клинические знания. Человек – довольно сложная машина, но это не повод отлынивать от изучения основных узлов и агрегатов.
8
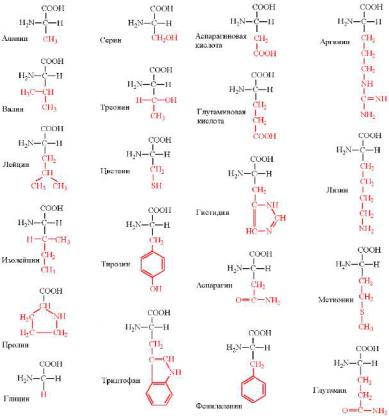
Эта великолепная двадцатка – твоё первое задание. Просто выучи формулы. Отпечатай в своей памяти. Ты можешь забыть имя своей сестры или забыть, на какой сигнал светофора надо переходить дорогу, но формулы аминокислот ты должен знать в лицо. Применяй ассоциации/стишки/молитвы – мне похуй, лишь бы выучил.
9
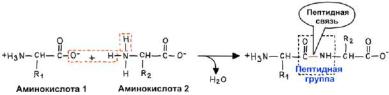
Аминокислоты могут соединяться друг с другом в цепочку, как «человеческая многоножка», образуя пептиды, полипептиды и белки. Отличить одно от другого можно по количеству аминокислот в цепочке: до 10 аминокислот – пептид, до 40 – полипептид, 40 и больше – белок.
Связь, которая возникает между двумя аминокислотами называется половой пептидной. Она образуется между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты. Карбоксильные и аминогруппы есть и в радикалах, но они не участвуют в пептидной связи, это позволено только альфа-группам, которые крепятся к первому углероду. Радикалы же болтаются по разные стороны.
Аминокислоты сшиваются между собой рибосомами, за что им большое спасибо. Если ты смотришь на эту реакцию и не понимаешь, почему от углерода отходят четыре палочки, а от азота всего три, то закрой нахуй биохимию и открой учебник по химии за 8 класс.
10
Соседние файлы в предмете Клиническая биохимия
- #
- #
- #
- #
- #
Загрузить PDF
Загрузить PDF
Биохимия соединяет в себе биологию и химию. Эта наука занимается изучением метаболических путей (химических превращений) в живых организмах на клеточном уровне.[1]
Помимо того, что биохимия изучает метаболические пути в растениях и микроорганизмах, она является экспериментальной наукой, для занятий которой необходимо соответствующее специальное оборудование. Эта обширная наука базируется на ряде основных понятий и идей, которые изучают в начале курса биохимии.
-
1
Запомните структуру аминокислот. Аминокислоты являются строительными кирпичиками, из которых сложены все белки. При изучении биохимии необходимо запомнить структуру и свойства всех 20 аминокислот. Выучите их однобуквенные и трехбуквенные обозначения, чтобы вы могли легко распознавать их в дальнейшем.[2]
- Изучите пять групп аминокислот, по четыре кислоты в каждой группе.
- Запомните важные свойства аминокислот, такие как заряд и полярность.
- Вновь и вновь чертите структуру аминокислот до тех пор, пока она не отложится в вашей памяти.
-
2
Ознакомьтесь со структурой белков. Белки состоят из цепочек аминокислот. Для знания основ биохимии необходимо распознавать различные уровни структуры белков и уметь изобразить наиболее важные из них (альфа-спирали и бета-листы). Существует четыре уровня структуры белков:[3]
- Первичная структура представляет собой линейное расположение аминокислот.
- Вторичная структура соответствует участкам белка в виде альфа-спиралей и бета-листов.
- Третичная структура — это трехмерное строение молекулы белка, которое обусловлено взаимодействием аминокислот. Это физиологическая форма белка. Третичная структура многих белков все еще неизвестна.
- Четвертичная структура возникает в результате взаимодействия нескольких белков, которые образуют более крупную молекулу белка.
-
3
Узнайте об уровне pH. Уровень pH раствора характеризует его кислотность. Он указывает на количество присутствующих в растворе ионов водорода и гидроксид-ионов. В кислых растворах содержится больше ионов водорода и сравнительно мало гидроксид-ионов. И наоборот, в щелочных растворах преобладают гидроксид-ионы.[4]
- Кислоты выполняют роль доноров ионов водорода (H+).
- Щелочи являются акцепторами ионов водорода (H+).
-
4
Научитесь определять pKa раствора. Константа диссоциации кислоты Ka показывает, насколько легко кислота отдает ионы водорода в данном растворе. Эта константа определяется как Ka = [H+][A—]/[HA]. Для большинства растворов Ka можно найти по таблицам в справочниках или интернете. Величина pKa определяется как отрицательный десятичный логарифм константы Ka.[5]
- Сильные кислоты имеют очень низкие значения pKa.
-
5
Научитесь находить pH по pKa с помощью уравнения Гендерсона-Гассельбаха. Это уравнение используют для приготовления буферных растворов в лабораторных условиях.[6]
Уравнение Гендерсона-Гассельбаха записывается в следующем виде: pH = pKa + lg [основание]/[кислота]. Величина pKa раствора равна уровню pH данного раствора в том случае, если концентрации кислоты и основания одинаковы.[7]
- Буферным называется такой раствор, уровень pH которого не меняется при добавлении умеренного количества кислоты или основания. Такие растворы важны для поддержания постоянного уровня pH.[8]
- Буферным называется такой раствор, уровень pH которого не меняется при добавлении умеренного количества кислоты или основания. Такие растворы важны для поддержания постоянного уровня pH.[8]
-
6
Узнайте об ионных и ковалентных химических связях. Ионная связь между атомами возникает в том случае, если один или несколько электронов переходят от одного атома к другому. В результате образуются положительный и отрицательный ионы, которые притягиваются друг к другу. При ковалентной связи атомы обмениваются электронными парами.[9]
- Важны и другие виды взаимодействия, такие как водородная связь, при которой возникает притяжение между атомами водорода и молекулами с высокой электроотрицательностью.[10]
- Тип связи между атомами определяет некоторые свойства молекул.
- Важны и другие виды взаимодействия, такие как водородная связь, при которой возникает притяжение между атомами водорода и молекулами с высокой электроотрицательностью.[10]
-
7
Узнайте о ферментах. Ферменты представляют собой белки, которые играют важную роль в организме — они катализируют (ускоряют) биохимические реакции. Почти каждая биохимическая реакция в организме ускоряется с помощью определенного фермента, поэтому изучение каталитического действия ферментов является важнейшей задачей биохимии. Каталитические механизмы исследуются главным образом с точки зрения кинетики.[11]
- Ингибирование ферментов используется в фармакологии для лечения многих видов болезней.
Реклама
-
1
Почитайте о метаболических путях и изучите соответствующие диаграммы. Существует множество важных метаболических путей, которые следует запомнить при изучении биохимии. В частности, к таким путям относятся: гликолиз, окислительное фосфорилирование, цикл трикарбоновых кислот (цикл Кребса), дыхательная цепь переноса электронов, фотосинтез.[12]
- Почитайте описание метаболических путей и изучите их изображения на диаграммах.
- Не исключено, что на экзамене вас попросят нарисовать полную схему того или иного метаболического пути.
-
2
Изучайте один путь за раз. Если вы попытаетесь одновременно выучить все метаболические пути, то запутаетесь и не сможете как следует запомнить ни один из них. Сосредоточьтесь на одном пути и посвятите ему несколько дней, прежде чем перейти к изучению следующего.
- После того как вы запомните какой-либо путь, постарайтесь не забыть его. Почаще рисуйте этот путь, чтобы освежить память.
-
3
Начертите основной путь. Начинайте с изучения основного метаболического пути. Некоторые пути представляют собой повторяющиеся циклы (цикл трикарбоновых кислот), другие имеют вид линейного процесса (гликолиз).[13]
Для начала запоминайте форму пути, где он начинается, какие вещества при этом распадаются и какие синтезируются.- В начале каждого цикла имеются исходные молекулы, такие как никотинамидадениндинуклеотид, аденозиндифосфат (АДФ) или глюкоза, и конечные продукты, например аденозинтрифосфат или гликоген. В первую очередь запомните исходные вещества и конечные продукты.
-
4
Изучите коферменты и метаболиты. Теперь ознакомьтесь с данным путем более подробно. Метаболиты представляют собой промежуточные продукты, которые образуются в ходе процесса, они используются в последующих реакциях. Существуют также коферменты, которые делают реакцию возможной или ускоряют ее.[14]
- Не заучивайте материал автоматически, без понимания. Обращайте внимание на то, как одни вещества превращаются в другие, чтобы действительно понимать данный процесс, а не просто вызубрить его.[15]
- Не заучивайте материал автоматически, без понимания. Обращайте внимание на то, как одни вещества превращаются в другие, чтобы действительно понимать данный процесс, а не просто вызубрить его.[15]
-
5
Запишите необходимые ферменты. Конечный этап в изучении метаболического пути заключается в том, чтобы добавить к нему ферменты, необходимые для протекания реакций. Такое поэтапное запоминание пути облегчит вашу задачу. Вы завершите изучение метаболического пути после того, как запомните названия соответствующих ферментов.[16]
- После этого вы легко сможете записать все белки, метаболиты и молекулы, которые участвуют в данном метаболическом пути.
-
6
Регулярно повторяйте изученные пути. Информацию подобного типа следует еженедельно освежать в памяти, иначе вы забудете ее. Каждый день повторяйте какой-то метаболический путь. К концу недели вы повторите все пути и сможете начать заново на следующей неделе.
- Когда подойдет время контрольной работы или экзамена, вам не придется лихорадочно заучивать метаболические пути, поскольку вы уже будете их знать.
Реклама
-
1
Читайте учебник. Чтение учебника необходимо при изучении любого предмета. Перед занятиями прочитайте соответствующий материал.[17]
Составьте краткий конспект того, что вы прочитали, — это позволит вам лучше подготовиться к занятиям.- Читайте вдумчиво. После каждого раздела делайте краткие пометки и записывайте наиболее важные моменты.
- Попробуйте ответить на некоторые вопросы в конце раздела, чтобы проверить, как вы усвоили материал.
-
2
Внимательно изучайте приведенные в учебнике рисунки. Эти рисунки содержат много важной информации и помогают лучше представить то, о чем рассказано в тексте. Часто намного легче понять что-либо, если взглянуть на рисунок, а не только прочитать текст.
- Переносите важные рисунки в свой конспект, чтобы в дальнейшем вы могли вернуться к ним.
-
3
Отмечайте свои записи разными цветами. В биохимии есть множество сложных процессов. Разработайте для своих записей систему цветов. Например, можно отмечать одним цветом сложный материал, а другой цвет использовать для простого и понятного вам материала.
- Используйте подходящую вам систему. Не переписывайте бездумно конспект своего друга — так вы не добьетесь лучшего понимания материала.
- Не переусердствуйте. Хотя слишком большое количество разных цветов и придаст вашему конспекту красочный вид, это не облегчит понимание материала.[18]
-
4
Задавайте вопросы. При чтении учебника записывайте возникающие у вас вопросы, а затем задавайте их в ходе лекции. Не бойтесь поднимать руку. Если вам что-нибудь не ясно, вполне возможно, что у других студентов также возникли вопросы по этому поводу.
- Если вы не успели задать какие-то вопросы в ходе лекции, попробуйте поговорить с преподавателем после занятий.
-
5
Сделайте карточки.[19]
В биохимии есть множество специальных терминов, с которыми вы могли не сталкиваться раньше. Выучите основные термины в начале курса, чтобы затем лучше понимать базирующиеся на них более сложные идеи и концепции.- Сделайте карточки с новыми терминами в бумажном или электронном виде. В последнем случае вы сможете записать их на свой мобильный телефон.
- Когда у вас выдастся свободная минутка, доставайте карточки и просматривайте их.
Реклама
Об этой статье
Эту страницу просматривали 21 581 раз.
Была ли эта статья полезной?
БХ — наверное первый экзамен, который учить было хотя бы приятно. Наверное именно поэтому я ничто до этого так не готовил, как биохимию. Как бы я к «стандартной схеме», то есть изучению предмета весь год добавил ещё и непосредственную подготовку перед экзаменом. Наверное потому, что я чувствовал реальное отношение биохимии к медицине, я так стал её учить. Да, в некоторых моментах в течение года было лень, но их явно меньше чем в той же философии. Так, вот. За 4 дня до экзамена я плотно читал лекции, да кстати лекции по БХ — пожалуй одни из самых полезных. Пользовался только ими при подготовке и к семинарам и к экзамену. В особо сложных(или пропущенных) вопросах — Северин. Те учебники, что нам выдали можно было сразу сдать. Читал лекции, повторял поступательно с начала годы по темам. Так продолжалось до последнего дня. В него я прорешал все до единой задачи, и в основном учил циклы(ЦТК, орнитиновый, гликолизы, синтез кетоновых). Реально оценивая свои силы, я понимал, что задачу я скорее всего решу и всё зависило от вопросов которые попадут. Как известно, если ты не любишь какую-то тему именно она тебе и попадается. Перейдём к экзамену.
Пятое число. Я выспавшийся, довольный собой приезжаю на БФК к 8:00. Там уже полно людей. Хотя экзамен в 8:30. Поболтав и обсудив, что никто ничего не знает, нас определили в кабинет с Ерлыкиной и Кузьминой. Первая десятка пошла и я был десятым. Обстановка, как на экзамене(странно для экзамена): в углу один принимающий, у доски другой, куча зачёток, вещи на стуле, все сидят более-менее далеко друг от друга, не шороха ни вдоха, пока не начался сам экзамен. Тяну билет с задачей, задача про жирные кислоты, Билет №12. Первый вопрос(как Олег и догадывался) — Транскрипция. Рнк-полимераза и другие ферменты. Посттранскрипционный процессинг. Влияние антибиотиков. Второй вопрос я тут целиком не напишу, он был слишком большим по формулировке — примерно Мочевина и аммонийные соли и всё о них. Роль аспартата и малата. Происхождение атомов азота. Нарушение синтеза. Гипераммонемии. Азотный остаток. Патологии с азотным остатком. Я сел готовиться, написал весь второй вопрос с задаче и ждал, как все своей очереди. Зав. каф. — золотой человек, ищет в людях знания и ставит за них. Кузьмина — может и посучить, особенно если ты мало говоришь и не отвечаешь ей на вопросы. Я попал к Ерлыкиной. Довольно быстро ответил ей свой билет, на что получил высказывание типа «У тебя один вопрос полностью выпал, а два других хорошо. Дополнительный и 4.» Как итог я с тройкой ухожу домой, потому что не знаю особенности грудного молока и жиров грудного молока. Но мне не привыкать быть на грани между 4 и 3 и получать 3, поэтому я не сильно расстроенный поехал домой.
В заключении как всегда трём типам. Списать труднее чем, на анате или гисте, так что продумайте всё хорошо. Микронаушник, ну может и поможет, но на 3 или 4 потому, что когда садишься отвечать тут не спрашивают конкретно твой билет, уходят в сторону от твоих вопросов тоже. Нёрды, можее быть спокойны. Вы задротили не зря, вас скорее всего освободили от экзамена, потому что от БХ не так трудно освободиться. Достаточно не получать 3 за колки и ходить на кружок, ну и в конце года работу защитить. Типичные, этот экзамен не является сложным, поверьте. Просто всю биохимию возможно повторить за 4-5 дней, а в голове у вас за год обучения что-то да осталось. Пишите лекции, учите лекции, любите лекции. Тяните фартовый билет и не попадайте к Кузьминой, чтоб не засучили.
Download Article
Download Article
Biochemistry joins the study of biology with the study of chemistry to explore the metabolic pathways at the cellular level in organisms. In addition to its application to the study of metabolic pathways in plants and microorganisms, biochemistry is an experimental science that relies heavily on the availability of specific instrumentation unique to this discipline. It is a broad topic, but there are some basic concepts that will be covered in any beginning biochemistry course.
-
1
Memorize the structure of amino acids. Amino acids are the building blocks of all proteins. Memorizing the structure and properties of all 20 amino acids is an essential aspect of biochemistry. Know their single and triple letter abbreviations to quickly recognize them while studying. Making flashcards is a great way to memorize the structures of amino acids.[1]
- Learn the amino acids in 5 groups of 4.
- Memorize essential properties such as acidic (negatively charged) versus basic (positively charged) and polar versus hydrophobic.
- Draw their structures over and over until you have them committed to memory. Fortunately, the amino acids have similar structures. They each contain a basic amino group (−NH2), an acidic carboxyl group (−COOH), and a hydrogen group (-H). They are distinguished by an organic R group (or side chain), which determines their function and is unique to each amino acid.
-
2
Recognize protein structures. Proteins are composed of chains of amino acids. Recognizing the various levels of protein structures and being able to draw the important ones (alpha helices and beta sheets) are fundamental concepts in biochemistry. There are four levels of protein structure:
- Primary structure is the linear arrangement of amino acids. They are held together by peptide bonds in a polypeptide chain.
- Secondary structure makes up the sections of proteins that fold into alpha helices and beta sheets, which are driven by hydrogen bonding.
- Tertiary structure is the three-dimensional structure resulting from the interactions between amino acids, usually driven by disulfide bonds, hydrogen bonding, and hydrophobic interactions. It is the physiological shape of the protein. The tertiary structure of many proteins is still unknown.
- Quaternary structure results from multiple separate proteins interacting together to form one larger, single protein. They often contain subunits and are globular.
Advertisement
-
3
Understand the pH scale. The pH of a solution is a measure of acidity. This is related to the amount of hydrogen and hydroxide ions present in the solution. An acidic solution has more hydrogen ions present in the solution and fewer hydroxide ions. The opposite is true for basic solutions: more hydroxide ions, fewer hydrogen ions.[2]
- Acids are hydrogen ion (H+) donors and have a pH < 7.
- Bases are hydrogen ion (H+) acceptors and have a pH > 7.
-
4
Define the pKa of a solution. The Ka of a solution is used to predict the extent of acid dissociation or how readily the acid gives up its hydrogen ions. It is defined by the equation Ka = [H+][A—]/[HA]. The Ka of most solutions can be located in a table in your textbook or online. The pKa is defined as the negative log of the Ka.[3]
- Strong acids dissociate completely and have very small pKas. Weak acids dissociate incompletely and have higher pKas.
-
5
Relate pH and pKa using the Henderson-Hasselbalch Equation. The Henderson-Hasselbalch Equation is used to prepare buffers for solutions in the laboratory.[4]
It is also used in acid-base reactions to find the equilibrium pH. The equation states that pH = pKa + log [base]/[acid]. The pKa of a solution is equal to the pH of the solution when the concentrations of the acid and the base are the same.[5]
- A buffer is a solution that resists changes in pH when small amounts of acidic or basic solutions are added to it. They are important for keeping solutions at a stable pH.[6]
Buffers are also important in biological systems, such as keeping the human body at a pH of 7.4.
- A buffer is a solution that resists changes in pH when small amounts of acidic or basic solutions are added to it. They are important for keeping solutions at a stable pH.[6]
-
6
Recognize ionic and covalent bonds. An ionic bond forms between atoms when one or more electrons is removed from one atom and donated to the other atom. The resulting positive and negatively charged ions then attract each other. Covalent bonds form when two atoms share pairs of electrons.[7]
- Other forces such as hydrogen bonds (attractive forces between hydrogen atoms and highly electronegative molecules) are also important.[8]
- The type of bond formed between atoms determines some of the properties that molecule will have.
- Other forces such as hydrogen bonds (attractive forces between hydrogen atoms and highly electronegative molecules) are also important.[8]
-
7
Learn about enzymes. Enzymes are an important class of proteins in the body that are used to catalyze (increase the speed of) biochemical reactions by lowering activation energy. Almost every biochemical reaction in the body is catalyzed by a specific type of enzyme; therefore, the investigation of the mechanism of enzymatic function is a major subject in biochemistry. It is investigated mostly from the kinetic point of view.[9]
- Enzyme inhibition is used pharmacologically to treat many types of diseases that affect the body.
- Enzymes do not change or get used up in reactions, so they can perform many rounds of catalysis.
Advertisement
-
1
Read and study the figures of the pathway. There are a number of essential metabolic pathways you will have to memorize when taking biochemistry: glycolysis, oxidative phosphorylation, the citric acid cycle (Krebs Cycle), the electron transport chain, and photosynthesis, to name a few.
- Read the associated text in your book and study the figure detailing the process of the pathway.
- It’s likely that you will need to be able to draw the entire cycle on a test.
-
2
Learn one pathway at a time. If you try to study all of the pathways at once, you will confuse them and won’t have a strong foundation for any of them. Focus on learning one pathway and review that pathway for a few days before you move onto the next one.
- Once you have learned one, don’t let it fade away. Redraw it often to make sure you keep it fresh in your mind.
- Take online quizzes or have a friend quiz you so the metabolic pathways stay fresh in your mind.
-
3
Draw the basic pathway. When you first start learning, start with the basic pathway. Some pathways are a cycle that continue (the citric acid cycle) while other pathways are a linear process (glycolysis). Start learning by memorizing the shape of the pathway, where the pathway starts, what gets broken down, and what gets synthesized.
- For each cycle, you will have starting molecules such as NADH, ADP, or glucose, and end products such as ATP and glycogen. Memorize these general pieces first.
-
4
Add in the cofactors and metabolites. Now get more specific with the pathway. Metabolites are intermediate molecules that get formed during the process, but then get used up as the reaction continues. There are also cofactors that are required for or help to increase the rate of the reaction.[10]
- Avoid memorizing for the sake of memorizing. Learn how each intermediate transforms into the next so that you have an actual understanding of the process instead of just rote memorization.[11]
- Avoid memorizing for the sake of memorizing. Learn how each intermediate transforms into the next so that you have an actual understanding of the process instead of just rote memorization.[11]
-
5
Draw in the necessary enzymes. The final step to memorizing the pathway is adding in the enzymes necessary to carry out the reaction. Learning the pathway in pieces like this will make it less overwhelming to start with. Once you learn all the names of the enzymes, you will have the whole pathway finished.[12]
- You should now be able to easily write out every protein, metabolite, and molecule involved in the metabolic pathway.
- Make sure you know which steps of the pathway are irreversible and why (if applicable).
-
6
Review the pathways frequently. This type of information needs to be reviewed and redrawn on a weekly basis or else you will forget it. Take time each day to review a different pathway, and be sure you know where in the body it takes place. By the end of the week you will have reviewed them all and then you can start all over the next week.
- When test time comes around, you won’t have to worry about learning all of the metabolic pathways because you will have already have them memorized.
Advertisement
-
1
Read the textbook. Reading the textbook for any course you take is essential for studying the subject. Before class, read and review the material that will be covered that day.[13]
Take notes on what you read and you will be better prepared for class.- Be sure to read for comprehension. At the end of each section, summarize the material in your notes.
- Try answering some of the questions at the end of the chapter to check your understanding of the concepts.
-
2
Study the figures of the textbook. The figures of your textbook are very detailed and help to visualize what the text is telling you. Oftentimes, it is much easier to understand a concept by looking at a picture of it than just reading words.
- Redraw important figures in your notes to go back and study later.
-
3
Color code your notes. There are many complicated processes in biochemistry. Develop and use a color coding system for your notes. Maybe write your notes based on difficulty with one color representing really complicated concepts and another color, concepts you easily remember and understand.
- Use a system that works for you. Don’t just copy your friend’s notes and hope it makes you better at studying.
- Avoid overdoing it. Using too many different colors will turn your notes into a rainbow, but will not be as useful.[14]
-
4
Ask questions. While you are reading the textbook, write down questions on statements or concepts that are confusing. Ask questions during lecture as well. Don’t be afraid to raise your hand. If you have a question, it’s likely that other people in the class have the same question.
- Seek out your teacher to ask questions that may not have been answered during class time.
-
5
Make flashcards.[15]
There are a lot of vocabulary words associated with biochemistry that you may not have seen before, and many of the words are similar. Learning these words and the differences between them in the beginning will help you understand the concepts later that build upon this vocabulary.- Write out paper flashcards or make digital flashcards that you can carry with you on your phone.
- Whenever you have downtime, take out your flashcards and flip through them.
Advertisement
Add New Question
-
Question
What is the structure of paracetamol?
C8H9NO2 — eight carbons attached to nine hydrogens and a nitro group.
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
-
Biochemistry is centered around a finite number of reactions that are used over and over again.
-
Aim to learn concepts rather than memorize facts.
-
Always try to relate the specifics back to the big picture and try to relate topics to one another.
Advertisement
Video
About This Article
Thanks to all authors for creating a page that has been read 80,953 times.
Did this article help you?
Download Article
Download Article
Biochemistry joins the study of biology with the study of chemistry to explore the metabolic pathways at the cellular level in organisms. In addition to its application to the study of metabolic pathways in plants and microorganisms, biochemistry is an experimental science that relies heavily on the availability of specific instrumentation unique to this discipline. It is a broad topic, but there are some basic concepts that will be covered in any beginning biochemistry course.
-
1
Memorize the structure of amino acids. Amino acids are the building blocks of all proteins. Memorizing the structure and properties of all 20 amino acids is an essential aspect of biochemistry. Know their single and triple letter abbreviations to quickly recognize them while studying. Making flashcards is a great way to memorize the structures of amino acids.[1]
- Learn the amino acids in 5 groups of 4.
- Memorize essential properties such as acidic (negatively charged) versus basic (positively charged) and polar versus hydrophobic.
- Draw their structures over and over until you have them committed to memory. Fortunately, the amino acids have similar structures. They each contain a basic amino group (−NH2), an acidic carboxyl group (−COOH), and a hydrogen group (-H). They are distinguished by an organic R group (or side chain), which determines their function and is unique to each amino acid.
-
2
Recognize protein structures. Proteins are composed of chains of amino acids. Recognizing the various levels of protein structures and being able to draw the important ones (alpha helices and beta sheets) are fundamental concepts in biochemistry. There are four levels of protein structure:
- Primary structure is the linear arrangement of amino acids. They are held together by peptide bonds in a polypeptide chain.
- Secondary structure makes up the sections of proteins that fold into alpha helices and beta sheets, which are driven by hydrogen bonding.
- Tertiary structure is the three-dimensional structure resulting from the interactions between amino acids, usually driven by disulfide bonds, hydrogen bonding, and hydrophobic interactions. It is the physiological shape of the protein. The tertiary structure of many proteins is still unknown.
- Quaternary structure results from multiple separate proteins interacting together to form one larger, single protein. They often contain subunits and are globular.
Advertisement
-
3
Understand the pH scale. The pH of a solution is a measure of acidity. This is related to the amount of hydrogen and hydroxide ions present in the solution. An acidic solution has more hydrogen ions present in the solution and fewer hydroxide ions. The opposite is true for basic solutions: more hydroxide ions, fewer hydrogen ions.[2]
- Acids are hydrogen ion (H+) donors and have a pH < 7.
- Bases are hydrogen ion (H+) acceptors and have a pH > 7.
-
4
Define the pKa of a solution. The Ka of a solution is used to predict the extent of acid dissociation or how readily the acid gives up its hydrogen ions. It is defined by the equation Ka = [H+][A—]/[HA]. The Ka of most solutions can be located in a table in your textbook or online. The pKa is defined as the negative log of the Ka.[3]
- Strong acids dissociate completely and have very small pKas. Weak acids dissociate incompletely and have higher pKas.
-
5
Relate pH and pKa using the Henderson-Hasselbalch Equation. The Henderson-Hasselbalch Equation is used to prepare buffers for solutions in the laboratory.[4]
It is also used in acid-base reactions to find the equilibrium pH. The equation states that pH = pKa + log [base]/[acid]. The pKa of a solution is equal to the pH of the solution when the concentrations of the acid and the base are the same.[5]
- A buffer is a solution that resists changes in pH when small amounts of acidic or basic solutions are added to it. They are important for keeping solutions at a stable pH.[6]
Buffers are also important in biological systems, such as keeping the human body at a pH of 7.4.
- A buffer is a solution that resists changes in pH when small amounts of acidic or basic solutions are added to it. They are important for keeping solutions at a stable pH.[6]
-
6
Recognize ionic and covalent bonds. An ionic bond forms between atoms when one or more electrons is removed from one atom and donated to the other atom. The resulting positive and negatively charged ions then attract each other. Covalent bonds form when two atoms share pairs of electrons.[7]
- Other forces such as hydrogen bonds (attractive forces between hydrogen atoms and highly electronegative molecules) are also important.[8]
- The type of bond formed between atoms determines some of the properties that molecule will have.
- Other forces such as hydrogen bonds (attractive forces between hydrogen atoms and highly electronegative molecules) are also important.[8]
-
7
Learn about enzymes. Enzymes are an important class of proteins in the body that are used to catalyze (increase the speed of) biochemical reactions by lowering activation energy. Almost every biochemical reaction in the body is catalyzed by a specific type of enzyme; therefore, the investigation of the mechanism of enzymatic function is a major subject in biochemistry. It is investigated mostly from the kinetic point of view.[9]
- Enzyme inhibition is used pharmacologically to treat many types of diseases that affect the body.
- Enzymes do not change or get used up in reactions, so they can perform many rounds of catalysis.
Advertisement
-
1
Read and study the figures of the pathway. There are a number of essential metabolic pathways you will have to memorize when taking biochemistry: glycolysis, oxidative phosphorylation, the citric acid cycle (Krebs Cycle), the electron transport chain, and photosynthesis, to name a few.
- Read the associated text in your book and study the figure detailing the process of the pathway.
- It’s likely that you will need to be able to draw the entire cycle on a test.
-
2
Learn one pathway at a time. If you try to study all of the pathways at once, you will confuse them and won’t have a strong foundation for any of them. Focus on learning one pathway and review that pathway for a few days before you move onto the next one.
- Once you have learned one, don’t let it fade away. Redraw it often to make sure you keep it fresh in your mind.
- Take online quizzes or have a friend quiz you so the metabolic pathways stay fresh in your mind.
-
3
Draw the basic pathway. When you first start learning, start with the basic pathway. Some pathways are a cycle that continue (the citric acid cycle) while other pathways are a linear process (glycolysis). Start learning by memorizing the shape of the pathway, where the pathway starts, what gets broken down, and what gets synthesized.
- For each cycle, you will have starting molecules such as NADH, ADP, or glucose, and end products such as ATP and glycogen. Memorize these general pieces first.
-
4
Add in the cofactors and metabolites. Now get more specific with the pathway. Metabolites are intermediate molecules that get formed during the process, but then get used up as the reaction continues. There are also cofactors that are required for or help to increase the rate of the reaction.[10]
- Avoid memorizing for the sake of memorizing. Learn how each intermediate transforms into the next so that you have an actual understanding of the process instead of just rote memorization.[11]
- Avoid memorizing for the sake of memorizing. Learn how each intermediate transforms into the next so that you have an actual understanding of the process instead of just rote memorization.[11]
-
5
Draw in the necessary enzymes. The final step to memorizing the pathway is adding in the enzymes necessary to carry out the reaction. Learning the pathway in pieces like this will make it less overwhelming to start with. Once you learn all the names of the enzymes, you will have the whole pathway finished.[12]
- You should now be able to easily write out every protein, metabolite, and molecule involved in the metabolic pathway.
- Make sure you know which steps of the pathway are irreversible and why (if applicable).
-
6
Review the pathways frequently. This type of information needs to be reviewed and redrawn on a weekly basis or else you will forget it. Take time each day to review a different pathway, and be sure you know where in the body it takes place. By the end of the week you will have reviewed them all and then you can start all over the next week.
- When test time comes around, you won’t have to worry about learning all of the metabolic pathways because you will have already have them memorized.
Advertisement
-
1
Read the textbook. Reading the textbook for any course you take is essential for studying the subject. Before class, read and review the material that will be covered that day.[13]
Take notes on what you read and you will be better prepared for class.- Be sure to read for comprehension. At the end of each section, summarize the material in your notes.
- Try answering some of the questions at the end of the chapter to check your understanding of the concepts.
-
2
Study the figures of the textbook. The figures of your textbook are very detailed and help to visualize what the text is telling you. Oftentimes, it is much easier to understand a concept by looking at a picture of it than just reading words.
- Redraw important figures in your notes to go back and study later.
-
3
Color code your notes. There are many complicated processes in biochemistry. Develop and use a color coding system for your notes. Maybe write your notes based on difficulty with one color representing really complicated concepts and another color, concepts you easily remember and understand.
- Use a system that works for you. Don’t just copy your friend’s notes and hope it makes you better at studying.
- Avoid overdoing it. Using too many different colors will turn your notes into a rainbow, but will not be as useful.[14]
-
4
Ask questions. While you are reading the textbook, write down questions on statements or concepts that are confusing. Ask questions during lecture as well. Don’t be afraid to raise your hand. If you have a question, it’s likely that other people in the class have the same question.
- Seek out your teacher to ask questions that may not have been answered during class time.
-
5
Make flashcards.[15]
There are a lot of vocabulary words associated with biochemistry that you may not have seen before, and many of the words are similar. Learning these words and the differences between them in the beginning will help you understand the concepts later that build upon this vocabulary.- Write out paper flashcards or make digital flashcards that you can carry with you on your phone.
- Whenever you have downtime, take out your flashcards and flip through them.
Advertisement
Add New Question
-
Question
What is the structure of paracetamol?
C8H9NO2 — eight carbons attached to nine hydrogens and a nitro group.
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
-
Biochemistry is centered around a finite number of reactions that are used over and over again.
-
Aim to learn concepts rather than memorize facts.
-
Always try to relate the specifics back to the big picture and try to relate topics to one another.
Advertisement
Video
About This Article
Thanks to all authors for creating a page that has been read 80,953 times.