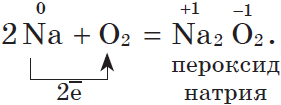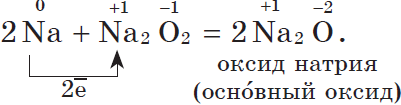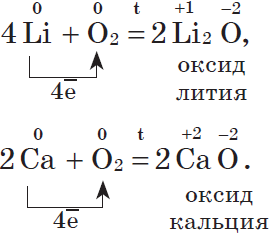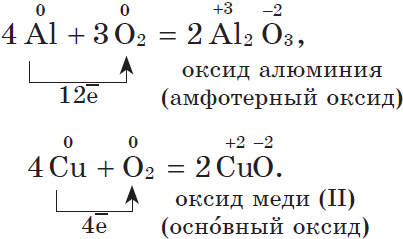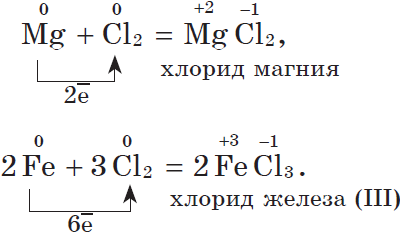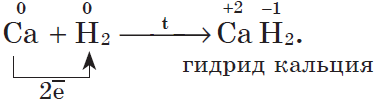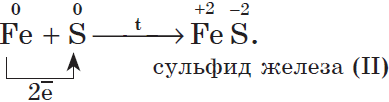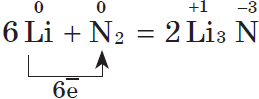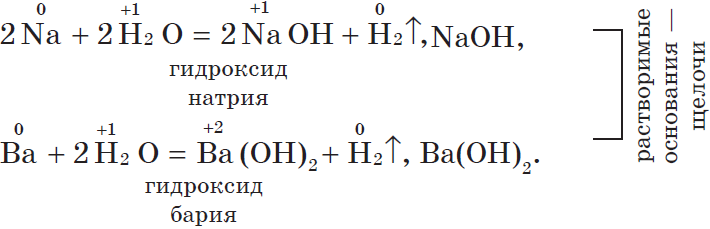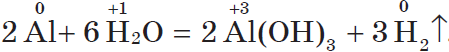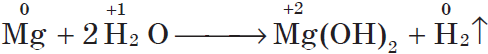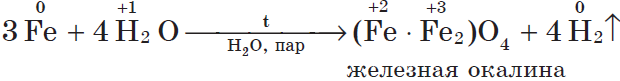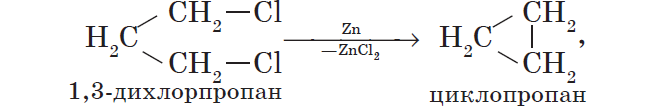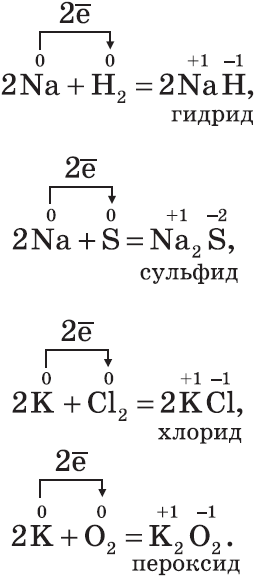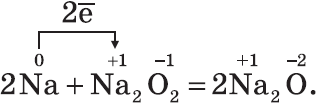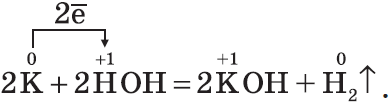Download Article
Download Article
Inorganic chemistry is the branch of chemistry dealing with the study of inorganic compounds (compounds without carbon), their properties, and their reactions with other compounds.[1]
Students usually find it difficult to excel in this subject because of the complexity of chemical equations and reactions. The best way to truly excel in inorganic chemistry is to devote time and energy to truly understand each fundamental concept before moving on to more complex ones.
-
1
Investigate the atom and its atomic structure. Being a branch of chemistry, inorganic chemistry requires that you understand the basic structure of an atom and the properties that arise from this structure. Knowing atomic structure and the way in which atoms can interact with each other is essential to excelling in inorganic chemistry.[2]
- Have a firm knowledge and understanding of atomic mass, electron configuration, atomic number, protons, neutrons, electrons, etc.
-
2
Memorize the periodic table. This may seem a little crazy, but memorizing the periodic table will help you have a fundamental understanding of the elements, how they’re arranged, and how they interact with each other. Knowing the group and period of an element gives you information about its structure, electron shells, valence electrons, and reactivity with other elements.[3]
- The columns of the periodic table are called “groups” while the rows are called “periods.”
- The table is split up into metals and non-metals.[4]
- Knowing the chemical symbol of an element will also help you when working with inorganic equations.
Advertisement
-
3
Understand chemical bonding of elements. The types of bonds that form between elements affect how a compound will react with other compounds. There are two main types of chemical bonding: ionic and covalent. Ionic bonds form when an electron is transferred from one atom to another while covalent bonds result from two atoms sharing an electron.[5]
- There are also attractive forces that allow for weak bonding between molecules called hydrogen bonds and van der Waals interactions.
- Bonding specifically between metal ions is referred to as metallic bonding.
-
4
Practice problems with all types of chemical reactions. Redox reactions, combustion, acid-base reactions, and decomposition are all types of reactions that you will see when working with inorganic chemistry. A good way to learn them is to understand the context in which these reactions are written.
- In books, many reactions are written for the same element to illustrate its chemical properties. Once you understand the basic concept, the rest should fall into place.
- Don’t forget to balance your reactions.[6]
-
5
Learn about coordination chemistry. A coordination compound forms when a molecule has a metal center and is bound to a ligand such as another atom, ion, or molecule that donates an electron to the metal. These compounds have properties different from that of the properties of each individual atom that comprises it.[7]
- The ligand and the complex geometries that result in these complexes are an important aspect of inorganic chemistry that must be mastered.
Advertisement
-
1
Reframe your thinking about inorganic chemistry. Stop thinking that you have to study only because you have to pass an exam or give a presentation. Learning this subject will undoubtedly help you in Organic and Physical Chemistry too as many concepts taught here are used in these fields as well. Additionally, inorganic chemistry is an essential building block for a career in medicine or chemical engineering.
- Find the fun in inorganic chemistry. Try to apply some of the concepts to the real world and solve real problems with what you’re learning.[8]
- Find the fun in inorganic chemistry. Try to apply some of the concepts to the real world and solve real problems with what you’re learning.[8]
-
2
Read your syllabus and prepare a study plan. At the beginning of the course, read through the syllabus and figure out how much time you think you will need to study inorganic chemistry each week. Read the corresponding chapters of the textbook before class.[9]
- Write up a study plan that designates certain topics to specific days of the week for study. Spreading out the studying over time will help you avoid cramming for the exam later.[10]
- Write up a study plan that designates certain topics to specific days of the week for study. Spreading out the studying over time will help you avoid cramming for the exam later.[10]
-
3
Designate regular time to this subject. The key to learning any subject is to study it regularly. Set aside an hour each day or maybe two hours every other day to focus specifically on inorganic chemistry. Read your textbook, answer practice problems, and use online resources to increase your understanding of the subject.
- Choose a time of day where you are most alert. If inorganic chemistry is the subject you struggle with the most, study it first so you are not too tired by other subjects.[11]
- Choose a time of day where you are most alert. If inorganic chemistry is the subject you struggle with the most, study it first so you are not too tired by other subjects.[11]
-
4
Study your lecture notes after each class session. You should review everything, paying special attention to concepts you found confusing. Look for areas where you have gaps so that you can follow-up on them before you get behind.
- If your instructor allows it, record the lectures so that you have all of the information. You should still take notes, however, as this will help you retain the information better.
-
5
Form a study group so that you can learn with others. Your study group will help keep you accountable to your study commitments. You’ll also be able to help each other better understand the material. You can solidify the information you know by teaching it to others, or you can have your gaps in knowledge filled in by the other people in your group.
- Choose a location for studying that will promote learning, such as the library.
-
6
Do lots of practice problems. Much of chemistry involves chemical reactions and determining how certain compounds will react with each other. The best way to master this subject is to do lots of practice problems of all types of reactions until you have a firm understanding of each one.[12]
- Redo your homework assignments, answer questions in the back of the book, and seek out more problems online.
-
7
Attend office hours. Your professor will have office hours at least once a week. Go to them and ask any questions you may have about the subject or the homework assignments. Office hours are specifically for you to have one-on-one time with your professor to discuss concepts that you didn’t fully understand during the lecture. Take advantage of them!
- If your professor’s office hours conflict with another one of your courses, ask your professor about scheduling another time to meet up and ask questions.
Advertisement
Add New Question
-
Question
How do I memorize inorganic chemical reactions?
MirsadaZ
Community Answer
First understand what happens in each reaction and be able to explain it with words. Then just write and balance it.
-
Question
How can I make potassium permaganate?
Potassium permanganate is commercially prepared by mixing solution of KOH and powdered manganese oxide, with oxidizing agents like potassium chlorate. The mixture is boiled evaporated and the residue is heated in iron pans until it has acquired a pasty consistency.
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
Video
References
About This Article
Article SummaryX
To excel in inorganic chemistry, start by writing a study plan that sets out regular slots for each topic so you don’t fall behind or feel rushed at exam time. When planning your study, give yourself sufficient time to understand the reactions and concepts, and if it’s a hard subject for you, try to choose times when you’re most alert, like early morning or before dinner. During study time, read your textbook and lecture notes, answer practice problems, and use online resources to help you learn and review. Since inorganic chemistry involves working out how certain compounds react with each other, do lots of practice problems on all types of reactions to find out what you still need to learn. You can do this by redoing homework assignments, answering questions from your textbook and looking for online practice tests. For more tips, including how to memorize inorganic chemistry basics, scroll down!
Did this summary help you?
Thanks to all authors for creating a page that has been read 64,472 times.
Did this article help you?
Download Article
Download Article
Inorganic chemistry is the branch of chemistry dealing with the study of inorganic compounds (compounds without carbon), their properties, and their reactions with other compounds.[1]
Students usually find it difficult to excel in this subject because of the complexity of chemical equations and reactions. The best way to truly excel in inorganic chemistry is to devote time and energy to truly understand each fundamental concept before moving on to more complex ones.
-
1
Investigate the atom and its atomic structure. Being a branch of chemistry, inorganic chemistry requires that you understand the basic structure of an atom and the properties that arise from this structure. Knowing atomic structure and the way in which atoms can interact with each other is essential to excelling in inorganic chemistry.[2]
- Have a firm knowledge and understanding of atomic mass, electron configuration, atomic number, protons, neutrons, electrons, etc.
-
2
Memorize the periodic table. This may seem a little crazy, but memorizing the periodic table will help you have a fundamental understanding of the elements, how they’re arranged, and how they interact with each other. Knowing the group and period of an element gives you information about its structure, electron shells, valence electrons, and reactivity with other elements.[3]
- The columns of the periodic table are called “groups” while the rows are called “periods.”
- The table is split up into metals and non-metals.[4]
- Knowing the chemical symbol of an element will also help you when working with inorganic equations.
Advertisement
-
3
Understand chemical bonding of elements. The types of bonds that form between elements affect how a compound will react with other compounds. There are two main types of chemical bonding: ionic and covalent. Ionic bonds form when an electron is transferred from one atom to another while covalent bonds result from two atoms sharing an electron.[5]
- There are also attractive forces that allow for weak bonding between molecules called hydrogen bonds and van der Waals interactions.
- Bonding specifically between metal ions is referred to as metallic bonding.
-
4
Practice problems with all types of chemical reactions. Redox reactions, combustion, acid-base reactions, and decomposition are all types of reactions that you will see when working with inorganic chemistry. A good way to learn them is to understand the context in which these reactions are written.
- In books, many reactions are written for the same element to illustrate its chemical properties. Once you understand the basic concept, the rest should fall into place.
- Don’t forget to balance your reactions.[6]
-
5
Learn about coordination chemistry. A coordination compound forms when a molecule has a metal center and is bound to a ligand such as another atom, ion, or molecule that donates an electron to the metal. These compounds have properties different from that of the properties of each individual atom that comprises it.[7]
- The ligand and the complex geometries that result in these complexes are an important aspect of inorganic chemistry that must be mastered.
Advertisement
-
1
Reframe your thinking about inorganic chemistry. Stop thinking that you have to study only because you have to pass an exam or give a presentation. Learning this subject will undoubtedly help you in Organic and Physical Chemistry too as many concepts taught here are used in these fields as well. Additionally, inorganic chemistry is an essential building block for a career in medicine or chemical engineering.
- Find the fun in inorganic chemistry. Try to apply some of the concepts to the real world and solve real problems with what you’re learning.[8]
- Find the fun in inorganic chemistry. Try to apply some of the concepts to the real world and solve real problems with what you’re learning.[8]
-
2
Read your syllabus and prepare a study plan. At the beginning of the course, read through the syllabus and figure out how much time you think you will need to study inorganic chemistry each week. Read the corresponding chapters of the textbook before class.[9]
- Write up a study plan that designates certain topics to specific days of the week for study. Spreading out the studying over time will help you avoid cramming for the exam later.[10]
- Write up a study plan that designates certain topics to specific days of the week for study. Spreading out the studying over time will help you avoid cramming for the exam later.[10]
-
3
Designate regular time to this subject. The key to learning any subject is to study it regularly. Set aside an hour each day or maybe two hours every other day to focus specifically on inorganic chemistry. Read your textbook, answer practice problems, and use online resources to increase your understanding of the subject.
- Choose a time of day where you are most alert. If inorganic chemistry is the subject you struggle with the most, study it first so you are not too tired by other subjects.[11]
- Choose a time of day where you are most alert. If inorganic chemistry is the subject you struggle with the most, study it first so you are not too tired by other subjects.[11]
-
4
Study your lecture notes after each class session. You should review everything, paying special attention to concepts you found confusing. Look for areas where you have gaps so that you can follow-up on them before you get behind.
- If your instructor allows it, record the lectures so that you have all of the information. You should still take notes, however, as this will help you retain the information better.
-
5
Form a study group so that you can learn with others. Your study group will help keep you accountable to your study commitments. You’ll also be able to help each other better understand the material. You can solidify the information you know by teaching it to others, or you can have your gaps in knowledge filled in by the other people in your group.
- Choose a location for studying that will promote learning, such as the library.
-
6
Do lots of practice problems. Much of chemistry involves chemical reactions and determining how certain compounds will react with each other. The best way to master this subject is to do lots of practice problems of all types of reactions until you have a firm understanding of each one.[12]
- Redo your homework assignments, answer questions in the back of the book, and seek out more problems online.
-
7
Attend office hours. Your professor will have office hours at least once a week. Go to them and ask any questions you may have about the subject or the homework assignments. Office hours are specifically for you to have one-on-one time with your professor to discuss concepts that you didn’t fully understand during the lecture. Take advantage of them!
- If your professor’s office hours conflict with another one of your courses, ask your professor about scheduling another time to meet up and ask questions.
Advertisement
Add New Question
-
Question
How do I memorize inorganic chemical reactions?
MirsadaZ
Community Answer
First understand what happens in each reaction and be able to explain it with words. Then just write and balance it.
-
Question
How can I make potassium permaganate?
Potassium permanganate is commercially prepared by mixing solution of KOH and powdered manganese oxide, with oxidizing agents like potassium chlorate. The mixture is boiled evaporated and the residue is heated in iron pans until it has acquired a pasty consistency.
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
Video
References
About This Article
Article SummaryX
To excel in inorganic chemistry, start by writing a study plan that sets out regular slots for each topic so you don’t fall behind or feel rushed at exam time. When planning your study, give yourself sufficient time to understand the reactions and concepts, and if it’s a hard subject for you, try to choose times when you’re most alert, like early morning or before dinner. During study time, read your textbook and lecture notes, answer practice problems, and use online resources to help you learn and review. Since inorganic chemistry involves working out how certain compounds react with each other, do lots of practice problems on all types of reactions to find out what you still need to learn. You can do this by redoing homework assignments, answering questions from your textbook and looking for online practice tests. For more tips, including how to memorize inorganic chemistry basics, scroll down!
Did this summary help you?
Thanks to all authors for creating a page that has been read 64,472 times.
Did this article help you?
САМОУЧИТЕЛЬ ПО ХИМИИ
Предлагаемый вашему вниманию Самоучитель — не обычный учебник по химии. В нём не просто излагаются какие-то факты, не просто описываются свойства веществ, как в обычном пособии. Этот курс по изучению химии объясняет и учит, особенно в тех случаях, если вы не можете или стесняетесь обратиться за разъяснениями к учителю. Данный самоучитель в виде рукописи использовался с 1991 г. школьниками, и не было ни одного ученика, который бы «провалился» на экзамене по химии и в школе, и в вузах. Большинство из них начинало с «нуля»!
Курс рассчитан на самостоятельную работу ученика. Главное, чтобы вы отвечали по ходу чтения на те вопросы, которые встречаются в тексте. Если вы не смогли ответить на вопрос, — читайте внимательнее ещё раз: все ответы имеются рядом. Желательно также выполнять все задания которые встречаются по ходу объяснения нового материала, а также задания ЕГЭ, которые взяты из реальных сборников ФИПИ разных лет издания. В этом вам помогут многочисленные обучающие алгоритмы, которые есть в каждой части Самоучителя по химии.
В интерактивном учебнике приведены, в основном, схемы химических реакций. Коэффициенты нужно расставлять самим, даже если об этом не сказано в задании. В конце каждого урока имеются упражнения, вопросы и задачи, которые проверяют степень усвоения предложенного материала. Если вы смогли, не подглядывая в текст урока, ответить на эти вопросы, сделать все упражнения, решить все задачи — замечательно. В противном случае ещё раз перечитайте урок.
В последних уроках самоучителя приведены также способы решения базовых задач по химии. В случае затруднений при решении задачи, условие которой имеется в конце главы, найдите эту задачу среди задач для самостоятельного решения в уроках 29–32, а потом посмотрите, как решается такая задача.
Изучив данный Самоучитель, вы сможете легко ответить на многие вопросы ЕГЭ и просто понять и, возможно, полюбить этот непростой, но очень интересный предмет ХИМИЯ.
Если ты готов, то дерзай! И да прибудет с тобой химия 🙂
ЕГЭ по химии состоит из тестовой и письменной частей. Из 34 заданий 28 тестовых и 6 письменных. Всего на экзамене по химии можно набрать 56 баллов — 36 в первой части и 20 во второй. Чтобы оставить себе место для ошибки, рекомендуем решать всю первую и всю вторую части. В статье разберем пять полезных советов преподавателей, чтобы успешно сдать экзамен.
Содержание:
- Лайфхак №1. Тренируйтесь в решении заданий блоками
- Лайфхак № 2. Ищите сходства и придумывайте ассоциации в неорганике
- Лайфхак №3. Заучивайте исключения
- Лайфхак №4. Тайм-менеджмент
- Лайфхак №5. Пользуйтесь шпаргалками из КИМа
- Что нужно взять на ЕГЭ по химии в 2023?
- Вывод
Лайфхак №1. Тренируйтесь в решении заданий блоками
В спецификаторах на сайте ФИПИ указаны темы, знание которых будет проверяться на экзамене. Экзаменационный материал разделен на следующие блоки:
- Теоретические основы химии (Общая химия).
- Неорганическая химия:
- оксиды;
- основания;
- амфотерные гидроксиды;
- кислоты;
- соли;
- соединения галогенов, кислорода, азота, фосфора, серы, углерода, кремния, металлов IA- и IIA-групп, алюминия, цинка, хрома, марганца, железа, меди, серебра.
- Органическая химия:
- алканы;
- алкены;
- алкины;
- алкадиены;
- циклоалканы;
- циклоалкены;
- арены;
- одноатомные и многоатомные спирты;
- фенолы;
- альдегиды;
- кетоны;
- карбоновые кислоты;
- амины;
- аминокислоты;
- жиры;
- белки;
- углеводы.
- Химия и жизнь.
- Расчетные задания / Математика.
Рассмотрим подробнее, что проверяют задания. Красным цветом отмечены задания, за которые дается 1 балл, желтым — 2 балла, зеленым 3 и более баллов.
| № | Общая химия | Неорганическая химия | Органическая химия | Расчетные задания |
| 1 | электронная конфигурация | |||
| 2 | закономерности таблицы Менделеева | |||
| 3 | валентность и степень окисления | |||
| 4 | химические связи и кристаллические решетки | |||
| 5 | номенклатура (тривиальная и международная) | |||
| 6 | свойства простых веществ
реакции ионного обмена (РИО) |
|||
| 7 | соотнесение вещества с рядом веществ | |||
| 8 | составление уравнения реакции | |||
| 9 | взаимосвязь неорганических веществ | |||
| 10 | номенклатура (тривиальная и международная) | |||
| 11 | гомологи и изомеры в органике | |||
| 12 | свойства УВ и кислородсодержащих производных | |||
| 13 | свойства азотсодержащих производных БИО | |||
| 14 | составление уравнения (углеводороды) | |||
| 15 | свойства кислородсодержащих производных УВ | |||
| 16 | составление уравнений (производные УВ) | |||
| 17 | классификация химических реакций | |||
| 18 | скорость химической реакции | |||
| 19 | окислительно-восстановительные реакции | |||
| 20 | электролиз | |||
| 21 | гидролиз | |||
| 22 | химическое равновесие | |||
| 23 | расчеты по уравнению обратимой реакции | |||
| 24 | качественные реакции | качественные реакции | ||
| 25 | блок «Химия и жизнь»: вещества и области их применения | |||
| 26 | расчеты массовой доли | |||
| 27 | расчет теплового эффекта реакции | |||
| 28 | расчеты по уравнению реакции | |||
| 29 | окислительно-восстановительные реакции | |||
| 30 | реакции ионного обмена | |||
| 31 | цепочка из четырех реакций (4 балла) | |||
| 32 | цепочка из пяти реакций (5 баллов) | |||
| 33 | органическая расчетная задача (3 балла) | |||
| 34 | неорганическая расчетная задача (4 балла) |
Рекомендуем расписать подготовку к сдаче ЕГЭ таким образом, чтобы наращивать знания от простого к сложному. Начните с общей химии. Это база, без знания которой можно потерять баллы на заданиях, посвященных органической и неорганической химии. О расписании расскажем в лайфхаке №4.
Лайфхак № 2. Ищите сходства и придумывайте ассоциации в неорганике
Вы могли заметить, что в органической химии больше логики, чем в неорганической. Однако в неорганике также можно проследить аналогии. Например, если вы знаете классификацию веществ, вам проще определить свойства конкретного вещества:
- способность реагировать с другими веществами;
- способность к разложению;
- способность к диссоциации.
Ассоциации — это более творческий подход к запоминанию материала. Вы можете продумать ассоциации для конкретного вещества или группы веществ, наделяя их «характером», манерой поведения или другими образными признаками. Рисуйте на их основе схемы, иллюстрации, придумывайте рифму, используйте свой творческий потенциал, чтобы облегчить обучение и сделать подготовку увлекательнее и интереснее.
Обратите внимание, подготовка к сдаче ЕГЭ часто сводится к выводу четких алгоритмов решений, которые проще вспомнить и применить на экзамене. Тем не менее в экзамене по химии прослеживается тенденция к тому, чтобы оценивать, как ученик понимает материал, а не владеет алгоритмами.
Лайфхак №3. Заучивайте исключения
Многие составители и преподаватели объединяют два первых раздела общую и неорганическую химию. Однако здесь важно учитывать следующее: в теоретических основах химии есть четкие алгоритмы, как заучивать материал при подготовке. При этом в ЕГЭ по химии много заданий построено на исключениях. Преимущественно они сконцентрированы именно в блоке неорганической химии.
Помните, что без знания теоретических основ очень сложно решать задания на неорганическую химию, но не пренебрегайте исключениями при подготовке к экзамену. Запомнить их можно, прибегая к ассоциациям, о которых мы говорили в предыдущем лайфхаке.
Лайфхак №4. Тайм-менеджмент
Сколько нужно готовиться к ЕГЭ по химии?
Период подготовки зависит от уровня знаний о предмете и расписания. С нуля рекомендуется начинать готовиться за 2 года до экзамена. Если у вас есть база, начните готовиться к экзамену с сентября одиннадцатого класса.
Подготовку эксперты рекомендуют разделить по месяцам:
| Месяц | Теория | Практика |
| Сентябрь | Основы общей химии | |
| Октябрь | Неорганическая химия | |
| Ноябрь | Органическая химия | |
| Декабрь | Расчетные задачи | |
| Январь | Комплексные задачи* | |
| Февраль | Основы общей химии | |
| Март | Неорганическая химия | |
| Апрель | Органическая химия | |
| Май | Повторение всего изученного материала | Письменная часть экзамена |
*К комплексным задачам рекомендуется переходить после того, как освоили разделы общей, неорганической и органической химии и математики.
Что если до подготовки к экзамену остался один триместр. Можно ли подготовиться к ЕГЭ по химии за 3 месяца?
Если до экзамена осталось три месяца, их желательно посвятить повторению пройденного материала на практике. Подготовка к ЕГЭ по химии за 3 месяца с нуля потребует высокого темпа ежедневной тренировки, изучения большого объема теории и его отработке. Чтобы подготовиться к ЕГЭ за 3 месяца найдите компетентного специалиста — частного репетитора или курсы.
Специалист поможет выстроить программу обучения. Вне зависимости от сроков это необходимый этап подготовки. Важно составить подробную схему — какие темы изучаете, в какой последовательности и сколько по времени. Заранее выстроенная логика прохождения материала позволит без стресса и спешки готовиться к экзамену.
Следует уделять подготовке 1,5—2 часа в день 3—4 раза в неделю.
Чтобы приучить себя к структуре экзамена, важно не только решать задания из пособий, демоверсии 2023 года и вариантов экзамена, которые сдавали выпускники 2022 года и предыдущих лет. Необходимо максимально приблизить условия экзамена во время тренировки — не подглядывать и не списывать, а также четко отводить 3 ч 30 мин на написание экзамена.
Другой метод работы со временем, которые советуют эксперты — фиксировать время, потраченное на каждое задание. Это позволит отследить, какие задания являются для вас наиболее времязатратными.
Лайфхак №5. Пользуйтесь шпаргалками из КИМа
- ручка;
- документ, удостоверяющий личность;
- лекарства и питание при необходимости;
- непрограммируемый калькулятор.
Остальные необходимые материалы для экзамена выпускникам выдаст организатор. В КИМах помимо бланков можно будет найти Периодическую систему, Таблицу растворимости и Электрохимический ряд напряжений.
Рассмотрим, как они помогут на экзамене.
Периодическая система химических элементов Д.И. Менделеева
Помимо периода, группы и порядкового номера по таблице можно сказать многое. Например:
- количество протонов, электронов в атоме элемента;
- количество оболочек;
- распределение электронов по оболочкам;
- количество электронов на валентной оболочке;
- подгруппу элемента;
- химические свойства простого вещества;
- сведения о соединении элемента.
Периодическая система нужна преимущественно для решения первых четырех заданий: №1 — строение атома, № 2 — периодический закон, №3 — электроотрицательность и степень окисления, №4 — связи и кристаллические решетки.
Электрохимический ряд напряжений
Он показывает:
- как от лития Li до золота Au уменьшается активность металлов;
- поведение оксидов в пирометаллургии;
- поведение солей в гидрометаллургии;
- взаимодействие простого вещества с кислотами;
- поведение соли в гидролизе и электролизе;
- поведение нитрата при разложении.
Эта шпаргалка пригодится во всех заданиях блока неорганической химии — №5—9; задания на электролиз и гидролиз №20, 21; качественные реакции — №24; химия и жизнь — 25; неорганические цепочки — №31.
Таблица растворимости кислот, солей и оснований в воде
В этой таблице собрано большое количество важной информации, например:
- заряд иона;
- степень окисления элемента в ионе;
- поведение при гидролизе;
- поведение в реакциях ионного обмена;
- поведение в качественных реакциях.
Таблица будет полезна для решения заданий на степень окисления в ионе — №3, 19, 29. Для решения всего блока неорганической химии — №5—9; задания на гидролиз — №21, качественные реакции — 24, реакции ионного обмена 30, неорганические цепочки — №31 и сложной комплексной задачи — №34.
Вывод
Мы рассмотрели 5 лайфхаков для ЕГЭ по химии от экспертов и преподавателей. Они помогут ученикам продумать и построить верный курс к успешной сдаче ЕГЭ. Резюмируя, мы предлагаем при подготовке разделить задания экзамена на тематические блоки:
- общую химию;
- неорганическую химию;
- органическую химию;
- математику;
- химию и жизнь (задание №25).
На основе выявленных блоков мы рекомендуем вам составить четкое расписание. При подготовке важно идти по запланированному пути — знать, с чего начинать готовиться, и как последовательно выстроить темы. Кроме того, мы выявили, что эксперты рекомендуют подбирать ассоциации, продумывать аналогии при изучении и повторении материала.
Последнее, чему важно научиться в процессе подготовки — это пользоваться тремя ключевыми таблицами:
- Периодической системой;
- Таблицей растворимости;
- Электрохимическим рядом напряжений металлов.
Рекомендуем сразу скачать те варианты таблиц, что будут в КИМах. Их можно найти на сайте ФИПИ в разделе «Демоверсии, спецификаторы и кодификаторы». Умение работать с этими материалами позволит существенно сэкономить время на экзамене.
Главное при подготовке к экзамену — научиться понимать задачи, а не только зазубривать теорию и структуру. Если вы видите, что не понимаете определенные темы, задавайте вопросы учителю химии в школе, подберите репетитора или курсы. Компетентный специалист построит программу с учетом ваших пробелов в определенных темах и поможет успешно сдать ЕГЭ по химии.
Характерные химические свойства простых веществ — металлов: щелочных, щелочноземельных, алюминия, переходных металлов — меди, цинка, хрома, железа
Простые вещества — металлы
С развитием производства металлов (простых веществ) и сплавов связано возникновение цивилизации (бронзовый век, железный век).
Начавшаяся примерно $100$ лет назад научно-техническая революция, затронувшая и промышленность, и социальную сферу, также тесно связана с производством металлов. На основе вольфрама, молибдена, титана и других металлов начали создавать коррозионностойкие, сверхтвердые, тугоплавкие сплавы, применение которых сильно расширило возможности машиностроения. В ядерной и космической технике из сплавов вольфрама и рения делают детали, работающие при температурах до $3000°С$; в медицине используют хирургические инструменты из сплавов тантала и платины, уникальной керамики на основе оксидов титана и циркония.
И, конечно же, мы не должны забывать, что в большинстве сплавов используют давно известный металл железо, а основу многих легких сплавов составляют сравнительно «молодые» металлы — алюминий и магний.
Сверхновыми стали композиционные материалы, представляющие, например, полимер или керамику, которые внутри (как бетон железными прутьями) упрочнены металлическими волокнами из вольфрама, молибдена, стали и других металлов и сплавов — все зависит от поставленной цели и необходимых для ее достижения свойств материала.
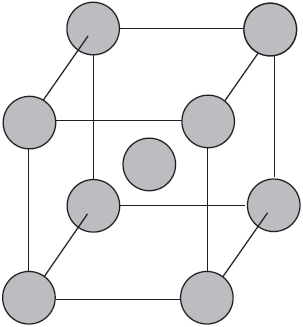
Вы уже имеете представление о природе химической связи в кристаллах металлов. Напомним на примере одного из них — натрия, как она образуется. На рисунке изображена схема кристаллической решетки натрия. В ней каждый атом натрия окружен восемью соседями. У атома натрия, как и у всех металлов, имеется много свободных валентных орбиталей и мало валентных электронов. Электронная формула атома натрия: $1s^{2}2s^{2}2p^{6}3s^{1}3p^{0}3d^{0}$, где $3s, 3p, 3d$ — валентные орбитали.
Единственный валентный электрон атома натрия $3s^1$ может занимать любую из девяти свободных орбиталей — $3s$ (одна), $3р$ (три) и $3d$ (пять), ведь они не очень отличаются по уровню энергии. При сближении атомов, когда образуется кристаллическая решетка, валентные орбитали соседних атомов перекрываются, благодаря чему электроны свободно перемещаются с одной орбитали на другую, осуществляя связь между всеми атомами кристалла металла.
Такую химическую связь называют металлической. Металлическую связь образуют элементы, атомы которых на внешнем слое имеют мало валентных электронов по сравнению с большим числом внешних энергетически близких орбиталей. Их валентные электроны слабо удерживаются в атоме. Электроны, осуществляющие связь, обобществлены и перемещаются по всей кристаллической решетке в целом нейтрального металла.
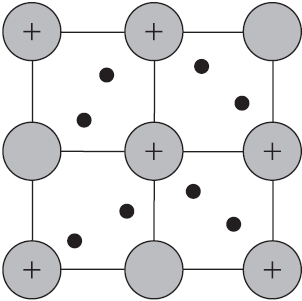
Веществам с металлической связью присущи металлические кристаллические решетки, которые обычно изображают схематически так, как показано на рисунке. Катионы и атомы металлов, расположенные в узлах кристаллической решетки, обеспечивают ее стабильность и прочность (обобществленные электроны изображены в виде черных маленьких шариков).
Металлическая связь — это связь в металлах и сплавах между атомионами металлов, расположенными в узлах кристаллической решетки, осуществляемая обобществленными валентными электронами.
Некоторые металлы кристаллизуются в двух или более кристаллических формах. Это свойство веществ — существовать в нескольких кристаллических модификациях — называют полиморфизмом.
Например, железо имеет четыре кристаллических модификации, каждая из которых устойчива в определенном температурном интервале:
- $α$ — устойчива до $768°С$, ферромагнитная;
- $β$ — устойчива от $768$ до $910°С$, неферромагнитная, т.е. парамагнитная;
- $γ$ — устойчива от $910$ до $1390°С$, неферромагнитная, т.е. парамагнитная;
- $δ$ — устойчива от $1390$ до $1539°С$ ($t°_{пл.} железа), неферромагнитная.
Олово имеет две кристаллические модификации:
- $α$ — устойчива ниже $13,2°С$ ($ρ=5,75 г/см^3$). Это серое олово. Оно имеет кристаллическую решетку типа алмаза (атомную);
- $β$ — устойчива выше $13,2°С$ ($ρ=6,55 г/см^3$). Это белое олово.
Белое олово — серебристо-белый очень мягкий металл. При охлаждении ниже $13,2°С$ он рассыпается в серый порошок, т.к. при переходе $β→α$ значительно увеличивается его удельный объем. Это явление получило название «оловянной чумы».
Конечно, особый вид химической связи и тип кристаллической решетки металлов должны определять и объяснять их физические свойства.
Каковы же они? Это металлический блеск, пластичность, высокая электрическая проводимость и теплопроводность, рост электрического сопротивления при повышении температуры, а также такие значимые свойства, как плотность, высокие температуры плавления и кипения, твердость, магнитные свойства.
Давайте попробуем объяснить причины, определяющие основные физические свойства металлов.
Почему металлы пластичны?
Механическое воздействие на кристалл с металлической кристаллической решеткой вызывает смещение слоев ион-атомов друг относительно друга, а так как электроны перемещаются по всему кристаллу, разрыв связей не происходит, поэтому для металлов характерна большая пластичность.
Аналогичное воздействие на твердое вещество с ковалентными связями (атомной кристаллической решеткой) приводит к разрыву ковалентных связей. Разрыв связей в ионной решетке приводит к взаимному отталкиванию одноименно заряженных ионов. По этому вещества с атомными и ионными кристаллическими решетками хрупкие.
Наиболее пластичные металлы — это $Au, Ag, Sn, Pb, Zn$. Они легко вытягиваются в проволоку, поддаются ковке, прессованию, прокатыванию в листы. Например, из золота можно изготовить золотую фольгу толщиной $0,003$ мм, а из $0,5$ г этого металла можно вытянуть нить длиной $1$ км.
Даже ртуть, которая, как вы знаете, при комнатной температуре жидкая, при низких температурах в твердом состоянии становится ковкой, как свинец. Не обладают пластичностью лишь $Bi$ и $Mn$, они хрупкие.
Почему металлы имеют характерный блеск, а также непрозрачны?
Электроны, заполняющие межатомное пространство, отражают световые лучи (а не пропускают, как стекло), причем большинство металлов в равной степени рассеивают все лучи видимой части спектра. Поэтому они имеют серебристо-белый или серый цвет. Стронций, золото и медь в большей степени поглощают короткие волны (близкие к фиолетовому цвету) и отражают длинные волны светового спектра, поэтому имеют светло-желтый, желтый и медный цвета.
Хотя на практике металл не всегда нам кажется светлым телом. Во-первых, его поверхность может окисляться и терять блеск. Поэтому самородная медь выглядит зеленоватым камнем. А во-вторых, и чистый металл может не блестеть. Очень тонкие листы серебра и золота имеют совершенно неожиданный вид — они имеют голубовато-зеленый цвет. А мелкие порошки металлов кажутся темно-серыми, даже черными.
Наибольшую отражательную способность имеют серебро, алюминий, палладий. Их используют при изготовлении зеркал, в том числе и в прожекторах.
Почему металлы имеют высокую электрическую проводимость и теплопроводны?
Хаотически движущиеся электроны в металле под воздействием приложенного электрического напряжения приобретают направленное движение, т. е. проводят электрический ток. При повышении температуры металла возрастают амплитуды колебаний находящихся в узлах кристаллической решетки атомов и ионов. Это затрудняет перемещение электронов, электрическая проводимость металла падает. При низких температурах колебательное движение, наоборот, сильно уменьшается и электрическая проводимость металлов резко возрастает. Вблизи абсолютного нуля сопротивление у металлов практически отсутствует, у большинства металлов появляется сверхпроводимость.
Следует отметить, что неметаллы, обладающие электрической проводимостью (например, графит), при низких температурах, наоборот, не проводят электрический ток из-за отсутствия свободных электронов. И только с повышением температуры и разрушением некоторых ковалентных связей их электрическая проводимость начинает возрастать.
Наибольшую электрическую проводимость имеют серебро, медь, а также золото, алюминий, наименьшую — марганец, свинец, ртуть.
Чаще всего с той же закономерностью, как и электрическая проводимость, изменяется теплопроводность металлов.
Она обусловлена большой подвижностью свободных электронов, которые, сталкиваясь с колеблющимися ионами и атомами, обмениваются с ними энергией. Происходит выравнивание температуры по всему куску металла.
Механическая прочность, плотность, температура плавления у металлов очень сильно отличаются. Причем с увеличением числа электронов, связывающих ион-атомы, и уменьшением межатомного расстояния в кристаллах показатели этих свойств возрастают.
Так, щелочные металлы ($Li, K, Na, Rb, Cs$), атомы которых имеют один валентный электрон, мягкие, с небольшой плотностью (литий — самый легкий металл с $ρ=0,53 г/см^3$) и плавятся при невысоких температурах (например, температура плавления цезия $29°С$). Единственный металл, жидкий при обычных условиях, — ртуть — имеет температуру плавления, равную $–38,9°С$.
Кальций, имеющий два электрона на внешнем энергетическом уровне атомов, гораздо более тверд и плавится при более высокой температуре ($842°С$).
Еще более прочной является кристаллическая решетка, образованная ионами скандия, который имеет три валентных электрона.
Но самые прочные кристаллические решетки, большие плотности и температуры плавления наблюдаются у металлов побочных подгрупп V, VI, VII, VIII групп. Это объясняется тем, что для металлов побочных подгрупп, имеющих неспаренные валентные электроны на d-подуровне, характерно образование очень прочных ковалентных связей между атомами, помимо металлической, осуществляемой электронами внешнего слоя с $s$-орбиталей.
Вспомните, что самый тяжелый металл — это осмий $Os$ с $ρ=22,5 г/см^3$ (компонент сверхтвердых и износостойких сплавов), самый тугоплавкий металл — это вольфрам $W$ с $t_{пл.}=3420°С$ (применяется для изготовления нитей накаливания ламп), самый твердый металл — это хром $Cr$ (царапает стекло). Они входят в состав материалов, из которых изготавливают металлорежущий инструмент, тормозные колодки тяжелых машин и др.
Металлы по-разному взаимодействуют с магнитным полем. Такие металлы, как железо, кобальт, никель и гадолиний выделяются своей способностью сильно намагничиваться. Их называют ферромагнетиками. Большинство металлов (щелочные и щелочноземельные металлы и значительная часть переходных металлов) слабо намагничиваются и не сохраняют это состояние вне магнитного поля — это парамагнетики. Металлы, выталкиваемые магнитным полем, — диамагнетики (медь, серебро, золото, висмут).
Напомним, что при рассмотрении электронного строения металлов мы разделили металлы на металлы главных подгрупп ($s-$ и $р-$элементы) и металлы побочных подгрупп (переходные $d-$ и $f-$элементы).
В технике принято классифицировать металлы по различным физическим свойствам:
а) плотности — легкие ($ρ < 5 г/см^3$) и тяжелые (все остальные);
б) температуре плавления — легкоплавкие и тугоплавкие.
Железо и его сплавы принято считать черными металлами, а все остальные — цветными.
Существуют классификации металлов по химическим свойствам.
Металлы с низкой химической активностью называют благородными (серебро, золото, платина и ее аналоги — осмий, иридий, рутений, палладий, родий).
По близости химических свойств выделяют щелочные (металлы главной подгруппы I группы), щелочноземельные (кальций, стронций, барий, радий), а также редкоземельные металлы (скандий, иттрий, лантан и лантаноиды, актиний и актиноиды).
Атомы металлов сравнительно легко отдают валентные электроны и переходят в положительно заряженные ионы, т.е. окисляются. В этом, как вам известно, заключается главное общее свойство и атомов, и простых веществ — металлов.
Металлы в химических реакциях всегда восстановители. Восстановительная способность атомов простых веществ — металлов, образованных химическими элементами одного периода или одной главной подгруппы Периодической системы Д.И. Менделеева, изменяется закономерно.
Электрохимический ряд напряжений металлов
Восстановительную активность металла в химических реакциях, которые протекают в водных растворах, отражает его положение в электрохимическом ряду напряжений металлов.
На основании этого ряда напряжений можно сделать следующие важные заключения о химической активности металлов в реакциях, протекающих в водных растворах при стандартных условиях ($t=25°С, р=1 атм$):
- Чем левее стоит металл в этом ряду, тем более сильным восстановителем он является.
- Каждый металл способен вытеснять (восстанавливать) из солей в растворе те металлы, которые в ряду напряжений стоят после него (правее).
- Металлы, находящиеся в ряду напряжений левее водорода, способны вытеснять его из кислот в растворе.
Восстановительная активность металла, определенная по электрохимическому ряду, не всегда соответствует положению его в Периодической системе. Это объясняется тем, что при определении положения металла в ряду напряжений учитывают не только энергию отрыва электронов от отдельных атомов, но и энергию, затрачиваемую на разрушение кристаллической решетки, а также энергию, выделяющуюся при гидратации ионов.
Металлы, являющиеся самыми сильными восстановителями (щелочные и щелочноземельные), в любых водных растворах взаимодействуют прежде всего с водой.
Например, литий более активен в водных растворах, чем натрий (хотя по положению в Периодической системе $Na$ — более активный металл). Дело в том, что энергия гидратации ионов $Li^+$ значительно больше, чем энергия гидратации $Na^+$, поэтому первый процесс является энергетически более выгодным.
Рассмотрев общие положения, характеризующие восстановительные свойства металлов, перейдем к конкретным химическим реакциям.
Взаимодействие металлов с неметаллами
1. С кислородом большинство металлов образуют оксиды — основные и амфотерные. Кислотные оксиды переходных металлов, например оксид хрома (VI) $CrO_3$ или оксид марганца(VII) $Mn_2O_7$, не образуются при прямом окислении металла кислородом. Их получают косвенным путем.
Щелочные металлы $Na, K$ активно реагируют с кислородом воздуха, образуя пероксиды:
Оксид натрия получают косвенным путем, при прокаливании пероксидов с соответствующими металлами:
Литий и щелочноземельные металлы взаимодействуют с кислородом воздуха, образуя основные оксиды:
Другие металлы, кроме золота и платиновых металлов, которые вообще не окисляются кислородом воздуха, взаимодействуют с ним менее активно или при нагревании:
2. С галогенами металлы образуют соли галогеноводородных кислот, например:
3. С водородом самые активные металлы образуют гидриды — ионные солеподобные вещества, в которых водород имеет степень окисления $–1$, например:
Многие переходные металлы образуют с водородом гидриды особого типа — происходит как бы растворение или внедрение водорода в кристаллическую решетку металлов между атомами и ионами, при этом металл сохраняет свой внешний вид, но увеличивается в объеме. Поглощенный водород находится в металле, по-видимому, в атомарном виде.
Существуют и гидриды металлов промежуточного характера.
4. С серой металлы образуют соли — сульфиды, например:
5. С азотом металлы реагируют несколько труднее, т.к. химическая связь в молекуле азота $N_2$ очень прочна; при этом образуются нитриды. При обычной температуре взаимодействует с азотом только литий:
Взаимодействие металов со сложными веществами
1. С водой. Щелочные и щелочноземельные металлы при обычных условиях вытесняют водород из воды и образуют растворимые основания — щелочи, например:
Другие металлы, стоящие в ряду напряжений до водорода, тоже могут при определенных условиях вытеснять водород из воды. Но алюминий бурно взаимодействует с водой, только если удалить с его поверхности оксидную пленку:
Магний взаимодействует с водой только при кипячении, при этом также выделяется водород:
Если горящий магний внести в воду, то горение продолжается, т.к. протекает реакция: $2H_{2}+O_{2}=2H_2O$ (говорит водород). Железо взаимодействует с водой только в раскаленном виде:
2. С кислотами в растворе ($HCl, H_2SO_{4(разб.)}, CH_3COOH$ и др., кроме $HNO_3$) взаимодействуют металлы, стоящие в ряду напряжений до водорода. При этом образуются соль и водород.
Например:
$2Al↖{0}+6{H}↖{+1}Cl=2Al↖{+3}Cl_{3}+3{H_2}↖{0}↑,$
$2CH_3COO{H}↖{+1}+Mg↖{0}=Mg↖{+2}(CH_3COO)_2+{H_2}↖{0}↑$
А вот свинец (и некоторые другие металлы), несмотря на его положение в ряду напряжений (слева от водорода), почти не растворяется в разбавленной серной кислоте, т.к. образующийся сульфат свинца $PbSO_4$ нерастворим и создает на поверхности металла защитную пленку.
3. С солями менее активных металлов в растворе. В результате такой реакции образуется соль более активного металла и выделяется менее активный металл в свободном виде.
Например:
$Fe↖{0}+{Cu}↖{+2}SO_4=Fe↖{+2}SO_4+Cu↖{0}$
Нужно помнить, что реакция идет в тех случаях, когда образующаяся соль растворима. Вытеснение металлов из их соединений другими металлами впервые подробно изучил Н.Н. Бекетов — крупный русский физико-химик. Он расположил металлы по химической активности в «вытеснительный ряд», ставший прототипом ряда напряжений металлов.
4. С органическими веществами. Взаимодействие с органическими кислотами аналогично реакциям с минеральными кислотами. Спирты же могут проявлять слабые кислотные свойства при взаимодействии со щелочными металлами:
$2C_2H_5O{H}↖{+1}+2{Na}↖{0}→2C_2H_5O{Na}↖{+1}+{H_2}↖{0}↑$.
Аналогично реагирует и фенол:
$2C_6H_5O{H}↖{+1}+2{Na}↖{0}→2C_6H_5O{Na}↖{+1}+{H_2}↖{0}↑$.
Металлы участвуют в реакциях с галогеналканами, которые используют для получения низших циклоалканов и для синтезов, в ходе которых происходит усложнение углеродного скелета молекулы (реакция А. Вюрца):
${2CH_3Cl}↙{хлорметан}+2Na→{C_2H_6}↙{этан}+2NaCl$
5. Со щелочами в растворе взаимодействуют металлы, гидроксиды которых амфотерны.
Например:
$2Al+2KOH+6{H_2}↖{+1}O=2K[Al↖{+3}(OH)_4]+3{H_2}↖{0}↑$.
6. Металлы могут образовывать друг с другом химические соединения, которые получили общее название интерметаллических соединений. В них чаще всего не проявляются степени окисления атомов, которые характерны для соединений металлов с неметаллами. Например:
$Cu_3Au, LaNi_5, Na_2Sb, Ca_3Sb_2$ и др.
Интерметаллические соединения обычно не имеют постоянного состава, химическая связь в них в основном металлическая. Образование этих соединений более характерно для металлов побочных подгрупп.
Химические свойства щелочных металлов ($Na, K$)
Щелочные металлы — это элементы главной подгруппы I группы Периодической системы. На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону, находящемуся на большом удалении от ядра. Они легко отдают этот электрон, поэтому являются сильными восстановителями. Во всех соединениях щелочные металлы проявляют степень окисления $+1$. Все они типичные металлы, имеют серебристо-белый цвет, мягкие (режутся ножом), легкие и легкоплавкие. Активно взаимодействуют со всеми неметаллами:
Все щелочные металлы при взаимодействии с кислородом (исключение — $Li$) образуют пероксиды. В свободном виде щелочные металлы не встречаются из-за их высокой химической активности.
Оксиды — твердые вещества, имеют основные свойства. Их получают, прокаливая пероксиды с соответствующими металлами:
Гидроксиды $NaOH, KOH$ — твердые белые вещества, гигроскопичны, хорошо растворяются в воде с выделением теплоты, их относят к щелочам:
Соли щелочных металлов почти все растворимы в воде. Важнейшие из них: $Na_2CO_3$ — карбонат натрия; $Na_2CO_3·10H_2O$ — кристаллическая сода; $NaHCO_3$ — гидрокарбонат натрия, пищевая сода; $K_2CO_3$ — карбонат калия, поташ; $Na_2SO_4·10H_2O$ — глауберова соль; $NaCl$ — хлорид натрия, пищевая соль.
Химические свойства щелочноземельных металлов ($Ca, Mg$)
Кальций ($Ca$) является представителем щелочноземельных металлов, как называют элементы главной подгруппы II группы, но не все, а только начиная с кальция и вниз по группе. Это те химические элементы, которые, взаимодействуя с водой, образуют щелочи. Кальций на внеш нем энергетическом уровне содержит два электрона, степень окисления $+2$.
Физические и химические свойства кальция и его соединений представлены в таблице.
Магний ($Mg$) имеет такое же строение атома, как и кальций, степень его окисления также $+2$. Мягкий металл, но его поверхность на воздухе покрывается защитной пленкой, что немного снижает его химическую активность. Его горение сопровождается ослепительной вспышкой. $MgO$ и $Mg(OH)_2$ проявляют основные свойства. Хотя $Mg(OH)_2$ и малорастворим, но окрашивает раствор фенолфталеина в малиновый цвет.
Оксиды $MgO$ — твердые белые тугоплавкие вещества. В технике $CaO$ называют негашеной известью, а $MgO$ — жженой магнезией, их используют в производстве строительных материалов.
Реакция оксида кальция с водой сопровождается выделением теплоты и называется гашением извести, а образующийся $Ca(OH)_2$ — гашеной известью. Прозрачный раствор гидроксида кальция называется известковой водой, а белая взвесь $Ca(OH)_2$ в воде — известковым молоком.
Соли магния и кальция получают взаимодействием их с кислотами.
$CaCO_3$ — карбонат кальция, мел, мрамор, известняк. Применяется в строительстве. $MgCO_3$ — карбонат магния — применяется в металлургии для освобождения от шлаков. $CaSO_4·2H_2O$ — гипс. $MgSO_4$ — сульфат магния — называют горькой, или английской, солью, содержится в морской воде. $BaSO_4$ — сульфат бария — благодаря нерастворимости и способности задерживать рентгеновские лучи применяется в диагностике («баритовая каша») желудочно-кишечного тракта.
На долю кальция приходится $1,5%$ массы тела человека, $98%$ кальция содержится в костях.
Кальций и его соединения.
| Кальций | Оксид и гидроксид кальция | Соли кальция |
| 1. Серебристо-белый металл. 2. Активный металл, окисляется простыми веществами — неметаллами: $2Ca+O_2=2CaO$ $Ca+Cl_2=CaCl_2$ $Ca+S=CaS$ $Ca+H_2=CaH_2$ 3. Вытесняет водород из воды: $Ca+2H_2O=Ca(OH)_2+H_2↑$ 4. Вытесняет металлы из их оксидов (кальциотермия): $2Ca+ThO_2=Th+2CaO$ Получение Разложение электрическим током расплава хлорида кальция: $CaCl_2=Ca+Cl_2↑$ |
1. Порошки белого цвета. 2. Оксид кальция (негашеная известь) проявляет свойства основного оксида: а) взаимодействует с водой с образованием основания: $CaO+H_2O=Ca(OH)_2$ б) взаимодействует с кислотными оксидами: $CaO+SiO_2=CaSiO_3$ 3. Гидроксид кальция проявляет свойства сильного основания: $Ca(OH)_2=Ca^{2+}+2OH^{–}$ $Ca(OH)_2+CO_2=CaCO_3↓+H_2O$; $Ca(OH)_2+Ca(HCO_3)_2=2CaCO_3↓+2H_2O$$ Получение 1. Оксида — обжиг известняка: $CaCO_3=CaO+CO_2↑$ 2. Гидроксида — гашение негашеной извести: $CaO+H_2O=Ca(OH)_2$ |
1. Образует нерастворимый карбонат: $Ca^{2+}+CO_3^{2−}=CaCO_3↓$ и растворимый гидрокарбонат: $CaCO_{3(кр)}+CO_2+H_2O=Ca(HCO_3)_{2(р-р)}$ 2. Образует нерастворимый фосфат: $3Сa_{2+}+2PO_4^{3−}=Ca_3(PO_4)_2↓$ и растворимый дигидрофосфат: $Ca_3(PO_4)_{2(кр)}+4H_3PO_4=3Ca(H_2PO_4)_{2(р-р)}$ 3. Гидрокарбонат разлагается при кипячении или испарении раствора: $Ca(HCO_3)_2=CaCO_3↓+CO_2↑+H_2O$ 4. Обожженный природный гипс: $CaSO_4·2H_2O=CaSO_4·0,5H_2O+1,5H_2O$ затвердевает при взаимодействии с водой, снова образуя кристаллогидрат: $CaSO_4·0,5H_2O+1,5H_2O=CaSO_4·2H_2O$ |
Химические свойства алюминия
Алюминий ($Al$) — элемент главной подгруппы III группы Периодической системы. У него на внешнем энергетическом уровне три электрона, которые алюминий легко отдает при химических взаимодействиях. У атомов алюминия восстановительные свойства выражены ярче, чем у бора, т.к. у алюминия имеется промежуточный слой с восемью электронами ($2e↖{-}; 8e↖{-}; 3e↖{-}$), который препятствует притяжению электронов к ядру. Алюминий имеет степень окисления $+3$.
Алюминий — серебристо-белый металл, $t°_{пл}=660°С$. Это самый распространенный металл земной коры, обладает высокой коррозионной стойкостью. Малая плотность алюминия ($2,7 г/{см^3}$) в сочетании с высокой прочностью и пластичностью его сплавов делают алюминий незаменимым в самолетостроении. Высокая электропроводность алюминия (в $1.6$ раза меньше, чем у меди) позволяет заменять медные провода более легкими — алюминиевыми.
Высокая химическая активность алюминия используется в алюминотермии, с помощью которой получают хром, ванадий, титан и другие металлы.
Прочность химической связи в оксиде $Al_2O_3$ обуславливает его механическую прочность, твердость. $Al_2O_3$ — корунд, абразивный материал. Искусственный рубин — $Al_2O_3$ с добавлением оксида хрома. Химические свойства алюминия и его соединений обобщены в таблице.
Алюминий и его соединения.
| Алюминий | Соединения алюминия | |
| Оксид алюминия | Гидроксид алюминия | |
| 1. Серебристо-белый легкий металл. 2. Окисляется на воздухе с образованием защитной пленки: $4Al+3O_2=2Al_2O_3$ 3. Вытесняет водород из воды: $2Al+6H_2O=2Al(OH)_3↓+3H_2↑$ 4. Взаимодействует с кислотами: $2Al^{0}+6H^{+}=2Al^{3+}+3H_2^0{↑}$ 5. Взаимодействует с водным раствором щелочи: $2Al+2H_2O+2NaOH=2NaAlO_2+3H_2{↑}$ 6. Вытесняет металлы из их оксидов (алюминотермия): $8Al+3Fe_3O_4=9Fe+4Al_2O_3+Q$ Получение Разложение электрическим током расплава оксида алюминия (в криолите): $2Al_2O_3=4Al+3O_2{↑}–3352 кДж$ |
1. Очень твердый порошок белого цвета 2. Амфотерный оксид, взаимодействует: а) с кислотами: $Al_2O_3+6H^{+}=2Al^{3+}+3H_2O$ б) со щелочами: $Al_2O_3+2OH^{–}=2AlO_2^{−}+H_2O$ Образуется: а) при окислении или горении алюминия на воздухе: $4Al+3O_2=2Al_2O_3$ б) в реакции алюминотермии: $2Al+Fe_2O_3=Al_2O_3+2Fe$; в) при термическом разложении гидроксида алюминия: $2Al(OH)_3=Al_2O_3+3H_2O$ |
1. Белый нерастворимый в воде порошок. 2. Проявляет амфотерные свойства, взаимодействует: а) с кислотами: $Al(OH)_3+3HCl=AlCl_3+3H_2O$ $Al(OH)_3+3H^{+}=Al^{3+}+3H_2O$ б) со щелочами: $Al(OH)_3+NaOH=NaAlO_2+2H_2O$ $Al(OH)_3+OH^{–}=AlO_2^{−}+2H_2O$ 3. Разлагается при нагревании: $2Al(OH)_3=Al_2O_3+3H_2O$ Образуется при: а) взаимодействии растворов солей алюминия с растворами щелочей (без избытка): $Al^{3+}+3OH^{–}=Al(OH)_3↓$ б) взаимодействии алюминатов с кислотами (без избытка): $AlO_2^{−}+H^{+}+H_2O=Al(OH)_3↓$ Соли алюминия в водных растворах гидролизуются: $Al^{3+}+H_2O⇄AlOH^{2+}+H^{+}$ $AlOH^{2+}+H_2O⇄Al(OH)_2^{+}+H^{+}$ $Al(OH)_2^{+}+H_2O⇄Al(OH)_{3}+H^{+}$ |
Химические свойства меди
Медь ($Cu$) — элемент побочной подгруппы первой группы. Электронная формула: ($…3d^{10}4s^1$). Десятый d-электрон атома меди подвижный, т. к. переместился с $4s$-подуровня. Медь в соединениях проявляет степени окисления $+1(Cu_2O)$ и $+2(CuO)$.
Медь — мягкий, блестящий металл, имеющий красную окраску, ковкий и обладает хорошими литейными качествами, хороший тепло- и электропроводник. Температура плавления $1083°С$.
Как и другие металлы побочной подгруппы I группы Периодической системы, медь стоит в ряду активности правее водорода и не вытесняет его из кислот, но реагирует с кислотами-окислителями:
$Cu+2H_2SO_{4(конц.)}=CuSO_4+SO_2↑+2H_2O$;
$Cu+4HNO_{3(конц.)}=Cu(NO_3)_2+2NO_2↑+2H_2O$.
Под действием щелочей на растворы солей меди выпадает осадок слабого основания голубого цвета — гидроксида меди (II), который при нагревании разлагается на основный оксид $CuO$ черного цвета и воду:
$Cu^{2+}+2OH^{–}=Cu(OH)_2↓; Cu(OH)_2 {→}↖{t°} CuO+H_2O$
Химические свойства цинка
Цинк ($Zn$) — элемент побочной подгруппы II группы. Его электронная формула следующая: ($…3d^{10}4s^2$). Так как в атомах цинка предпоследний $d-$подуровень полностью завершен, то цинк в соединениях проявляет степень окисления $+2$.
Цинк — металл серебристо-белого цвета, практически не изменяющийся на воздухе. Обладает коррозионной стойкостью, что объясняется наличием на его поверхности оксидной пленки.
Цинк — один из активнейших металлов, при повышенной температуре реагирует с простыми веществами:
$Zn+Cl_2→↖{t°}ZnCl_2$,
$2Zn+O_2→↖{t°}2ZnO$,
$Zn+S→↖{t°}ZnS$.
Цинк вытесняет водород из кислот:
$Zn+2Н^{+}=Zn^{2+}+H_2↑$
Гидроксид цинка амфотерен, т. е. проявляет свойства и кислоты, и основания. При постепенном приливании
| 1 | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ | |
| 1.1 | Современные представления о строении атома | |
| 1.1.1 | Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов. | |
| 1.2 | Периодический закон и периодическая система химических элементов Д.И. Менделеева | |
| 1.2.1 | Закономерности изменения химических свойств элементов и их соединений по периодам и группам периодической таблицы химических элементов. | |
| 1.2.2 | Общая характеристика металлов IА–IIIА групп в связи с их положением в периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | |
| 1.2.3 | Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И.Менделеева и особенностям строения их атомов. | |
| 1.3 | Химическая связь и строение вещества | |
| 1.3.1 | Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь. | |
| 1.3.2 | Электроотрицательность. Степень окисления и валентность химических элементов. | |
| 1.3.3 | Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения. | |
| 1.4 | Химическая реакция | |
| 1.4.1 | Классификация химических реакций в неорганической и органической химии. | |
| 1.4.2 | Тепловой эффект химической реакции. Термохимические уравнения. | |
| 1.4.3 | Скорость реакции, ее зависимость от различных факторов. | |
| 1.4.4 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов. | |
| 1.4.5 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. | |
| 1.4.6 | Реакции ионного обмена. | |
| Особенности взаимодействия кислых солей со щелочами. | ||
| 1.4.7 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. | |
| Необратимый гидролиз бинарных соединений. | ||
| 1.4.8 | Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее. | |
| 1.4.9 | Электролиз расплавов и растворов (солей, щелочей,кислот). | |
| 2 | НЕОРГАНИЧЕСКАЯ ХИМИЯ | |
| 2.1 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная). | |
| 2.2 | Химические свойства простых веществ — металлов | |
| 2.2.1 | Характерные химические свойства щелочных металлов. | |
| 2.2.2 | Характерные химические свойства бериллия, магния и щелочноземельных металлов. | |
| 2.2.3 | Характерные химические свойства алюминия. | |
| 2.2.4 | Химические свойства переходных металлов (меди, цинка, хрома, железа). | |
| 2.3 | Химические свойства простых веществ — неметаллов | |
| 2.3.1 | Химические свойства водорода и галогенов. | |
| 2.3.2 | Химические свойства кислорода и серы. | |
| 2.3.3 | Химические свойства азота и фосфора. | |
| 2.3.4 | Химические свойства углерода и кремния. | |
| 2.4 | Характерные химические свойства оксидов: основных, амфотерных, кислотных. | |
| 2.5 | Характерные химические свойства оснований и амфотерных гидроксидов. | |
| 2.6 | Характерные химические свойства кислот. | |
| 2.7 | Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка). | |
| 3 | ОРГАНИЧЕСКАЯ ХИМИЯ | |
| 3.1 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. | |
| 3.2 | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа. | |
| 3.3 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная). | |
| 3.4 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). | |
| 3.5 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. | |
| 3.6 | Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. | |
| 3.7 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. | |
| 3.8 | Биологически важные вещества: жиры, белки, углеводы (моносахарады, дисахариды, полисахариды) | |
| 3.8.1 | Жиры. | |
| 3.8.2 | Белки. | |
| 3.8.3 | Углеводы (моносахариды, дисахариды, полисахариды). | |
| 3.9 | Взаимосвязь органических соединений. | |
| 4 | МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ | |
| 4.1 | Экспериментальные основы химии | |
| 4.1.1 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. | |
| 4.1.2 | Методы разделения смесей и очистки веществ. | |
| 4.1.3 | Определение характера среды водных растворов веществ. Индикаторы. | |
| 4.1.4 | Качественные реакции на неорганические вещества и ионы. | |
| 4.1.5 | Качественные реакции органических соединений. | |
| 4.1.7 | Основные способы получения углеводородов. | |
| 4.1.8 | Основные способы получения кислородсодержащих соединений. | |
| 4.2 | Общие представления о промышленных способах получения важнейших веществ | |
| 4.2.1 | Понятие о металлургии: общие способы получения металлов. | |
| 4.2.2.1 | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). | |
| 4.2.3 | Природные источники углеводородов, их переработка. | |
| 4.2.4 | Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки. | |
| 4.3 | Рачеты по химическим формулам и уравнениям реакций | |
| 4.3.1 | Расчеты с использованием понятия «массовая доля вещества в растворе». | |
| 4.3.2 | Расчеты объемных отношений газов при химических реакциях. | |
| 4.3.3 | Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ. | |
| 4.3.4 | Расчеты теплового эффекта реакции. | |
| 4.3.5 | Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси). | |
| 4.3.6 | Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества. |