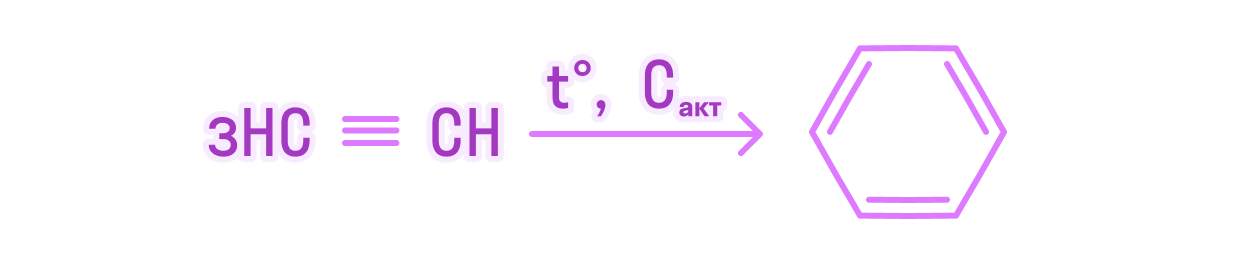Всем привет! На календаре 26 января, а это значит, что до ЕГЭ по химии осталось 4 месяца. По этой прекрасной (нет) причине сегодня хочу обсудить с вами организацию подготовки к экзамену в оставшееся время.
В доброй традиции химия открывает хит-парад ЕГЭ:
- досрочный этап — 21 марта
- основной этап — 26 мая
Иногда не хватает маленькой детали, чтобы стать счастливым…
Для начала посмотрим на структуру ЕГЭ по химии (нужно ведь знать, с кем мы будем бороться 🧐 ). Условно можно выделить 4 блока:
🧪 общая химия, примерно 25% баллов
🧪 неорганика, примерно 30% баллов
🧪 органика, примерно 30% баллов
🧪 расчётные задачи, примерно 15% баллов
На выполнение заданий даётся 3 часа 30 минут. При хорошей подготовке к ЕГЭ по химии 3 часов на выполнение всех заданий вполне достаточно. У вас останется ещё 30 минут, чтобы всё перепроверить.
Обратите внимание, что первая (тест) и вторая (задания с развернутым ответом) части взаимосвязаны между собой по темам, поэтому первый общий совет: ботайте тест вместе со второй частью!
Например, вы разбираете свойства классов неорганических соединений и сразу же закрепляете теорию на тестовых заданиях 7,8,9 и прописываете реакции в 31 задании. Даже если вы не знаете каких-то реакций, напишите хотя бы то, что успели разобрать.
Второй общий совет: ботайте задачи!
Ботая задачи, вы одновременно повторяете теорию, учитесь писать реакции, прокачиваете расчётную часть. Не нужно сразу решать сложные задачи, можно начать с простых и постепенно усложнять (свою жизнь).
_________________
Я предлагаю три плана подготовки на разные баллы
_________________
Первый план: 65-75 баллов
На эти баллы подготовиться вполне просто, достаточно пользоваться школьным учебником (я всё же рекомендую профильный) и практиковать пройденное в сборниках Д.Ю. Добротина или Ю.Н. Медведева
Вам нужно знать основные понятия химии, общие вещи, уметь узнавать реакции и прописывать их своей рукой, решать не самые сложные задачи. Вот основной пул тем, на которые стоит обратить внимание:
⚛️ Общая химия: электронная конфигурация атома, закономерности изменения свойств по таблице Менделеева, степень окисления и валентность, химические связи и кристаллические решетки, классификация химических реакций, скорость химической реакции и химическое равновесие, электролиз, гидролиз и реакции ионного обмена
⚛️ Неорганика: классификация неорганических веществ, основные классы неорганики (оксиды, основания, амфотерные гидроксиды, кислоты, соли), химия неметаллов (водород, галогены, кислород, сера, азот, фосфор, углерод, кремний)
⚛️ Органика: классификация органических веществ, химия углеводородов (алканы, циклоалканы, алкены, диены, алкины, ароматические углеводороды)
⚛️ Расчётные задачи: массовая доля вещества в растворе, расчеты по уравнению реакции, термохимические расчеты
Второй план: 75-90 баллов
Вы уже знаете всю химию, в каждом разделе неплохо ориентируетесь, посмотрев вышеперечисленные темы вспомнили все основные моменты. Баллы вы теряете чаще всего по невнимательности или из-за незнания тонких моментов. Здесь вы занимаетесь углубленными вещами:
⚛️ Общая химия: окислительно-восстановительные реакции, химия и жизнь
⚛️ Неорганика: химия металлов (щелочные, щелочноземельные, алюминий, цинк, хром, марганец, железо, медь, серебро), написание цепочек в задании 31
⚛️ Органика: химия производных углеводородов (спирты, фенолы, альдегиды и кетоны, карбоновые кислоты, сложные эфиры), химия азотсодержащих органических веществ (амины и аминокислоты), написание цепочек в задании 32
⚛️ Расчётные задачи: некоторые сюжеты задач 33-34 (например, задачи на пластинку или электролиз, избыток/недостаток)
Из литературы могу посоветовать «Начала химии» В.В. Ерёмина, там же есть и задачи. Что касается сборников: тренинги В.Н. Доронькина, лично у меня два фаворита: тренировочные варианты и задания высокого уровня сложности. То есть вы решаете сборники подобного уровня, какой-то материал изучаете сразу на практике, учитесь искать закономерности и применять их в новой ситуации
Третий план: 90-100 баллов
Вы буквально живёте химией: вместо имен друзей в вашей памяти молярные массы всех элементов, во сне вы решаете 33 задачи, а в самых страшных кошмарах напрямую окисляете бензол кислородом🤯 На самом деле, вы прекрасно работаете и, скорее всего, теряете баллы не из-за незнания темы, а из-за мелких ошибок. Или теряете балл на оформлении, в расчетах (арифметические ошибки).
Главное — это внимание к деталям. Вы должны помнить все тонкие моменты и отмечать их сразу же, тотально контролировать цифры. Также вы обязаны ботать сложные задачи: для этого подойдут сборники задач из «Начал химии» или упражнения И.Г. Хомченко, смотрите варианты отборочных и заключительных этапов перечневых олимпиад, можно заглядывать в ДВИ, тут поможет книга «Олимпиады и конкурсные экзамены по химии в МГУ». Как это работает: вы решаете задачу и понимаете, что можете спокойно её решить, делаете это, постепенно усложняете варианты, ищете новые типы заданий. Ну и конечно же, расширяете кругозор и развиваете химическое воображение и химическую эрудицию.
Пользуйтесь «Началами химии», можно заглядывать и в вузовские учебники.
_________________
Вы не можете знать, что будет у вас на экзамене, поэтому готовиться надо к разным исходам и развитию событий
_________________
А сколько времени на это всё надо?
Для первого плана вполне достаточно 1-2 часов в день. Это чтение учебников, решение тестов и простейших расчетных задач, просмотр видео по темам.
Для второго плана нужно потратить 3-5 часов в день. Это повторение уже изученного материала, освоение новой литературы, изучение новых типов задач, написание пробников.
Для третьего плана условно вы тратите n часов в день, где n стремится к бесконечности, так как вы постоянно расширяете кругозор, находитесь в активном поиске сложных задач.
ПОДЫТОЖИМ:
- Расширяйте свой кругозор, даже если не нужны высокие баллы
- Внимание к мелочам
- Решайте сложные задания
- Развивайте межпредметные связи: математика, биология, физика вполне могут пригодиться на экзамене по химии
- Качайте soft skills: грамотный отдых поможет отвлечься от химии и не допустить выгорания, а ещё вы получите крутой навык. Например, можно начать учить новый язык, записаться на шахматы или танцы, заняться мнемотехникой или скорочтением, why not?
- Ботайте химию и верьте в себя, всё будет круто❤️🦊
А если хотите круто подготовиться к ЕГЭ за оставшееся время, то приходите на экспресс-курсы Фоксфорда:
- У вас будет сразу 2 преподавателя, которым можно доверить подготовку
- Разбирайте все темы ЕГЭ по химии: основная цель преподавателей — чтобы вы поняли сам предмет, увидели его структуру и логику. Тогда на экзамене вы справитесь с заданием даже в непривычной формулировке, которая не встречалась в пробных вариантах.
- Распределяйте время и не беспокойтесь, что не успеете: с февраля по май вы успеете прорешать все задания с кратким и развёрнутым ответами, узнаете об изменениях этого года и деталях оформлениях. Особое внимание преподаватели уделят задачам из второй части, чтобы вы могли заработать максимум баллов.
- Вручную проверяем пробники и домашние работы: мы не оставляем задания части с развёрнутым ответом на самопроверку — ими занимаются эксперты ЕГЭ. Проверяем «по-настоящему», как на экзамене, и в результате вы получаете развёрнутую обратную связь. Всё это — ради скорости подготовки и ваших заветных баллов для поступления.
- Личный куратор ответит на любой вопрос в течение двух часов: Кураторы — это студенты, которые сдали ЕГЭ на 90+ баллов и знают, как непросто бывает с подготовкой. Они разбираются в программе и предмете, поэтому легко ответят на вопросы по курсу и домашке и сориентируют по поступлению в ВУЗ. Самое важное — кураторы будут поддерживать вас и помогать справиться со стрессом и страхом перед экзаменами.
Смотреть видео:
#химия #химияпросто #неорганика #егэпохимии #эксперименты #химик #егэхимия #неорганическая_химия #огэхимия
Свежая информация для ЕГЭ и ОГЭ по Химии (листай):
С этим видео ученики смотрят следующие ролики:

Как подготовиться к ЕГЭ 2022 по химии за 4 месяца на 80+ баллов с любого уровня?
Химия ЕГЭ сотка

Как подготовиться к ЕГЭ 2022 по химии за 5 месяцев на 80+ баллов с любого уровня?
Химия ЕГЭ сотка

Как подготовиться к ЕГЭ по химии за 3 месяца с любого уровня?
Химия ЕГЭ сотка

ЕГЭ по химии. Можно ли подготовиться за год с нуля? | Химия ЕГЭ 2022 | Parta
Parta химия ЕГЭ
Облегчи жизнь другим ученикам — поделись! (плюс тебе в карму):
18.01.2022
Подготовка к ЕГЭ по химии
Как проходит ЕГЭ по химии в 2023 году
На ЕГЭ по химии, как и в случае с большинством других предметов, ученик 11 класса должен будет справиться с 2 частями экзамена:
-
1-я часть: 28 заданий с кратким ответом;
-
2-я часть: 6 заданий с развернутым ответом.
Чтобы решить все 34 задания единого государственного экзамена, у ученика будет 210 минут. За это время нужно будет успеть ответить на вопросы обеих частей, подготовить полное решение для задач 2-й части и перенести ответы в бланк.
Кстати, в отличие от ОГЭ, на ЕГЭ по химии не будет задания-эксперимента. Только обычные химические задания разной сложности. В таблице ниже можно посмотреть, сколько будет легких, средних и сложных вопросов.
| Уровень сложности заданий на ЕГЭ по химии | |
|---|---|
| Базовая | 17 |
| Повышенная | 11 |
| Высокая | 6 |
Если вы хотите больше узнать об особенностях экзамена и подготовки к нему, советуем заглянуть в раздел «Демоверсии, спецификации, кодификаторы» сайта ФИПИ. Там вы найдете всю актуальную информацию о ЕГЭ по химии и методические рекомендации. Все это поможет распланировать подготовку к экзамену так, чтобы сдать его на 100 баллов.
Изменения в ЕГЭ по химии
По сравнению с 2022 годом экзамен по химии немного изменится. Вот список нововведений:
-
Немного поменялось условие задания 23, в котором нужно рассчитать концентрацию веществ. Теперь данные в нем будут записаны текстом, а не в таблице.
-
Задания 33 и 34 поменялись местами.
-
Задания 9, 12 и 16 теперь станут повышенной сложности.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Демоурок по подготовке к экзаменам
Составим ваш личный путь к высоким баллам — учтем сроки, уровень знаний и цель.
Как хорошо сдать ЕГЭ по химии: разбор сложных задач
Как мы узнали из таблицы в предыдущем разделе, экзамен по химии — один из самых сложных. На 34 задания в нем приходится целых 11 повышенной сложности и 6 — высокой. Но если вы хотите поступить в вуз мечты, советуем научиться их решать так, чтобы не упустить ни одного балла. А потому предлагаем начать подготовку прямо сейчас и вместе разобрать несколько таких задач.
Задание 7
Это задание проверяет буквально все ваши знания в области неорганической химии. Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Установите соответствие между веществом и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Вещество | Реагенты |
|---|---|
| А) S | 1) AgNO3, K3PO4, Cl2 |
| Б) SO3 | 2) BaO, NaOH, H2O |
| В) Zn(OH)2 | 3) H2, Cl2, O2 |
| Г) ZnBr2 | 4) HBr, LiOH, CH3COOH (p-p) |
| 5) H3PO4 (p-p), BaCl2, CuO |
Решение:
-
Вариант под буквой А — простое вещество, сера. Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
-
Вещество под буквой Б — кислотный оксид. Кислотные оксиды не реагируют с кислотами, поэтому смело вычеркиваем варианты, где присутствует хоть одна кислота. Остаются варианты № 1–3. Реагенты под цифрой 3 тоже можем вычеркнуть, так как кислотный оксид уже в своей максимальной степени окисления и дальше взаимодействовать с кислородом не может. Остаются варианты № 1 и № 2. Оксид серы (VI) может реагировать с основным оксидом с образованием соли, со щелочью с образованием соли и воды, и с водой, при этом образуя кислоту. Выбираем № 2.
-
Амфотерный нерастворимый в воде гидроксид цинка может взаимодействовать только с теми, что способны его растворить. Единственно верный вариант под № 4, где указаны кислоты и щелочь.
-
При взаимодействии соли с другими сложными веществами надо помнить про три признака протекания химической реакции: выпадения осадка, выделение газа и образование малодиссоциирующего вещества — воды. Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Ответ: 3241.
Задание 15
Это задание Единого государственного экзамена проверит ваши знания химических свойств органических соединений. Чтобы справиться с ним, нужно по записанным словами реагирующим веществам составить уравнение реакции и выбрать из перечня один из получившихся продуктов. Давайте рассмотрим на примере, как решать такую задачу.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Реагирующие вещества | Продукт взаимодействия |
|---|---|
| А) уксусная кислота и сульфид калия | пропионат калия |
| Б) муравьиная кислота и гидроксид калия | этилат калия |
| В) муравьиный альдегид и гидроксид меди (II) при нагревании | формиат меди (II) |
| Г) этанол и калий | формиат калия |
| ацетат калия | |
| углекислый газ |
Решение:
-
Органические кислоты могут реагировать с солями, если те имеют летучий анион. В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
-
Муравьиная кислота проявляет свойства неорганической кислоты и может взаимодействовать с щелочами с образованием соли и воды. Соль муравьиной кислоты — формиат. Правильный ответ № 4.
-
Под буквой В описана качественная реакция на альдегиды с образованием соответствующей кислоты, оксида меди (I) и воды. Исключение — муравьиный альдегид. Он окисляется до углекислого газа, а остальные продукты реакции те же. Соответственно, правильный ответ № 6.
-
Калий как активный металл может замещать протон водорода в гидроксогруппе у спиртов с образованием алкоголята. Правильный ответ: № 2.
Ответ: 5462.
Задание 16
Это задание всё так же проверяет ваши знания по химическим свойствам и, как следствие, умение записывать превращения в рамках органической химии. Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами х и у:
-
2-бромбутан;
-
этаналь;
-
этен;
-
метилпропан;
-
хлорэтан.
Решение:
Посмотрим, что случилось с известными нам веществами.
-
У спирта исчезла ОН-группа, затем что-то произошло, и углеродная цепочка увеличилась вдвое. Мы помним, что когда цепочка увеличивается вдвое, то, скорее всего, это реакция Вюрца. А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
-
Бутан подвергают нагреванию с использованием катализатора. Нужно помнить, что в таких условиях проводится изомеризация алканов. Из бутана получается метилпропан. Ответ: № 4.
Ответ: 54.
Задание 26
Теперь разберем задачи, которые заканчивают тестовую часть ЕГЭ по химии. Рассмотрим условие одной из них на нахождение массы соли, которую необходимо добавить для получения раствора с новой заданной массовой долей.
Вычислите массу нитрата калия (в граммах), которую следует растворить в 160 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. Ответ округлите до десятых.
Чтобы решить эту задачу, вспомним основную формулу нахождения массовой доли:
-
Найдем массу изначально растворенного нитрата калия в растворе, выразив из формулы выше:
подставим значения:
-
Чтобы увеличить массовую долю соли в растворе, необходимо ее добавить еще. Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
-
Далее в дело вступает чистая математика. Разделим обе части уравнения на 100%:
-
По пропорции перемножим крест-накрест:
0,12 * (160 + X) = 16 + X.
-
Раскроем скобки:
19,2 + 0,12Х = 16 + Х.
-
Приведем подобные: с Х в одну сторону, без Х — в другую:
3,2 = 0,88Х.
-
Найдем Х:
Масса нитрата калия, которую необходимо добавить для увеличения массовой доли раствора до 12%, равна 3,6 граммам.
Ответ: 3,6.
Задание 28
Эта задача может встретиться на экзамене в нескольких вариантах. Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
В результате реакции тримеризации ацетилена объемом 26,88 л (н.у) получили 24,96 г бензола. Вычислите массовую долю выхода продукта реакции от теоретически возможного.
Решение:
-
Для начала напишем формулу, по которой считается доля выхода продукта:
Как определить, какая масса практическая, а какая — теоретическая? Значения, которые даются после слова «получили», — это практическая масса. Та, которая получилась в результате проведения химической реакции в реальных условиях. Масса теоретическая — та, которую рассчитывают из уравнения реакции, зная массу исходных реагентов.
-
Напишем уравнение химической реакции тримеризации ацетилена:
-
Найдем количество вещества ацетилена:
подставим значения:
-
Перейдем на количество вещества бензола, получаемого из ацетилена:
-
Зная количество вещества бензола, найдем его массу:
подставим значения:
m = 0,4 * 78 = 31,2 грамма.
-
Масса, рассчитываемая по уравнению реакции, является теоретической. Масса практическая дана нам по условию. Подставим полученные данные по массам в формулу для нахождения доли выхода продукта реакции:
Доля выхода бензола из данного объема ацетилена составляет 80%.
Ответ: 80.
Как оценивают готовые работы на ЕГЭ по химии
1-я часть
В 1-й части Единого государственного экзамена по химии задания 1–5, 9–13, 16–21, 25–28 оценивают 1 баллом, если вы запишете верный ответ по эталону. При этом в заданиях 1, 3, 4, 11, 12, 13, 17 и 18 ответ — это ряд цифр. То, в каком порядке вы их запишете, не влияет на оценку. Например, если в задании верны варианты под номерами 1 и 4, их можно записать как 14 или как 41. И в обоих случаях ответ засчитают как верный.
За правильные ответы в заданиях 6, 7, 8, 14, 15, 22, 23 и 24 можно получить по 2 балла. Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
2-я часть
В этой части нужно записать не только ответ, но и решение. А значит, и оценивать такие задания будут сразу по нескольким критериям. Зато за верный ответ в некоторых вопросах можно получить больше баллов, чем за любое задание 1-й части. Максимум — 5 баллов. А теперь давайте разберемся, как именно их будут оценивать.
| Задание № 29 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества и записал уравнение химической реакции, составил электронный баланс, указал окислитель и восстановитель | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 30 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества, записал все нужные уравнения реакции | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 31 | Баллы |
|---|---|
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 4 |
| Задание № 32 | Баллы |
|---|---|
| Правильно записаны 5 уравнений реакции | 5 |
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 5 |
| Задание № 33 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 3 элемента | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 3 |
| Задание № 34 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 4 элемента | 4 |
| Правильно записаны только 3 элемента ответа | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 4 |
Как сдать ЕГЭ по химии на 3, 4 и 5
Мы уже познакомились с критериями, по которым будут оценивать работы на ЕГЭ. А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
Будьте внимательны: баллы из таблиц выше — первичные, а требования к абитуриентам на поступление выражены в тестовых. Чтобы понять, сколько заданий точно нужно решить, чтобы поступить, надо перевести баллы из одной системы в другую. Это можно сделать по таблице ниже.
| Первичные баллы | Тестовые баллы | Оценка |
|---|---|---|
| <11 | <36 | 2 |
| 11–25 | 36–55 | 3 |
| 26–38 | 56–72 | 4 |
| 39–56 | 73–100 | 5 |
6 рекомендаций, как подготовиться к ЕГЭ по химии
Единый государственный экзамен — это ответственная задача, от результатов подготовки к которой иногда многое зависит. Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
-
Узнайте все о структуре ЕГЭ и научитесь работать с КИМами.
-
Начинайте готовиться заранее. Но если получилось так, что осталось мало времени, составьте новый экспресс-план с помощью вашего преподавателя.
-
Ведите календарь подготовки к экзамену. Отмечайте на нем запланированные темы, разные методики, занятия у репетитора, пробные ЕГЭ и самоподготовку.
-
Распределяйте время на темы, исходя из ваших знаний. Больше учите то, что «западает», остальное — повторяйте.
-
Советуйтесь с учителем. Это может быть ваш преподаватель по химии или репетитор. Круто, если он сможет поделиться с вами опытом подготовки к ЕГЭ.
-
Заботьтесь о своем здоровье, не забывайте отдыхать, не лишайте себя живого общения. Все это может сказаться на вашем самочувствии, а значит, и баллах тоже.
Если вы хотите сдать ЕГЭ по химии на 100 баллов, советуем тщательно продумать, как вы будете готовиться к нему. Лучший из них — совмещать самостоятельную работу и дополнительные занятия.
На курсах подготовки к ЕГЭ по химии в Skysmart школьники отрабатывают все типы задач и разбирают критерии оценок. Для каждого из них мы составляем индивидуальный план, который приведет к нужным баллам. Он учитывает уровень знаний ученика и время до экзамена, что позволяет «выжать» максимум из подготовки. А еще мы рассказываем о ЕГЭ без «страшилок» и прикрас, чтобы школьник точно знал, что его ждет на экзамене. Ждем на первом бесплатном занятии!
Химия хоть и считается одним из сложных дисциплин, но также можно сказать про все остальные экзамены. Одно из главных отличий — изучается по школьной программе чаще всего не слишком углубленно, чтобы сдать хотя бы на средне-высокий балл. Плюс, дисциплина идет с класса седьмого — и то изучается только один раздел, а последний и самый сложный блок изучается только последние 2 года.
Начинаем
Чтобы узнать, как проводится сам экзамен, нужно найти официальную информацию. Она всегда находится на сайте ФИПИ — они составители единого госэкзамена и всех городских тестирований. Они отвечают за проверку знаний у школьников по всем предметам. Перед началом учебного года у них на сайте всегда выходит проект, в котором находится три документа:
- Спецификация — отвечает на все организационные вопросы, которые могут возникнуть у школьников. Также там расписаны баллы, формулировки и структура. Так как в течение года он обычно не изменяется, советуем прочитать его в самом начале, чтобы точно разобраться во всех интересующих тебя аспектах.
- Кодификатор — в нем будут все темы, которые стоит пройти, чтобы полностью подготовить теоретическую базу для сдачи. Хорошей идеей будет составить план, по которому будешь готовиться, на его основе — таким образом точно не пропустишь важные темы. Или сделай из него чек-лист — отмечай каждый пройденный пункт, чтобы видеть свой прогресс. *Пометка — то, что указано курсивом, учить не надо, так как они обычно не встречаются в КИМах.
- Демоверсия — проект КИМа, который скорее всего будет в текущем году на госах. Там есть четкие формулировки, которые будут встречаться в контрольно-измерительных материалах, плюс критерии оценивания развернутых заданий. Советуем распечатать отсюда справочные материалы — таблицу Менделеева, растворимости, ряд активности металлов. Их именно в таком виде будут выдавать в индивидуальном пакете в аудитории, поэтому если будешь пользоваться, пока готовишься, привыкнешь к ним и будешь быстро ориентироваться.
Также попробуй немного схитрить — скачай заодно файлы для экспертов, которые проверяют вторую часть. Там поймешь, какие недочеты не допускать.
Понять свой уровень
Одна из главных частей для начала подготовки — узнать, насколько плохо ты разбираешься в предмете. Если осознаешь, что у тебя не совсем нулевые знания, то прорешай разок демоверсию — неважно, будет у тебя два балла, ноль или гораздо больше. Запиши свой результат, чтобы видеть прогресс в процессе нарешивания и выучивания новой информации.
Структура
Всего будет тридцать четыре задания: в тесте двадцать восемь, а развернутых шесть. В целом их всех можно разделить на несколько блоков:
- Теоретические основы — всего номеров пять и только в тесте.
- Реакции — будет восемь упражнений, из которых два в письменной части.
- Неорганические — семь задач, из которых всего лишь одна развернутая.
- Органические — четыре, плюс еще одна с открытым решением.
- Методы познания — всего лишь дважды спрашивается и только в тестовом виде.
- Расчеты по формулам — четыре раза в тестовом виде и дважды в письменном.
Обычно за объемную долю тестирования дается лишь по одному баллу, здесь это правило тоже будет — только за номера 6, 7, 8, 14, 15, 22, 23, 24 будет получено максимум 2.
Всего больших разделов, знания которых будут проверяться в КИМе, три:
- Общая — строение атома, периодический закон, химическая связь, кристаллические решетки, скорость реакции, химическое равновесие, тепловой эффект, расчетные задачи.
Она проходится в течение всего времени изучения дисциплины, но, конечно, больше всего ей времени уделено в начале обучения, так как она покрывает базу. Это достаточно легкая тема, но все еще вызывает много проблем в начале обучения. Если учишь полностью с нуля за год, тебе предстоит долго с ней просидеть, потому что она действительно охватывает самые основы. Поймешь, как все работает на базовом уровне — быстро схватишь, как протекают остальные процессы.
- Неорганика — оксиды, основания, кислоты и соли; металлы, неметаллы.
Она же изучается только до конца девятого класса — в ОГЭ проверяются знания по ней. Если ты сдавал ОГЭ по предмету, то тебе будет гораздо легче готовиться к тестированию в одиннадцатом.
- Органика — алканы, алкены, алкадиены, алкины, циклы, бензол и его гомологи; галогенопроизводные; спирты, фенолы, альдегиды, кетоны, карбоновые кислоты, эфиры и жиры; амины, аминокислоты, углеводы и белки.
В целом для этой дисциплины теория и практика примерно равномерно распределена — над всем придется долго сидеть. Но это не значит, что тренироваться нужно столько же по времени, сколько учить новую информацию — на практику все еще делается упор. Обработаешь кучу задачек — улучшишь свои навыки, значит сможешь быстро делать все в аудитории. Не забывай, что время ограничено, и нужно уложиться в определенный промежуток, так еще и перепроверить и переписать все на бланки. Потренируйся дома с таймером — пиши пробники хотя бы раз в месяц, а лучше — раз в неделю. Ставь себе таймер, распечатывай КИМ, убери все ненужное со стола и сиди решай. Если у тебя проводятся в школе пробники — постоянно ходи на них: опыт получай как только угодно. Если несколько людей сдают у одного учителя, попробуйте попросить выделить вам немного дополнительных часов, чтобы решали в классе. Если еще учитель согласится проверять ваши письменные ответы — будет чудно. Если же препод не особо понимающий, то просто собирайтесь и проверяйте друг у друга, чтобы понимать, какие есть недочеты, и не допускать их.
Как составить систему
Когда составляешь план, во-первых, ориентируйся на кодификатор, во-вторых, разберись с помощью преподов или видео на YouTube, например, с каких тем стоит начать заниматься, а какие, наоборот, выгоднее оставить на потом. И внимательно следи за своей схемой — не отходи от нее, не изучай то, что находится в самом конце, если все еще пропущены разделы в середине. Иди по порядку — так гораздо выше шанс аккуратно уложить все в голове, чтобы не было проблем с пониманием.
Также помни: не зазубривай наизусть теорию — лучше уделить много времени, чтобы действительно понять почему вещества ведут себя подобным образом в реакциях. Эта дисциплина до ужаса логична — пойми пройденные процессы и тебе станет проще узнавать и выучивать новые.
Также уделяй внимание на изучение деталей, исключений, о которых даже не задумывался: ортофосфорная кислота является среднесильной, но в ЕГЭ считается слабой; а азотная кислота может восстанавливаться с образованием смеси продуктов, и только на основании логики можно выбрать верный ответ. Большинство таких ситуаций уже давно известны, поэтому советуем найти несколько видосов на YouTube, чтобы получше узнать все похожие ситуации. Плюс такие видео очень полезны для самоподготовки — у тебя есть кайфовые бесплатные материалы, так еще и с объяснением шарящих людей.
Пособия, которые тебе скорее всего пригодятся:
- Теория: «Репетитор по химии. Под редакцией — Егорова А.С.»;
- Практика: «Химия. Тематический тренинг. В.Н. Доронькин».
Их советуют преподаватели, так что точно не прогадаешь, если соберешься покупать.
Сборники же советуют выбирать от составителей, например, Д.Ю. Добротина. Конечно, их обязательно прорешивать, также веди статистику правильных решений и неверных, чтобы понимать, где у тебя сильное проседание, а где у тебя всегда верные ответы. Не переживай слишком сильно из-за ошибок: сделаешь множество дома — выше результат будет на реальном экзамене. Если запомнишь все свои недочеты, то в самой аудитории точно не допустишь их повторно. Главная проблема — стресс и паника. Они заставляют тебя потеряться и забыть все, что делал дома, в школе. Научись бороться с ними — лучший способ: ходи на любые олимпиады. Абсолютно не обязательно ходить именно по предмету: если это будет русский, математика или даже физическая культура — неважно, у тебя все равно будет новый опыт в стрессовой ситуации, особенно на более высоких этапах, чем школьный.
Как подготовиться к ЕГЭ по химии за 4 месяца Таисия Фламель. Как сдать ЕГЭ по химии. Методика подготовки к ЕГЭ по химии
Смотрите также:
Пробный вариант ЕГЭ 2021 по химии №8 с ответами
Напоминаем, что до дня «Х»
остается не так много времени, поэтому мы запускаем новый спецпроект, где будем
рассказывать, как подготовиться к ЕГЭ за несколько месяцев. Первый предмет –
химия.
1.
Для начала поймите, что заниматься надо
регулярно, чтобы вы смогли запомнить нужную информацию. Составьте распорядок
дня и запланируйте, что решать задачи по химии вы будете не менее часа в день.
2.
Если вы еще не приступали к подготовке, начните
с пробного теста. Обязательно выдерживайте временной режим, используйте только
разрешенные материалы (таблицу растворимости, Периодическую систему химических
элементов и ряд активности металлов). После – проверьте себя и посчитайте
баллы.
3. За
месяц до экзамена переходите к решению всего тестового билета с соблюдением
правил проведения экзамена. После проверки выписывайте те темы и вопросы,
которые вызвали ошибки и наибольшее затруднение. После их детальной проработки,
решайте тест еще раз.
Рекомендуем разбить темы
на несколько разделов и учить их в таком порядке:
1. Классификация
неорганических соединений. Основные
классы неорганической химии. Эти вопросы широко представлены в тестовой
части билета, и входят во вторую часть билета. Выучив примеры соответствующих
реакций можно приступать к теме ионных уравнений, гидролиза, решению задач.
2.Реакции ионного обмена,
гидролиз. Следует четко запомнить примеры сильных и слабых электролитов, не
забывать использовать таблицу растворимости.
3. Типы химических реакций. Окислительное – восстановительные реакции.
Электролиз. Надо четко помнить примеры окислителей, веществ с
окислительно-восстановительной двойственностью, отработать навык определения
степени окисления атомов элементов.
4. Типы химических реакций. Скорость химической реакции, химическое
равновесие. Внимательно смотрите на записи уравнений реакций, на агрегатные
состояния веществ.
5. Строение атома. Зависимость свойств химических элементов и их
соединений от положения в Периодической системе. Следует расписать электронное строение атомов 1,2,3,4
периодов.
6. Решение типовых, стандартных расчетных задач.
7. Классификация органических соединений. Необходимо повторить
общие формулы классов соединений, номенклатуру систематическую и тривиальную,
понятие функциональной группы.
8. Углеводороды и их реакционная способность. Следует выучить
способы получения и взаимные переходы между веществами.
9. Кислородсодержащие органические соединения. Выучите способы
получения и взаимные переходы между веществами.
10. Азотсодержащие органические соединения. Запомните способы
получения и взаимные переходы между веществами.
11. Решение задач на вывод формулы органического вещества.
12. Расчетные задачи повышенной трудности.
13. Виртуальная лабораторная работа.
При подготовке текста использованы материалы, предоставленные Сямтомовой Ольгой Владимировной, преподавателем химии, специалистом Центра по подготовке к ОГЭ/ЕГЭ «Феномен».
Государственное
бюджетное общеобразовательное учреждение
средняя
общеобразовательная школа №125
Красногвардейского
района Санкт-Петербурга
|
ПРИНЯТО Решением ГБОУ СОШ № 125 Красногвардейского протокол № 1 от 28 |
УТВЕРЖДАЮ Директор ГБОУ СОШ № 125 Красногвардейского ___________________________М. «___» _______________ |
План
подготовки к ОГЭ по химии
для
обучающихся 11 «Б» класса
на
2020-2021 учебный год
Ьаймашкина Татьяна Александровна
учитель химии
Санкт-Петербург
2020
Пояснительная
записка.
Программа
составлена на основе Обязательного минимума содержания основных образовательных
программ Федерального компонента государственного стандарта основного общего
образования по химии, базовый и профильный уровни.
Программа
предназначена для проведения консультационных занятий с учащимися 9 класса.
Реализация данной программы способствует использованию
разнообразных форм организации учебного процесса, внедрению современных методов
обучения и педагогических технологий.
Основной
формой организации учебного процесса является консультационная поддержка,
индивидуальные занятия, лекционные занятия, самостоятельная работа учащихся с
использованием современных информационных технологий.
План
подготовки
1. Изучение
ДЕМО версии.
2. Изучение
кодификатора 2020 – 2021 г.
3. Изучение
инструкции по заполнению бланков.
4. Повторение
учебного материала в следующей последовательности.
1)
Вещество
2)
Химическая реакция
3)
Элементарные основы неорганической химии
4)
Основы органических веществ
5)
Экспериментальные основы химии
6)
Химия и жизнь
5. Тренировочные
занятия по заданиям КИМов.
6. Правила
поведения на экзамене.
7. Пробный
экзамен.
8. Анализ
пробного экзамена, ликвидация пробелов
План
самостоятельной подготовки к ЕГЭ.
1. Познакомиться
со структурой экзаменационных работ прошлых лет.
2. Проанализировать
материал, который в них входит, и наметить последовательность его изучения.
3. Выбрать
учебные пособия, по которым необходимо заниматься.
4. Определить
наиболее простые и наиболее сложные разделы курса.
5. Работать
с курсом, обращая внимание на трудные разделы.
6. Работая
с текстом, обязательно задумываться над тем, что в нем говорится.
7. Составить
самостоятельные вопросы к отдельным фрагментам текста.
|
№ п/п |
Содержание |
Сроки |
|
Организационный блок |
||
|
1. |
Проведение Дня открытых дверей с |
14 ноября, 2020 |
|
2. |
Познакомить учащихся с материалами КИМов |
Октябрь |
|
3. |
Ориентирование учащихся на подготовку к диагностическим работам в формате ЕГЭ по химии. |
Октябрь |
|
4. |
Проведение диагностических работ в ходе подготовки и проведения ЕГЭ. |
В течение года |
|
5. |
Анализ результатов диагностических работ. |
В течение года (после каждой диагностической работы) |
|
Работа с учащимися |
||
|
6. |
Подготовка справочных, информационных, учебно- тренировочных материалов и оформление доступа к информационным ресурсам (стенды, настенные плакаты; графики консультаций для выпускников, сдающих ЕГЭ; |
Сентябрь (далее в течение года) |
|
7. |
Рекомендации учащимся о выходе в Интернет для самостоятельной отработки материала на базовом и сверхбазовом уровне в форме ЕГЭ. Интернет-ресурс:
· · |
1-2 раза в неделю в течение года |
|
8. |
Тренировочные работы на сайтах ФИПИ по подготовке к ЕГЭ в рамках школьной работы и самостоятельно в домашних условиях. |
В течение года: -еженедельно (четверг, пятница) ежедневно (дома) |
|
9. |
Мониторинговое исследование по химии. |
В течение года |
|
10. |
Организация групповой работы с учащимися 11 класса по химии. |
В течение года |
|
11. |
Индивидуальная консультация учащихся по вопросам ЕГЭ. |
В течение года |
|
12. |
Работа учащихся на уроках химии по подготовке к ЕГЭ. |
В течение года |
|
13. |
Организация повторения тем на уроках биологии и химии, требующих |
В течение года |
|
14. |
Использование информационных технологий на уроках повторения учебного материала при подготовке к итоговой аттестации. |
В течение года |
|
15. |
познакомить учащихся с:
|
В течение года |
|
16. |
проведение консультаций в 11 классе |
|
|
17. |
выделение времени на уроках для повторения |
В течение года |
|
18. |
применение различных видов деятельности (работа с текстами, |
В течение года |
|
19. |
применение различных форм контроля знаний (устно, письменно, |
В течение года |
|
20. |
самообразование по данной теме |
В течение года |
|
21. |
постоянный контроль за подготовкой учащихся 11 класса |
В течение года |
|
22. |
проведение пробных экзаменов |
В течение года |
|
23. |
мониторинг посещаемости и успешности подготовки |
В течение года |
Содержание курса.
Тема
1. Введение. Теоретические основы химии.
Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы.
Электронная конфигурация атома. Основное и возбужденное состояние атомов.
Закономерности изменения свойств элементов и их соединений по периодам и
группам.
Общая характеристика металлов IА–IIIА групп в связи с их положением в
Периодической системе химических элементов Д.И. Менделеева и особенностями
строения их атомов. Характеристика переходных элементов (меди, цинка, хрома,
железа) по их положению в периодической системе химических элементов Д.И.
Менделеева и особенностям строения их атомов.
Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в
Периодической системе химических элементов Д.И. Менделеева и особенностями
строения их атомов.
Ковалентная химическая связь, ее разновидности и механизмы образования.
Характеристики ковалентной связи (полярность и энергия связи). Ионная связь.
Металлическая связь. Водородная связь.
Электроотрицательность. Степень окисления и валентность химических элементов.
Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки.
Зависимость свойств веществ от их состава и строения.
Классификация
химических реакций в неорганической и органической химии.
Тепловой
эффект химической реакции. Термохимические уравнения.
Скорость
реакции, ее зависимость от различных факторов. Обратимые и необратимые
химические реакции. Химическое равновесие. Смещение химического равновесия под
действием различных факторов. Электролитическая диссоциация электролитов в
водных растворах. Сильные и слабые электролиты. Реакции ионного обмена.
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. Реакции
окислительно-восстановительные. Коррозия металлов и способы защиты от нее.
Электролиз расплавов и растворов (солей, щелочей, кислот).
Тема
2.
Неорганическая химия.
Классификация
неорганических веществ. Номенклатура неорганических веществ
(тривиальная и
международная). Характерные
химические свойства простых веществ –
металлов:
щелочных, щелочноземельных, алюминия; переходных металлов (меди, цинка, хрома,
железа).
Характерные химические свойства простых веществ – неметаллов: водорода,
галогенов, кислорода, серы, азота, фосфора, углерода, кремния.
Характерные
химические свойства оксидов: оснóвных, амфотерных, кислотных.
Характерные химические свойства оснований и амфотерных гидроксидов
Характерные химические свойства кислот.
Характерные химические свойства солей: средних, кислых, оснóвных; комплексных
(на примере соединений алюминия и цинка)
Взаимосвязь различных классов неорганических веществ.
Тема 3. Органическая
химия .
Теория строения органических соединений: гомология и изомерия (структурная и
пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах
органических веществ. Гибридизация атомных орбиталей углерода. Радикал.
Функциональная группа.
Классификация органических веществ. Номенклатура органических веществ
(тривиальная и международная).
Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов,
диенов, алкинов, ароматических углеводородов (бензола и толуола).
Характерные химические свойства предельных одноатомных и многоатомных спиртов,
фенола.
Характерные химические свойства альдегидов, предельных карбоновых кислот,
сложных эфиров.
Характерные химические свойства азотсодержащих органических соединений: аминов
и аминокислот.
Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды,
полисахариды).
Взаимосвязь
органических соединений.
Тема 4.
Методы
познания в химии. Химия и жизнь.
Правила работы в лаборатории.
Лабораторная посуда и оборудование. Правила безопасности при работе с едкими,
горючими и токсичными веществами, средствами бытовой химии. Научные методы
исследования химических веществ и превращений. Методы разделения смесей и
очистки веществ.
Определение характера среды водных растворов веществ. Индикаторы.
Качественные реакции на неорганические вещества и ионы. Качественные реакции
органических соединений.
Основные способы получения (в лаборатории) конкретных веществ, относящихся к
изученным классам неорганических соединений.
Основные способы получения углеводородов (в лаборатории).
Основные
способы получения кислородсодержащих соединений (в лаборатории).
Понятие о металлургии: общие способы получения металлов.
Общие
научные принципы химического производства (на примере промышленного получения
аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и
его последствия.
Природные источники углеводородов, их переработка.
Высокомолекулярные соединения. Реакции полимеризации и поликонденсации.
Полимеры. Пластмассы, волокна, каучуки
Вычисление массы растворенного вещества, содержащегося в определенной массе
раствора с известной массовой долей; вычисление массовой доли вещества в
растворе. Расчеты объемных отношений газов при химических реакциях.
Расчеты массы вещества или объема газов по известному количеству вещества,
массе или объему одного из участвующих в реакции веществ.
Расчеты теплового эффекта реакции. Расчеты массы (объема, количества вещества)
продуктов
реакции, если одно из веществ дано в избытке (имеет примеси)
Расчеты массы (объема, количества вещества) продукта реакции, если одно
из веществ дано в виде раствора с определенной массовой долей растворенного
вещества
Нахождение молекулярной формулы вещества
Расчеты массовой или объемной доли выхода продукта реакции от теоретически
возможного.
Расчеты массовой доли (массы) химического соединения в смеси.
Тематическое планирование.
|
Наименование |
Количество |
|
Тема 1. |
9 |
|
Тема 2. |
11 |
|
Тема 3. |
12 |
|
Тема 4. Методы |
2 |
|
Итого: |
34 |
Календарно —
тематическое планирование
|
№ |
Содержание |
Количество часов |
Даты проведения |
||
|
По |
По |
||||
|
Введение. |
9 |
||||
|
1 |
Строение |
1 |
|||
|
2 |
Виды |
1 |
|||
|
3 |
Общая |
1 |
|||
|
4 |
Классификация Тепловой |
1 |
|||
|
5 |
Скорость |
1 |
|||
|
6 |
Электролитическая |
1 |
|||
|
7 |
Гидролиз |
1 |
|||
|
8-9 |
Реакции |
2 |
|||
|
Тема 2. |
11 |
||||
|
10 |
Классификация |
1 |
|||
|
11 |
Характерные |
1 |
|||
|
12 |
Характерные |
1 |
|||
|
13 |
Характерные |
1 |
|||
|
14 |
Характерные |
1 |
|||
|
15-16 |
Вычисление |
2 |
|||
|
17-18 |
Расчеты |
2 |
|||
|
19-20 |
Взаимосвязь |
2 |
|||
|
Тема 4. Органическая |
12 |
||||
|
21 |
Теория |
1 |
|||
|
22 |
Характерные |
1 |
|||
|
23 |
Характерные |
1 |
|||
|
24 |
Характерные |
1 |
|||
|
25 |
Характерные |
1 |
|||
|
26 |
|
1 |
|||
|
27 |
Характерные |
1 |
|||
|
28 |
Биологически |
1 |
|||
|
29-30 |
Взаимосвязь |
1 |
|||
|
31-32 |
Нахождение |
1 |
|||
|
Тема 4. |
2 |
||||
|
33 |
Качественные |
1 |
|||
|
34 |
Общие |
1 |
|||
|
Итого: |
34 |
||||
Список
рекомендуемой литературы
Базовый уровень:
- «Химия. 11 класc» / Габриелян
О.С., Лысова Г.Г.; - «Химия. 10 класс» /
Габриелян О.С., Маскаев Ф.Н., Пономарев С.Ю., Теренин В.И.; - «Химия 8. Химия 9» /
Габриелян О.С.; - «Химия 8-9» /
Сатбалдина С.Т., Лидин Р.А.; - «Химия 8 класс. Химия 9
класс» / Минченков Е.Е. и др.; - «Химия: учебник для 8 и 9
классов средней общеобразовательной школы» / Кузнецова Л.М.
Повышенный
уровень:
- «Краткий курс химии» /
Кузьменко Н.Е., Еремин В.В., Попков В.А.; - «Пособие по химии для
поступающих в ВУЗы» / Хомченко Г.П.; - «Химия. Для школьников
старших классов и поступающих в вузы: Теоретические основы. Вопросы.
Задачи. Тесты. Учебное пособие» / Лидин Р.А., Молочко В.А., Андреева
Л.Л.; - «Химия. Краткий
справочник школьника. 8-11 классы» / Еремина Е.А., Еремин В.В.,
Кузьменко Н.Е.; - «Школьная энциклопедия химических
элементов» / Смолеговский А.М. и др.; - Химия. Справочник школьника и
студента; - «Химия в формулах. 8-11
классы» / Еремин В.В.; - «230 тестов по
химии» / Чунихина Л.А.
Высокий уровень:
- «Неорганическая химия:
10-11 классы. Теоретические основы. Углубленный курс» / Зайцев О.С.; - «Органическая химия:
10-11 классы. Теоретические основы. Углубленный курс» / Артеменко
А.И.; - «Органическая химия и
человек: 10-11 классы. Теоретические основы. Углубленный курс» /
Артеменко А.И.; - «Химия. 10-11 класс.
Профильный уровень: учебник для общеобразовательных учреждений» /
Еремин В.В., Кузьменко Н.Е., Лунин В.В.; - «Химия. Большой
справочник для подготовки к ЕГЭ: учебно-методическое пособие» /
Доронькин В.Н., Бережная А.Г., Сажнева Т.В., Февралева В.А.