Производство чугуна и стали
Ключевые слова конспекта: производство чугуна, производство стали, железная руда, чугун, сталь, руда, кокс, силикат кальция, пирит, доменная печь.
ПРОИЗВОДСТВО ЧУГУНА. ДОМЕННАЯ ПЕЧЬ
По объёму производства и потребления железо является важнейшим металлом. Обычно железо используется в виде сплавов. Отрасль промышленности, производящая железо и его сплавы, – чёрная металлургия.
Источником получения железа является железная руда. В руде основными компонентами являются соединения железа:
- Fe3O4 – магнетит (магнитный железняк),
- Fe2O3 – гематит (красный железняк),
- Fe2O3 nH2O – лимонит (бурый железняк),
- FeS2 – пирит (железный колчедан, серный колчедан).
Пирит сначала обжигают (в ходе производства серной кислоты), а огарок (Fe2O3) используют в производстве чугуна.
Продуктами производства являются чугун и сталь.
Чугун – сплав железа с углеродом, в котором массовая доля углерода составляет более 2%, а также имеются примеси кремния, фосфора, серы и марганца.
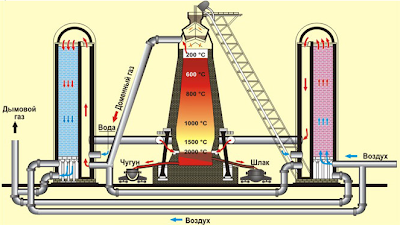
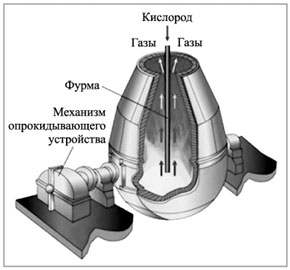
Производство чугуна осуществляют в доменных печах (см. рис). Сырьём для производства являются железная руда, кокс, известняк и горячий воздух.
Доменную печь загружают сначала коксом, а затем послойно агломератом и коксом. (Агломерат – это определённым образом подготовленная руда, спечённая с флюсом, в данном случае – с известняком.) Через специальные отверстия (фурмы) в нижнюю часть домны подаётся горячий воздух, обогащённый кислородом. В нижней части домны кокс сгорает, образуя СO2, который, поднимаясь вверх и проходя сквозь слои накалённого кокса, взаимодействует с ним и образует СО:
Руда последовательно претерпевает превращения:
В руде присутствует также пустая порода, которую образует главным образом кремнезём – SiO2. Это тугоплавкое вещество. Для превращения его в легкоплавкие соединения к руде добавляется флюс. Обычно это известняк. При взаимодействии его с кремнезёмом (SiO2) образуется силикат кальция:
СаСO3 + SiO2 = CaSiO3 + CO2↑ (800 °С)
Образующийся силикат легко отделяется в виде шлака.
При восстановлении руды железо получается в твёрдом состоянии. Постепенно оно опускается в более горячую часть печи – распар – и растворяет в себе углерод. Образуется чугун. Последний плавится и стекает в нижнюю часть домны, а жидкие шлаки собираются на поверхности чугуна, предохраняя его от окисления. Чугун и шлаки периодически выпускают через особые отверстия.
Когда металлическое железо выделяется в жидком состоянии, в нём сравнительно хорошо растворяется углерод. При кристаллизации такого раствора образуется чугун – сплав железа с углеродом. Он обладает высокой хрупкостью из-за большого содержания в нём карбида железа Fe3C (цементита), который образуется в результате побочных реакций:
3Fe + С = Fe3C
3Fe + 2СО = Fe3C + СO2
В чугуне содержатся примеси фосфора, серы. Сера ухудшает текучесть чугуна и вызывает красноломкость стали – хрупкость при нагревании до температуры красного каления. Фосфор вызывает хладноломкость стали – хрупкость при обычной температуре.
ПРОИЗВОДСТВО СТАЛИ
Сталь – сплав железа с углеродом, в котором массовая доля углерода составляет менее 2%.
Сущность получения стали из чугуна заключается в уменьшении содержания углерода в металле и возможно более полном удалении примесей – серы и фосфора, а также в доведении содержания кремния, марганца и других элементов до требуемых пределов.
Существует несколько способов переработки чугуна в сталь: мартеновский, бессемеровский и томасовский. Они различаются методами окисления.
В бессемеровском и томасовском способах окисление осуществляется кислородом воздуха, продуваемого через расплавленный металл. Во всех процессах углерод, содержащийся в металле, окисляется до СО и СO2, удаляемых из реакционной зоны. Кремний Si, марганец Мn, хром Сг и другие металлы, окисляясь, переходят в шлак в виде SiO2, МnО и т. д.
Механизм процесса окисления может быть представлен следующим образом. В первую очередь окисляется часть железа. Часть образующихся оксидов растворяется в металле и взаимодействует с примесями:
С + FeO ⇆ Fe + СО
Si + 2FeO ⇆ 2Fe + SiO2
2P + 5FeO ⇆ 5Fe + P2O5
Для максимального удаления примесей серы и фосфора необходимо, чтобы в процессе передела чугуна получались основные шлаки; это достигается путём добавления известняка или извести. Сера, содержащаяся в чугуне в виде FeS, реагирует с оксидом кальция СаО:
FeS + СаО = CaS + FeO
Образующийся сульфид кальция переходит в шлак. Образовавшийся P2O5 также взаимодействует с известью, образуя фосфат кальция, переходящий в шлак:
3СаО + P2O5 = Са3(РO4)2
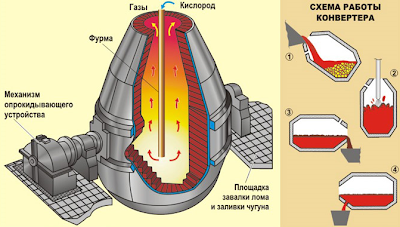
Бессемеровский и томасовский способы осуществляют в конвертерах. Конвертеры – аппараты грушевидной формы, изготовленные из специальной котельной стали (кожух) и футерованные изнутри огнеупорными материалами.
Конспект урока по химии «Производство чугуна и стали. Доменная печь». Выберите дальнейшее действие:
- Вернуться к Списку конспектов по химии
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
Понятие о металлургии: общие способы получения металлов
Металлургия — это наука о промышленных способах получения металлов. Различают черную и цветную металлургию.
Черная металлургия — это производство железа и его сплавов (сталь, чугун и др.).
Цветная металлургия — производство остальных металлов и их сплавов.
Широкое применение находят сплавы металлов. Наиболее распространенные сплавы железа — чугун и сталь.
Чугун — это сплав железа, в котором содержится 2-4 масс. % углерода, а также кремний, марганец и небольшие количества серы и фосфора.
Сталь — это сплав железа, в котором содержится 0,3-2 масс. % углерода и небольшие примеси других элементов.
Легированные стали — это сплавы железа с хромом, никелем, марганцем, кобальтом, ванадием, титаном и другими металлами. Добавление металлов придает стали дополнительные свойства. Так, добавление хрома придает сплаву прочность, а добавление никеля придает стали пластичность.
Основные стадии металлургических процессов:
- Обогащение природной руды (очистка, удаление примесей)
- Получение металла или его сплава.
- Механическая обработка металла
1. Нахождение металлов в природе
Большинство металлов встречаются в природе в виде соединений. Наиболее распространенный металл в земной коре — алюминий. Затем железо, кальций, натрий и другие металлы.
| Нахождение металлов в природе | ||
| Активные металлы — в виде солей | Металлов средней активности — в виде оксидов и сульфидов | Малоактивные металлы -в виде простых веществ |
| Хлорид натрия NaCl |
2. Получение активных металлов
Активные металлы (щелочные и щелочноземельные) классическими «химическими» методами получить из соединений нельзя. Такие металлы в виде ионов — очень слабые окислители, а в простом виде — очень сильные восстановители, поэтому их очень сложно восстановить из катионов в простые вещества. Чем активнее металл, тем сложнее его получить в чистом виде — ведь он стремится прореагировать с другими веществами.
Получить такие металлы можно, как правило, электролизом расплавов солей, либо вытеснением из солей другими металлами в жестких условиях.
Натрий в промышленности получают электролизом расплава хлорида натрия с добавками хлорида кальция:
2NaCl = 2Na + Cl2
Калий получают пропусканием паров натрия через расплав хлорида калия при 800°С:
KCl + Na = K↑ + NaCl
Литий можно получить электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси):
2LiCl = 2Li + Cl2
Цезий можно получить нагреванием смеси хлорида цезия и специально подготовленного кальция:
Са + 2CsCl = 2Cs + CaCl2
Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С:
MgCl2 → Mg + Cl2
Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция:
CaCl2 → Ca + Cl2
Барий получают из оксида восстановлением алюминием в вакууме при 1200 °C:
4BaO+ 2Al = 3Ba + Ba(AlO2)2
Алюминий получают электролизом раствора оксида алюминия Al2O3 в криолите Na3AlF6:
2Al2O3 → 4Al + 3O2
3. Получение малоактивных и неактивных металлов
Металлы малоактивные и неактивные восстанавливают из оксидов углем, оксидом углерода (II) СО или более активным металлом. Сульфиды металлов сначала обжигают.
3.1. Обжиг сульфидов
При обжиге сульфидов металлов образуются оксиды:
2ZnS + 3O2 → 2ZnO + 2SO2
Металлы получают дальнейшим восстановлением оксидов.
3.2. Восстановление металлов углем
Чистые металлы можно получить восстановлением из оксидов углем. При этом до металлов восстанавливаются только оксиды металлов, расположенных в ряду электрохимической активности после алюминия.
Например, железо получают восстановлением из оксида углем:
2Fe2O3 + 6C → 2Fe + 6CO
ZnO + C → Zn + CO
Оксиды металлов, расположенных в ряду электрохимической активности до алюминия, реагируют с углем с образованием карбидов металлов:
CaO + 3C → CaC2 + CO
3.3. Восстановление металлов угарным газом
Оксид углерода (II) реагирует с оксидами металлов, расположенных в ряду электрохимической активности после алюминия.
Например, железо можно получить восстановлением из оксида с помощью угарного газа:
2Fe2O3 + 6CО → 4Fe + 6CO2
3.4. Восстановление металлов более активными металлами
Более активные металлы вытесняют из оксидов менее активные. Активность металлов можно примерно оценить по электрохимическому ряду металлов:
Восстановление металлов из оксидов другими металлами — распространенный способ получения металлов. Часто для восстановления металлов применяют алюминий и магний. А вот щелочные металлы для этого не очень подходят – они слишком химически активны, что создает сложности при работе с ними.
Например, цезий взрывается на воздухе.
Алюмотермия – это восстановление металлов из оксидов алюминием.
Например: алюминий восстанавливает оксид меди (II) из оксида:
3CuO + 2Al = Al2O3 + 3Cu
Магниетермия – это восстановление металлов из оксидов магнием.
CuO + Mg = Cu + MgO
Железо можно вытеснить из оксида с помощью алюминия:
2Fe2O3 + 4Al → 4Fe + 2Al2O3
При алюмотермии образуется очень чистый, свободный от примесей углерода металл.
Активные металлы вытесняют менее активные из растворов их солей.
Например, при добавлении меди (Cu) в раствор соли менее активного металла – серебра (AgNO3) произойдет химическая реакция:
2AgNO3 + Cu = Cu(NO3)2 + 2Ag
Медь покроется белыми кристаллами серебра.
При добавлении железа (Fe) в раствор соли меди (CuSO4) на железном гвозде появился розовый налет металлической меди:
CuSO4 + Fe = FeSO4 + Cu
При добавлении цинка в раствор нитрата свинца (II) на цинке образуется слой металлического свинца:
Pb(NO3)2 + Zn = Pb + Zn (NO3)2
3.5. Восстановление металлов из оксидов водородом
Водород восстанавливает из оксидов только металлы, расположенные в ряду активности правее алюминия. Как правило, взаимодействие оксидов металлов с водородом протекает в жестких условиях – под давлением или при нагревании.
CuO + H2 = Cu + H2O
4. Производство чугуна
Чугун получают из железной руды в доменных печах.
Печь последовательно загружают сверху шихтой, флюсами, коксом, затем снова рудой, коксом и т.д.
1- загрузочное устройство, 2 — колошник, 3 — шахта, 4 — распар, 5 — горн, 6 — регенератор
Доменная печь имеет форму двух усеченных конусов, соединенных основаниями. Верхняя часть доменной печи — колошник, средняя — шахта, а нижняя часть — распар.
В нижней части печи находится горн. Внизу горна скапливается чугун и шлак и отверстия, через которые чугун и шлак покидают горн: чугун через нижнее, а шлак через верхнее.
Наверху печи расположено автоматическое загрузочное устройство. Оно состоит из двух воронок, соединенных друг с другом. Руда и кокс сначала поступают в верхнюю воронку, а затем в нижнюю.
Из нижней воронки руда и кокс поступают в печь. во время загрузки руды и кокса печь остается закрытой, поэтому газы не попадают в атмосферу, а попадают в регенераторы. В регенераторах печной газ сгорает.
Шихта — это железная руда, смешанная с флюсами.
Снизу в печь вдувают нагретый воздух, обогащенный кислородом, кокс сгорает:
C + O2 = CO2
Образующийся углекислый газ поднимается вверх и окисляет кокс до оксида углерода (II):
CO2 + С = 2CO
Оксид углерода (II) (угарный газ) — это основной восстановитель железа из оксидов в данных процессах. Последовательность восстановления железа из оксида железа (III):
Fe2O3 → Fe3O4 (FeO·Fe2O3) → FeO → Fe
Последовательность восстановления оксида железа (III):
3Fe2O3 + CO → 2Fe3O4 + CO2
Fe3O4 + CO → 3FeO + CO2
FeO + CO → Fe + CO2
Суммарное уравнение протекающих процессов:
Fe2O3 + 3CO → 2Fe + 3CO2
При этом протекает также частичное восстановление примесей оксидов других элементов (кремния, марганца и др.). Эти вещества растворяются в жидком железе.
Чтобы удалить из железной руды тугоплавкие примеси (оксид кремния (IV) и др.). Для их удаления используют флюсы и плавни (как правило, известняк CaCO3 или доломит CaCO3·MgCO3). Флюсы разлагаются при нагревании:
CaCO3 → CaO + CO2
и образуют с тугоплавкими примесями легкоплавкие вещества (шлаки), которые легко можно удалить из реакционной смеси:
CaO + SiO2 → CaSiO3
Материал для подготовки к ЕГЭ, ОГЭ
Производство чугуна и стали
Этапы производства
2
1 этап – обогащение руды
Железная руда (железняки магнитный Fe3O4 , красный Fe2O3 , бурый FeOOH)
Кокс (углерод, полученный при разложении каменного угля без доступа воздуха – его коксовании)
Флюсы (доломит MgCO3*Ca CO3 , известняк Ca CO3 ), необходимы для удаления примесей.
2 этап – выплавка чугуна (содержание углерода ≥ 2 % )
Процесс непрерывный, производится в доменных печах
Реакции, проходящие в доменной печи – восстановление железа из оксидов
Fe2O3 + 3 C → 2 Fe + 3 CO – Q
Fe2O3 + 3 CO → 2 Fe + 3 CO2 + Q
Виды выплавляемых чугунов:
|
Название чугуна |
Свойства |
Использование |
|
Белый (передельный) |
Содержит углерод в виде цементита(Fe3С), хрупкий |
Переплавка в сталь |
|
Серый |
Содержит графит, менее хрупок |
Изготовление радиаторов, моховых колес, скульптуры |
|
Сверхпрочный |
Содержит добавки Mg, высокопрочный |
Коленвалы двигателей |
|
Зеркальный |
Содержит добавки Mn |
Раскислитель (восстановитель) в производстве стали |
3 этап – выплавка стали (содержание углерода ≤ 1,9 % )
Химические реакции
|
Выжигание лишнего углерода |
Восстановление окисленного железа раскислителями |
|
2C + O2 → 2CO Fe3С + 2O2 → CO + 3FeO |
Mn + FeO → MnO + Fe MnO + SiO2 → MnSiO3 |
Виды сталеплавильных печей
|
Виды печей |
Особенности производства, преимущества |
|
Мартеновская печь |
Периодический процесс (6-8 ч). 900 т стали за одну плавку – можно разливать в крупную форму |
|
Кислородный конвертер |
Периодический процесс ( 40 мин.). Суммарная производительность выше – 2 млн.т. в год |
|
Дуговая электропечь |
Периодический процесс. Высокая температура ≥ 30000, возможно перемешивание, изменение скорости нагрева, время протекания процесса. Получение легированных сталей более высокого качества |
Способы обработки стали
Прокатка
Ковка
Штамповка
Волочение
Прессование
Производство
чугуна. Сырье:
железная руда.
Вспомогательные материалы: кокс (иногда природный газ), воздух, обогащенный кислородом, флюсы
(известняк, доломит). Основной химический процесс: содержащийся в руде оксид железа (III) восстанавливается оксидом
углерода (II). Кокс сгорает до оксида углерода (IV), при этом
выделяется теплота, необходимая для расплавления железа, шлаков, а также
проведения самой реакции. Оксид углерода (IV) восстанавливается коксом до
оксида углерода (II).
Побочные процессы: одновременно восстанавливаются оксиды других элементов, содержащихся в
железной руде: содержащаяся в руде тугоплавкая примесь (оксид кремния)
удаляется в виде шлака взаимодействием с оксидом кальция. Оксид кальция образуется при разложении
известняка или доломита. Особенности технологического процесса: чугун получают в специальных печах — домнах. В верхнюю часть домны
(колошник) подают последовательно сырье и вспомогательные материалы, в нижнюю
(горн) продувают противотоком воздух, предварительно нагретый в регенераторе за
счет сжигания колошникового газа. Производство непрерывное (однако засыпание
шихты и выпуск чугуна производятся периодически), используются теплота реакции
и принцип противотока.
Основной продукт: чугун.
Состав:
сплав железа, содержащий более 2,5% С; 0,3—5% Si; до 1% Mn; 0,1% S и 0,2% Р,
иногда легирующие металлы (Аl, Сr, Ni и др.).
Свойства:
самый дешевый металлический материал, обладает хорошими литейными и
антифрикционными свойствами, износостойкостью, способностью гасить вибрации.
Различают передельный, литейный и легированный чугун. Легированный чугун
отличается жаростойкостью и коррозионной стойкостью.
Применение:
передельный чугун — для производства стали; литейный — для изготовления
поршней, цилиндров, тормозных барабанов, шестерен, деталей автомобилей (задний
мост, картер, ступицы и др.); легированный — для изготовления дверец
мартеновских печей, колосников, деталей паровых котлов, печной арматуры,
футерованных плит, газотурбинных установок. Побочные продукты: шлак, колошниковый газ.
Утилизация побочных продуктов: шлак используют при производстве гравия, щебня, цемента, шлаковой ваты,
колошниковый газ — для обогрева воздухонагревателей.
Производство стали. Сырье: чугун, металлолом, оксиды железа.
Вспомогательные материалы: воздух, обогащенный кислородом, добавки (например, оксид кальция,
ферромарганец).
Основной химический процесс: содержащиеся в жидком чугуне элементы (углерод, кремний, марганец,
фосфор и сера) окисляются кислородом. Образовавшийся оксид железа (II) тоже
принимает участие в окислении примесей. Оксиды кремния и фосфора с известью
образуют шлак.
Побочные процессы: для удаления образующегося оксида железа (II) добавляют ферромарганец
(так называемый раскислитель).
Оксид марганца (II) переходит в шлак:
Особенности технологического процесса:
1) кислородно-конверторный способ.
Окисление примесей проводят в специальных аппаратах— конверторах продуванием
воздуха через расплавленный чугун (нижнее дутье) или кислорода над расплавом
(верхнее дутье);
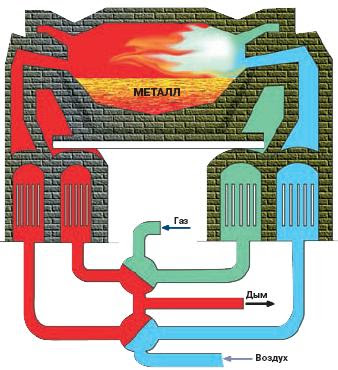
2) мартеновский способ. Примеси окисляют в
мартеновских печах, пропуская предварительно нагретый в регенераторах воздух и
топочные газы над расплавленным чугуном. Производство периодическое.
Выплавка стали в электронно-лучевой печи.
Выплавка стали в электропечи.
Основной продукт: сталь.
Состав:
сплав железа, содержащий менее 2% С, 0,35% Si, 0,6% Mn, 0,06% S, 0,07% Р,
легирующие металлы (Со, Cr, Ni, W, A1 и др.).
Свойства:
высокая прочность, пластичность, свариваемость, жаростойкость, износостойкость.
Применение:
конструкционные материалы, в строительстве, производстве труб для газо- и
нефтепроводов, деталей машин и механизмов (оси, шестерни, пружины, коленчатые
валы), аппаратов и деталей в химическом машиностроении.
Побочные продукты: шлак, отходящий газ.
Утилизация побочных продуктов: шлак, содержащий фосфор, используют в качестве минеральных удобрений. Новейшим
направлением в производстве стали является прямое восстановление железной руды
водородом, природным или генераторным газом, минуя доменные процессы. При этом
получают губчатое железо, состав которого в отличие от доменного чугуна очень
близок к стали. Мартеновский способ в настоящее время также устарел. Гораздо
более прогрессивными являются конверторный и электроплавильный. Происходит
бурное развитие технологии непрерывной разливки стали благодаря ее
исключительно высокой эффективности. Основными направлениями экономического и
социального развития до 2000 г. предусмотрено увеличить выплавку конверторной
стали и электростали в 1,3—1,4 раза, разливку стали непрерывным способом не
менее чем в 2 раза и выпуск металлических порошков более чем в 3 раза.
|
Углеродистые стали |
||
|
Тип стали |
Содержание |
Применения |
|
Низкоуглеродистая |
0,2 |
Общее |
|
Среднеуглеродистая |
0,3-0,6 |
Балки и |
|
0,6-1,5 |
Сверла, |
Источник: ресурсы Интернет
Дополнительный материал по вопросу:
Химия, 11 класс
Урок № 17. Принципы химического производства. Промышленное получение металлов. Производство чугуна и стали
Перечень вопросов, рассматриваемых в теме: урок посвящён ознакомлению с принципами химического производства, на примере промышленного получения ряда наиболее значимых веществ: серной и азотной кислот, аммиака и метанола. На уроке учащиеся познакомятся с понятием металлургии, узнают о производстве чугуна и стали.
Глоссарий
Конверсия — процесс переработки газов с целью изменения состава исходной газовой смеси.
Металлургия – наука о промышленных способах получения металлов из руд, а также об их механической и химической обработке.
Принцип Ле Шателье — Брауна — если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия, то в системе усиливаются процессы, направленные в сторону противодействия изменениям.
Промотор — вещество, добавляемое к катализатору в небольших количествах с целью улучшения его свойств, таких, как активность, селективность или стабильность.
Руда — минералы или чёрная порода, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно.
Сепаратор — аппарат, который разделяет продукт синтеза на фракции с разными характеристиками (например, отделить взвеси от жидкости).
Сталь – сплав железа, содержащий 0,02-2,14% углерода, небольшие количества кремния, марганца, фосфора и серы, а также не менее 45% железа. Если в стали содержится от 0,6 до 2,14% углерода, то такую сталь называют высокоуглеродистой.
Сырьё – природные материалы, используемые в промышленности для получения различных продуктов и ещё не прошедшие промышленную переработку.
Турбокомпрессор — устройство, которое сжимает газы для увеличения давления внутри системы.
Химическая промышленность — отрасль хозяйства, которая производит продукцию на основе химической переработки сырья.
Чугун – это сплав железа с углеродом, содержащий не менее 2,14% углерода, а также кремний марганец, серу и фосфор. Как правило, чугун хрупок.
Чугун белый — сплав железа с углеродом, в котором весь углерод находится в связанном виде (Fe3C).
Чугун серый — сплав железа с углеродом, в котором присутствует графит в виде хлопьевидных, пластинчатых или волокнистых включений.
Основная и дополнительная литература по теме урока
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тесто по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
Теоретический материал для самостоятельного изучения
«Зелёная» химия — научное направление в химии, к которому относятся любое усовершенствования химических процессов, положительно влияющие на окружающую среду. Данное направление возникло в 90-е годы XX века. Принципы «зелёной» химии:
- лучше предотвратить образование загрязнений, чем потом от них избавляться.
- Синтез веществ, следует планировать так, чтобы максимальное количество используемых материалов вошло в конечный продукт.
- Стремиться минимизировать энергетические затраты (понизить давление, понизить температуру).
- Вещества и процессы следует выбирать так, чтобы минимизировать вероятность несчастных случаев.
Способы реализации принципов «зелёной» химии:
- Поиск новых путей синтеза.
- Разработка методов синтеза на основе возобновляемых реагентов.
- Замена традиционных органических растворителей в технологических процессах (вода, биоразлагающиеся растворители, сверхкритические жидкости).
Последовательное использование принципов Зелёной химии постепенно приводит к снижению затрат на производство, потому что исчезают затраты на уничтожение, переработку побочных продуктов и использованных растворителей, так как их не образуется, а сокращение числа стадий ведет к экономии энергии. Перспективной для развития Зелёной химии является биотехнология (биоинженерия), так как ряд промышленно важных химических соединений может быть синтезирован с помощью микроорганизмов, растений, грибов, животных с высокими выходами и низкими затратами.
Для того, чтобы количественно оценить влияние химического производств на окружающую среду, профессором Р. Шелдоном были введены две основные характеристики: Е-фактор и атомная эффективность. Величина Е-фактора определяется как отношение массы всех побочных продуктов к массе целевого продукта, то есть этот фактор позволяет оценить количество отходов и степень использования сырья. Чем больше Е-фактор, тем менее «зелёной» является реакция или процесс. Например:
|
Производство |
Объём производства, тонн/год |
Е-фактор |
|
Нефтеперетаботка |
106 – 108 |
0,1 |
|
Тонкий химический синтез |
102 – 104 |
5 — 10 |
|
Фармацевтический синтез |
10 – 103 |
25 — 100 |
Величина Е-фактора в нефтепереработке мала, так как в основном все фракции нефти находят дальнейшее применение, то есть на данных производствах мало отходов. Максимальное значение Е-фактора имеет процесс синтеза лекарственных препаратов, так как это очень сложные производства, с большим числом стадий, а многие лекарства – чистые изомеры, для их синтеза используется большое число химических веществ.
Атомная эффективность – показатель, который рассчитывают как отношение молярной массы целевого продукта к сумме молярных масс всех остальных продуктов. Чем ближе атомная эффективность к 100%, тем более зеленой является данная реакция.
Промышленный органический синтез — раздел органической химической технологии, который изучает различные стороны получения органических соединений: способы синтеза, методики, идентификация, аппаратура и другие.
Промышленный органический синтез подразделяется на основной (производство метанола, анилина, уксусной кислоты, полимеров) и тонкий (производство красителей, лекарственных и душистых веществ, средств защиты растений). Важнейшими промышленными источниками органических веществ являются синтез-газ, природный газ, нефть и каменный уголь. В синтезах сложных органических соединений различают исходные вещества, промежуточные продукты и готовый продукт.
Зеркальный чугун — чугун с содержанием марганца 15-30%, углерода 4,5-6,5 %. Применяется в производстве стали. В изломе имеет характерный зеркальный блеск. Производился до 70-х гг. 20 в. в доменных печах. Применялся для получения чугуна специальных видов и в качестве раскислителя при выплавке стали.
Серый чугун применяется наиболее широко в таких отраслях, как машиностроение, строительство, также применяется в сантехнике. В зависимости от содержания углерода серый чугун делится на доэвтектический (с содержанием углерода от 2,14 до 4,3 %), эвтектический (с содержанием углерода 4,3 %) и заэвтектический (с содержанием углерода от 4,3 до 6,67 %). Также существует перлитный серый чугун: он имеет высокие прочностные свойства и применяется для изготовления втулок, цилиндров, различных нагруженных деталей двигателей и т.д. Для деталей, где не нужна такая высокая прочность, используют серый чугун с ферритно-перлитной металлической основой.
Белый чугун имеет низкие механические свойства и более хрупок, поэтому имеет ограниченное применение: из него изготавливают детали простой конфигурации, которые применяются для работы в условиях повышенного абразивного износа. Для повышения износостойкости белого чугуна, его легируют карбидообразующими элементами (Cr, Mo W, и др.), что повышает его износостойкость.
Половинчатый чугун содержит часть углерода в связанном виде (карбиды) и часть углерода в свободном состоянии. Такой вид чугуна применяется в качестве фрикционного материала, который работает в условиях сухого трения (поэтому из него производят тормозные колодки), а также для изготовления деталей, способных работать в условиях повышенной износостойкости (мукомольные, прокатные, бумагоделательные валки).
Существуют различные виды стали, все из которых находят применение в разных отраслях промышленности. По химическому составу стали делят на легированные и углеродистые. Последние по содержанию углерода подразделяют на низкоуглеродистые (до 0,25% углерода), среднеуглеродистые (0,3—0,55% углерода) и высокоуглеродистые (0,6—2% углерода); а легированные стали подразделяют по содержанию легирующих элементов на низколегированные — до 4% легирующих элементов, среднелегированные — до 11% легирующих элементов и высоколегированные — свыше 11 % легирующих элементов. Легированные стали маркируются цифрами и буквами, которые указывают примерный состав стали. Буква показывает, какой легирующий элемент входит в состав стали, стоящая за буквой цифра обозначает среднее содержание элемента в процентах ( при этом если его <1%, то цифра не ставится). Первые две цифры указывают содержание углерода в сотых долях процента. Маркировка по ГОСТ для обозначения легирующих элементов: А — Азот, Б — Ниобий, В —Вольфрам, Г — Марганец, Д — Медь, К — Кобальт, М — Молибден, Н — Никель, П — Фосфор, Р — Бор, С — Кремний, Т — Титан, Ц — Цирконий, Ф — Ванадий, Х — Хром, Ю — Алюминий.
Примеры видов стали:
сталь 18ХГТ — 0,18 % С, 1 % Сr, 1 % Мn, около 0,1 % Тi;
сталь 03Х13АГ19 — 0,03 % С, 13 % Сr, 0,2—0,3 % N, 19 % Мn.
По назначению стали бывают:
1) инструментальные, из которых изготовляют режущие и мерительные инструменты;
2) конструкционные — для изготовления машиностроительных и строительных изделий: для изготовления силовых пружин, амортизаторов, рессор, в приборостроении — для мембран, пружин, подвесок.
3) с особыми физическими и химическими свойствами, например, с определенными магнитными характеристиками, нержавеющие, жаростойкие.
Примеры и разбор решения задач тренировочного модуля
- Пример задачи. Сколько грамм раствора серной кислоты с массовой долей 96% необходимо влить в 1 л воды, чтобы получить раствор с массовой долей 10 %. Ответ представьте в виде целого числа.
Решение. Для решения задач на разбавление (смешение) растворов можно применить «правила креста». Суть этого правила заключается в составлении «креста», состоящего из двух пересекающихся линий. В центре указывают концентрацию, которую необходимо получить, у концов линий креста слева – концентрации исходных растворов (большую (а) – сверху, меньшую (b) — снизу), у концов линий креста справа –концентрации (или массы) растворов, которые получают вычитанием из одной величины другой, по направлению стрелочек (по модулю). В общем виде схема решения задач по правилу креста имеет вид:
То есть, из величины а вычитаем х, записываем как ma, и из b вычитаем х, записываем как mb. Таким образом, следует взять mа грамм раствора с массовой долей а% и прибавить к нему mB грамм раствора с массовой долей b% для получения концентрации х.
У нас есть два раствора: вода и серная кислота. Вода — чистый растворитель, следовательно, массовая доля растворённого в ней вещества равна 0%, так как это меньшее значение, записываем его в левом нижем углу. Исходная концентрация серной кислоты 96% — наибольшее значение, записываем в левом верхнем углу. Посередине – искомую концентрацию – 10%.
То есть для получения серной кислоты массовой долей 10 %, необходимо смешать 10 грамм серной кислоты массовой долей 96% и 86 грамм воды.
Но нам нужно узнать, как получить 10% раствор серной кислоты при ее растворении в 1 литре. Поэтому пользуемся пропорцией:
10 г серной кислоты — 86 г воды
х г серной кислоты — 1000 г воды
х = 116,3 г
Ответ: m (серной кислоты) = 116 г
2) Пример задачи. Добавьте в таблицу Менделеева недостающие химические элементы, которые входят в состав чугуна и стали.
Решение. Давайте вспомним, какие элементы входят в IV, V, VI, VII и VIII группы таблицы Менделеева.
Для решения данной задачи для начала необходимо вспомнить, какие элементы входят в состав чугуна и стали: C, Si, P, S, Mn, Fe.
Все знают, что атомный номер углерода – 12, поэтому его место легко найти в таблице. Далее вспоминаем, что углерод и кремний находятся в одной группе и заполняем окошко ниже. Переходим к VI группе, вспоминаем, какие элементы относятся к халькогенам и добавляем недостающий: S. Далее вспоминаем, какая валентность у марганца и располагаем его в группе VII. Остается два окошка. Железо относится к металлам побочной подгруппы, данное окошко свободно в VIII группе. Ну, и наконец, ставим P в V группу.
Химическая технология
Анализ результатов экзаменов, проведенных в
форме ЕГЭ, показывает, что учащиеся часто
допускают ошибки при ответе на вопросы части А
под номерами 27 и 29, составленные для проверки
знаний о способах получения веществ, оптимальных
условиях проведения химических реакций.
Мини-справочник, составленный мной в виде
обобщенных таблиц (табл. 1–7) и кратких сведений
по химической технологии, поможет в подготовке к
экзаменам по химии, а также при проведении
занятий по политехническим разделам химии и
профильных элективных занятий “Химия в
промышленности”.
Химическая технология – наука о
наиболее экономичных методах и средствах
массовой химической переработки природного
материала (сырья) в продукты потребления и
промежуточные продукты, применяемые в различных
отраслях народного хозяйства.
Главная задача химии и химической технологии –
это производство разнообразных веществ и
материалов с определенным комплексом
механических, физических, химических и
биологических свойств.
Общие принципы химической технологии:
1. Распределение производственного процесса по
стадиям.
2. Выбор и обогащение сырья.
3. Механизация и автоматизация всех
производственных процессов.
4. Непрерывность производства.
5. Комбинирование различных химических
производств.
6. Создание оптимальных условий для протекания
химических реакций.
7. Применение катализаторов.
8. Использование теплоты химических реакций.
9. Применение теплообмена.
10. Максимальное увеличение поверхности
соприкасающихся реагирующих веществ.
11. Использование противотока.
12. Применение циркуляционных процессов.
Таблица 1
Производство серной кислоты
контактным способом из пирита
|
Химическая реакция, |
Аппарат |
Назначение аппарата |
Принципы химической |
|
4FeS2 + 11O2 = 2Fe2O3 t = 800 °С |
Печь для обжига |
Обжиг твердого |
1. Обогащение сырья.
2. 3. Противоток. 4. Теплообмен. 5. Использование теплоты химической реакции. 6. Применение катализатора. 7. Автоматизация и механизация процессов |
|
– |
Циклон |
Очистка SO2 от |
|
|
Электрофильтр |
Очистка SO2 от |
||
|
Сушильная башня |
Очистка SO2 от |
||
|
Теплообменник |
Подогрев сернистого |
||
|
2SO2 + O2 t = 400 °C, катализатор: V2O5 |
Контактный аппарат |
Окисление оксида |
|
|
SO3 + H2O = H2SO4 nSO3 + H2SO4 = H2SO4•nSO3 |
Поглотительная башня |
Получение олеума – |
Таблица 2–3
Таблица 4–7
Производство алюминия
Технология производства
1. Очистка бокситов от примесей оксидов
кремния, железа и получение чистого Al2O3.
2. Расплавление криолита (Na3[AlF6])
при t = 1000 °C и добавление в него Al2O3
(10 % по массе).
3. В процессе электролиза Al2O3
(рис. 1) на графитовом катоде образуется
расплавленный Al, а на аноде – СО2.
Криолит остается в расплаве.
2Al2O3
4Al + 3О2,
О2 + С = СО2.
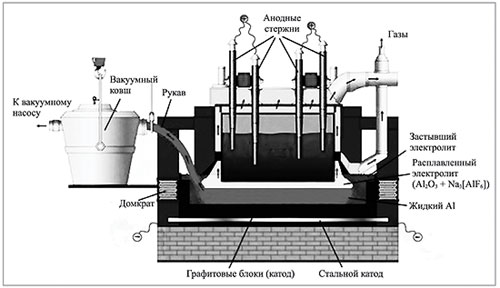 |
Рис. 1. Схема электролизера
|
Производство чугуна
Химические реакции, лежащие в основе
производства чугуна доменным способом (рис. 2):
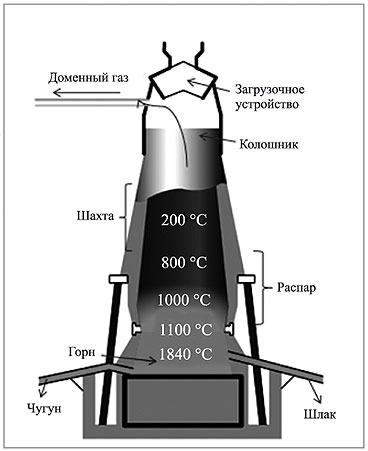 |
Рис. 2. Схема доменной печи для
|
получение восстановителя:
C + O2 = CO2 + 402 кДж,
CO2 + C 2CO;
восстановление железа:
Fe3O4 + CO 3FeO + CO2,
FeO + CO Fe + CO2;
суммарное уравнение восстановления железа из
руды:
Fe3O4 + 4CO 3Fe + 4CO2;
образование шлаков:
CaCO3 CaO + CO2,
CaO + SiO2 CaSiO3
(шлак).
Способы переработки чугуна в сталь
Химические реакции, лежащие в основе
переработки чугуна в сталь (рис. 3, 4, 5):
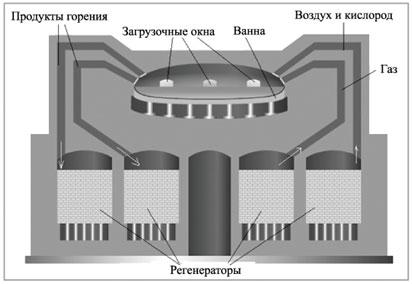 |
Рис. 3. Мартеновский способ
|
|
|
Рис. 4. Кислородно-конвертерный способ
|
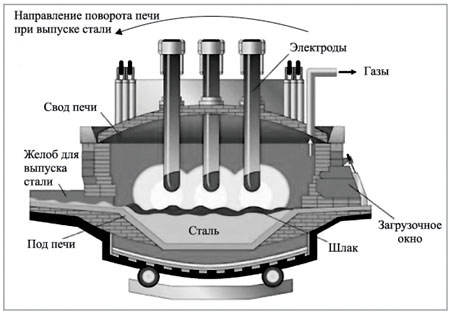 |
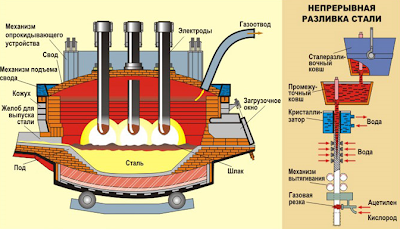
Рис. 5. Получение стали в электропечах |
окисление чугуна и примесей,
содержащихся в чугуне:
2Fe + O2 2FeO,
2C+ O2 2CO,
2Mn + O2 2MnO,
Si + O2 SiO2,
4P + 5O2 2P2O5,
S + O2 SO2;
окисление примесей оксидом железа(II):
2FeO + C 2Fe + CO2,
2FeO + Si 2Fe + SiO2,
FeO + Mn Fe + MnO,
5FeO +2P 5Fe + P2O5;
образование шлаков:
CaO + SiO2 CaSiO3,
3CaO + P2O5 Ca3(PO4)2;
раскисление стали:
FeO + Mn Fe + MnO,
MnO + SiO2 MnSiO3
(шлак).
Получение феноло-формальдегидной
смолы
Реакция поликонденсации (многостадийный
процесс):
Л и т е р а т у р а
Эпштейн Д.А. Учителю об основах химической
технологии. Пособие для учителей. М.: Просвещение,
1975; Цветков Л.А. Органическая химия. Учебник
для учащихся 10–11 классов общеобразовательных
учреждений. М.: Владос, 2001; Рудзитис Г.Е.,
Фельдман Ф.Г. Химия. 9 класс. Учебник для
общеобразовательных учреждений. М.: Астрель, 2003;
Сборник нормативных документов. Химия. Примерные
программы по химии. Сост. Э.Д.Днепров,
А.Г.Аркадьев. М.: Дрофа, 2008; Большая энциклопедия
Кирилла и Мефодия. Компакт-диск, 2003.
Р.М.ЧАРУШНИКОВА,
учитель гимназии № 152,
г. Казань
Среди многих
материалов, используемых человеком, особая роль принадлежит чёрным металлам,
то есть сплавам железа с углеродом и другими элементами.
Первое железо,
которое добыл человек, было неземным. Метеориты, падающие на Землю, имели
железную или железо-никелевую основу.
Древние люди
считали железо подарком Богов, так как оно приходило с неба и превосходило по
прочности многие известные тогда материалы.
Спустя столетия
люди поняли, что железо лежит под его ногами, но в чистом виде оно не
встречается. Его получение – это сложный технологический процесс.
Древние металлурги
в горнах выплавляли сталь, при этом получали ещё и чугун. Чугун
они называли «свинским железом» (свиньёй, или чушкой), так как он был очень
хрупок и не поддавался ковке.
Но затем поняли,
что при повторном плавлении чугун превращается в сталь, так как лишний углерод
при этом выгорает.
И только в 14 веке
было создано устройство – доменная печь, в которой и началось
производство чугуна.
В 30-х годах и в
послевоенные годы в Советском союзе увеличилось производство доменных печей.
Для производства чугуна
необходима железная руда, кокс и флюсы. Из железных руд
промышленное значение имеет красный железняк, содержащий 60-70%
оксида железа три и магнитный железняк, в котором 55-60% железной
окалины.
По запасам
железных руд Россия занимает ведущее место. Железные руды залегают на Урале, в
Курской области, Западной Сибири и других местах.
Основную массу
железной руды получают в России открытым способом. В открытых карьерах руду
добывают взрывным способом. Для этого бурят скважины, закладывают взрывчатое
вещество и производят взрыв.
Раздробленную руду
доставляют на обогатительную фабрику, здесь её измельчают и обогащают, то есть
рудный материал и пустую породу разделяют и получают концентрат – продукт с
повышенным содержанием оксидов железа.
Затем концентрат
смешивают с флюсами, известняком или доломитом, а также коксом. Все компоненты
перемешивают и затем спекают для выгорания серы и разложения известняка.
Полученный таким образом материал – шихта поступает на рудный двор
доменного цеха, который представляет собой сложный комплекс различных
сооружений: там есть доменная печь, литейный двор, воздухонагреватели и другие.
Специальная
скиповая тележка (вагонетка) подаёт шихту в воронку доменной печи. В нижней
части печи установлены фурмы для подачи нагретого воздуха. За одну минуту в
печь вдувается более шести тысяч кубических метров воздуха.
Воздух
предварительно нагревается в воздухонагревателях – регенераторах.
Доменная печь – это аппарат
длительного действия.
Она непрерывно
работает в течение нескольких лет. Сверху печи – шихта, а снизу раскалённые
газы. Температура здесь постепенно повышается, и создаются условия для
восстановления железа. В нижней части домны кислород воздуха реагирует с
углеродом кокса с выделением большого количества тепла.
Образовавшихся
оксид углерода четыре взаимодействует с раскалённым коксом и превращается в
оксид углерода два, который используется в качестве восстановителя железа из
его оксидов.
Для ускорения
восстановления в печь добавляют природный газ, содержащий метан. При его
горении образуется углекислый газ и вода. Оксид углерода четыре и водяной пар
реагируют с углеродом кокса и доменный газ обогащается восстановителями:
оксидом углерода два и водородом. Сейчас доменный газ используют в качестве
топлива – электроэнергии.
Восстановление
железа
начинается при температуре 300 градусов по Цэльсию. Сначала из
оксида железа три образуется железная окалина.
Затем окалина
восстанавливается до оксида железа два.
А из оксида железа
два получают восстановлением металлическое губчатое железо.
Губчатое железо
постепенно опускается в зону температуры 1100 градусов по Цэльсию, где оно
расплавляется. Часть этого железа реагирует с углеродом и превращается в карбид
железа.
Карбид железа и
углерода растворяются в жидком железе. Кремний, марганец, фосфор и сера,
которые получаются из оксидов, растворяются в расплавленном железе и образуется
жидкий чугун – сплав железа с углеродом, кремнием, марганцем,
фосфором и серой.
За сутки доменная
печь потребляет 68 вагонов коксованного угля и 220 вагонов железной руды.
Жидкий чугун
скапливается в горне. Из чугуна выливают крупные массивные детали, трубы,
большая часть чугуна идёт на производство стали.
Например, в
Новолипецком металлургическом комбинате производят более трёх с половиной
миллионов тонн чугуна в год. На производство этого комбината было потрачено
столько металлоконструкций, что из них можно было бы соорудить 10 Эйфелевых
башен.
Сталь можно
получить несколькими способами.
Рассмотрим конверторный
способ получения. Конвертер имеет металлический кожух, а
изнутри выложен огнеупорным кирпичом.
Через фурму
подаётся воздух, обогащённый кислородом. Сначала в конвертер загружают
металлолом, затем заливают жидкий чугун. Через желоб в конвертер поступает
железная руда, известь, окалина.
Затем через фурму
вдувается воздух, обогащённый кислородом. Температура при этом достигает 2400
градусов по Цэльсию. В производстве передела чугуна сначала окисляется железо,
концентрация которого в чугуне больше, чем других веществ.
Оксид железа два,
перемешиваясь с расплавом, окисляет кремний, марганец, фосфор и углерод.
Газообразные
продукты окисления удаляются, а остальные образуют шлак. За 1 год можно
получить около одного миллиона тонн шлака. Его хватило, чтобы обсыпать
Московскую кольцевую автомобильную дорогу (МКАД).
Затем происходит
выжигание углерода чугуна кислородом с образованием оксида углерода два.
После плавки
преступают к выпуску металла. В расплаве ещё содержится оксид железа два, от
которого сталь необходимо освободить. Для этого в жидкий металл добавляют
раскислители. После выпуска стали шлак идёт на производство цемента,
шлакоблоков, шлаковаты. Из стали изготавливают трубы, валы, стальные листы
используют для кузовов автомобилей, из стали делают рельсы, балки, инструменты,
подшипники.
Способ получения
стали в мартэновских печах аналогичен. Мартэновская печь – крупное сооружение.
Передняя стенка печи имеет окна, через которые подаётся шихта. В задней стенке
есть отверстия для выпуска стали и шлака.
Для ускорения
процесса плавки в мартэновскую печь вводится воздух, обогащённый кислородом.
После полного расплавления шихты в печь вводят оставшуюся железную руду,
которая вызывает интенсивное кипение. В период кипения металл освобождается от
серы, уменьшается содержание углерода. Полученная сталь через жёлоб сливается в
ковши. В процессе выплавки в металл вводят легирующие элементы.
Лучший способ
получения стали осуществляется в электропечах.
Здесь применяют
электроэнергию, что позволяет получать высокие температуры, в таких печах
получают самую лучшую нержавеющую сталь. Электропечь имеет стальной кожух, а
изнутри выложена огнеупорным кирпичом. Печь имеет рабочее окно и выпускное
отверстие со сливным жёлобом. Основные элементы электропечи – это
электроды, которые могут опускаться и подниматься.
Шихту загружают
сверху в печь. В шихту добавляют также известняк. Под действием высоких
температур шихта плавится при температуре 3500 градусов по Цэльсию. Вводятся
раскислители. По окончании правки металл разливают в ковши. Слитки стали
раскатывают в листы нужной толщины и закатывают в рулоны.
Если весь чугун,
произведённый в печи превратить в стальной лист, то получится такая полоса,
которой можно обернуть Землю по экватору 20 раз.
Таким образом,
получение чугуна и стали – сложный процесс, который состоит из множества
стадий. Сырьём для получения чугуна и стали является железная руда. Основная
масса чугуна идёт на производство стали. Сущность этого процесса заключается в
уменьшении содержания углерода в чугуне. Сталь получают в конвертерах, мартэновских
печах или в электропечах.