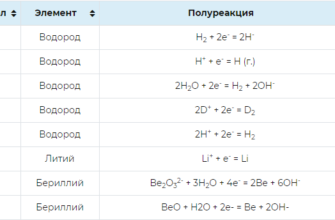
Таблица электроотрицательности химических элементов по Лайнусу Полингу
Автор Владислав Панарин На чтение 2 мин Просмотров 13.9к. Опубликовано 18.07.2022 Обновлено 23.07.2022
Вам также может понравиться
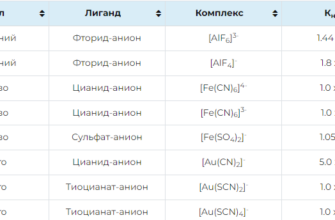
Константы нестойкости комплексных соединений.
014.6к.
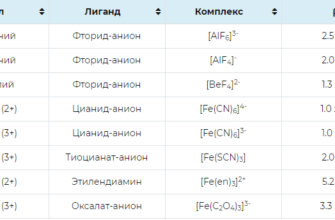
Константы устойчивости комплексных соединений.
124.4к.
Электрохимический ряд напряжений (активности) металлов —
015.2к.
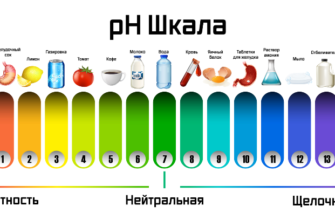
Полезные формулы для расчёта pH растворов электролитов
017.5к.
Таблица растворимости — это наглядная таблица со списком
016.7к.
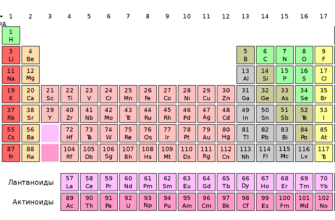
Длиннопериодная периодическая таблица (система) химических
09.7к.
Короткопериодная периодическая таблица (система) химических
010.4к.
Стандартные окислительно-восстановительные потенциалы
059.9к.
Таблица электроотрицательности химических элементов

4.6
Средняя оценка: 4.6
Всего получено оценок: 434.
4.6
Средняя оценка: 4.6
Всего получено оценок: 434.
Выяснить активность простых веществ можно с помощью таблицы электроотрицательности химических элементов. Обозначается как χ. Подробнее о понятии активности читайте в нашей статье.
Что такое электроотрицательность
Свойство атома химического элемента притягивать к себе электроны других атомов называется электроотрицательностью. Впервые понятие ввёл Лайнус Полинг в первой половине ХХ века.
Все активные простые вещества можно разделить на две группы в соответствии с физическими и химическими свойствами:
- металлы;
- неметаллы.
Все металлы являются восстановителями. В реакциях они отдают электроны и обладают положительной степенью окисления. Неметаллы могут проявлять свойства восстановителей и окислителей в зависимости от значения электроотрицательности. Чем выше электроотрицательность, тем сильнее свойства окислителя.
Полинг составил шкалу электроотрицательности. В соответствии со шкалой Полинга наибольшей электроотрицательностью обладает фтор (4), наименьшей – франций (0,7). Это значит, что фтор является самым сильным окислителем и способен притягивать электроны большинства элементов. Напротив, франций, как и другие металлы, является восстановителем. Он стремится отдать, а не принять электроны.
Электроотрицательность является одним из главных факторов, определяющих тип и свойства образованной между атомами химической связи.
Как определить
Свойства элементов притягивать или отдавать электроны можно определить по ряду электроотрицательности химических элементов. В соответствии со шкалой элементы со значением более двух являются окислителями и проявляют свойства типичного неметалла.
|
Номер элемента |
Элемент |
Символ |
Электроотрицательность |
|
87 |
Франций |
Fr |
0,79 |
|
55 |
Цезий |
Cs |
0,79 |
|
19 |
Калий |
K |
0,82 |
|
37 |
Рубидий |
Rb |
0,82 |
|
56 |
Барий |
Ba |
0,89 |
|
88 |
Радий |
Ra |
0,9 |
|
11 |
Натрий |
Na |
0,93 |
|
38 |
Стронций |
Sr |
0,95 |
|
3 |
Литий |
Li |
0,98 |
|
20 |
Кальций |
Ca |
1,0 |
|
57 |
Лантан |
La |
1,1 |
|
89 |
Актиний |
Ac |
1,1 |
|
70 |
Иттербий |
Yb |
1,1 |
|
58 |
Церий |
Ce |
1,12 |
|
59 |
Празеодим |
Pr |
1,13 |
|
61 |
Прометей |
Pm |
1,13 |
|
95 |
Америций |
Am |
1,13 |
|
60 |
Неодим |
Nd |
1,14 |
|
62 |
Самарий |
Sm |
1,17 |
|
64 |
Гадолиний |
Gd |
1,2 |
|
66 |
Диспрозий |
Dy |
1,22 |
|
39 |
Иттрий |
Y |
1,22 |
|
68 |
Эрбий |
Er |
1,24 |
|
69 |
Тулий |
Tm |
1,25 |
|
71 |
Лютеций |
Lu |
1,27 |
|
96 |
Кюрий |
Cm |
1,28 |
|
94 |
Плутоний |
Pu |
1,28 |
|
90 |
Торий |
Th |
1,3 |
|
97 |
Берклий |
Bk |
1,3 |
|
98 |
Калифорний |
Cf |
1,3 |
|
99 |
Эйнштейний |
Es |
1,3 |
|
100 |
Фермий |
Fm |
1,3 |
|
101 |
Менделевий |
Md |
1,3 |
|
102 |
Нобелий |
No |
1,3 |
|
12 |
Магний |
Mg |
1,31 |
|
40 |
Цирконий |
Zr |
1,33 |
|
93 |
Нептуний |
Np |
1,36 |
|
21 |
Скандий |
Sc |
1,36 |
|
92 |
Уран |
U |
1,38 |
|
73 |
Тантал |
Ta |
1,5 |
|
91 |
Протактиний |
Pa |
1,5 |
|
22 |
Титан |
Ti |
1,54 |
|
25 |
Марганец |
Mn |
1,55 |
|
4 |
Бериллий |
Be |
1,57 |
|
41 |
Ниобий |
Nb |
1,6 |
|
13 |
Алюминий |
Al |
1,61 |
|
81 |
Талий |
Tl |
1,62 |
|
30 |
Цинк |
Zn |
1,65 |
|
23 |
Ванадий |
V |
1,63 |
|
24 |
Хром |
Cr |
1,66 |
|
48 |
Кадмий |
Cd |
1,69 |
|
49 |
Индий |
In |
1,78 |
|
31 |
Галлий |
Ga |
1,81 |
|
26 |
Железо |
Fe |
1,83 |
|
82 |
Свинец |
Pb |
1,87 |
|
27 |
Кобальт |
Co |
1,88 |
|
29 |
Медь |
Cu |
1,9 |
|
75 |
Рений |
Re |
1,9 |
|
14 |
Кремний |
Si |
1,9 |
|
43 |
Технеций |
Tc |
1,9 |
|
28 |
Никель |
Ni |
1,91 |
|
47 |
Серебро |
Ag |
1,93 |
|
50 |
Олово |
Sn |
1,96 |
|
80 |
Ртуть |
Hg |
2 |
|
84 |
Полоний |
Po |
2 |
|
83 |
Висмут |
Bi |
2,02 |
|
5 |
Бор |
B |
2,04 |
|
51 |
Сурьма |
Sb |
2,05 |
|
42 |
Молибден |
Mo |
2,16 |
|
33 |
Мышьяк |
As |
2,18 |
|
15 |
Фосфор |
P |
2,19 |
|
1 |
Водород |
H |
2,2 |
|
77 |
Иридий |
Ir |
2,2 |
|
86 |
Радон |
Rn |
2,2 |
|
85 |
Астат |
At |
2,2 |
|
44 |
Рутений |
Ru |
2,2 |
|
46 |
Палладий |
Pd |
2,2 |
|
76 |
Осмий |
Os |
2,2 |
|
78 |
Платина |
Pt |
2,28 |
|
45 |
Родий |
Rh |
2,28 |
|
74 |
Вольфрам |
W |
2,36 |
|
79 |
Золото |
Au |
2,54 |
|
6 |
Углерод |
C |
2,55 |
|
34 |
Селен |
Se |
2,55 |
|
16 |
Сера |
S |
2,58 |
|
54 |
Ксенон |
Xe |
2,6 |
|
53 |
Йод |
I |
2,66 |
|
36 |
Криптон |
Kr |
2,96 |
|
7 |
Азот |
N |
3,04 |
|
17 |
Хлор |
Cl |
3,16 |
|
8 |
Кислород |
O |
3,44 |
|
9 |
Фтор |
F |
3,98 |
Вещества с электроотрицательностью два и меньше являются восстановителями и проявляют металлические свойства. Переходные металлы, обладающие переменной степенью окисления и относящиеся к побочным подгруппам таблицы Менделеева, имеют значения электроотрицательности в пределах 1,5-2. Ярко выраженными свойствами восстановителя обладают элементы с электроотрицательностью равной или меньше одного. Это типичные металлы.
В ряде электроотрицательности металлические и восстановительные свойства увеличиваются справа налево, а окислительные и неметаллические свойства – слева направо.
Помимо шкалы Полинга узнать, насколько выражены окислительные или восстановительные свойства элемента можно с помощью периодической таблицы Менделеева. Электроотрицательность увеличивается в периодах слева направо с увеличением порядкового номера. В группах значение электроотрицательности уменьшается сверху вниз.
Что мы узнали?
Электроотрицательность показывает способность элементов отдавать или принимать электроны. Эта характеристика помогает понять, насколько выражены свойства окислителя (неметалла) или восстановителя (металла) у конкретного элемента. Для удобства Полингом была разработана шкала электроотрицательности. Согласно шкале максимальными окислительными свойствами обладает фтор, минимальными – франций. В периодической таблице свойства металлов увеличиваются справа налево и сверху вниз.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Александр Котков
5/5
-
Александр Котков
5/5
-
Александр Котков
5/5
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 434.
А какая ваша оценка?
Таблица электроотрицательности химических элементов.
Электроотрицательность (χ) – фундаментальное химическое свойство атома, количественная характеристика способности атома в молекуле смещать к себе общие электронные пары, т.е. способность атомов притягивать к себе электроны других атомов.
На электроотрицательность атома химического элемента влияет как его атомный номер, так и расстояние, на котором находятся его валентные электроны от заряженного ядра. Чем выше связанная с этим электроотрицательность, тем больше атом притягивает электроны.
Обычно используют относительную электроотрицательность по шкале Полинга.
Таблица электроотрицательности химических элементов (1 часть):
| Атомный номер | Химический элемент | Символ | Электроотрицательность по шкале Полинга |
| 1 | Водород | H | 2,20 |
| 2 | Гелий | He | 4,5 |
| 3 | Литий | Li | 0,98 |
| 4 | Бериллий | Be | 1,57 |
| 5 | Бор | B | 2,04 |
| 6 | Углерод | C | 2,55 |
| 7 | Азот | N | 3,04 |
| 8 | Кислород | O | 3,44 |
| 9 | Фтор | F | 3,98 |
| 10 | Неон | Ne | 4,4 |
| 11 | Натрий | Na | 0,93 |
| 12 | Магний | Mg | 1,31 |
| 13 | Алюминий | Al | 1,61 |
| 14 | Кремний | Si | 1,90 |
| 15 | Фосфор | P | 2,19 |
| 16 | Сера | S | 2,58 |
| 17 | Хлор | Cl | 3,16 |
| 18 | Аргон | Ar | 4,3 |
| 19 | Калий | K | 0,82 |
| 20 | Кальций | Ca | 1,0 |
| 21 | Скандий | Sc | 1,36 |
| 22 | Титан | Ti | 1,54 |
| 23 | Ванадий | V | 1,63 |
| 24 | Хром | Cr | 1,66 |
| 25 | Марганец | Mn | 1,55 |
| 26 | Железо | Fe | 1,83 |
| 27 | Кобальт | Co | 1,88 |
| 28 | Никель | Ni | 1,91 |
| 29 | Медь | Cu | 1,90 |
| 30 | Цинк | Zn | 1,65 |
| 31 | Галлий | Ga | 1,81 |
| 32 | Германий | Ge | 2,01 |
| 33 | Мышьяк | As | 2,18 |
| 34 | Селен | Se | 2,55 |
| 35 | Бром | Br | 2,96 |
Таблица электроотрицательности химических элементов (2 часть):
| 36 | Криптон | Kr | 3,0 |
| 37 | Рубидий | Rb | 0,82 |
| 38 | Стронций | Sr | 0,95 |
| 39 | Иттрий | Y | 1,22 |
| 40 | Цирконий | Zr | 1,33 |
| 41 | Ниобий | Nb | 1,6 |
| 42 | Молибден | Mo | 2,16 |
| 43 | Технеций | Tc | 1,9 |
| 44 | Рутений | Ru | 2,2 |
| 45 | Родий | Rh | 2,28 |
| 46 | Палладий | Pd | 2,20 |
| 47 | Серебро | Ag | 1,93 |
| 48 | Кадмий | Cd | 1,69 |
| 49 | Индий | In | 1,78 |
| 50 | Олово | Sn | 1,96 |
| 51 | Сурьма | Sb | 2,05 |
| 52 | Теллур | Te | 2,1 |
| 53 | Йод | I | 2,66 |
| 54 | Ксенон | Xe | 2,6 |
| 55 | Цезий | Cs | 0,79 |
| 56 | Барий | Ba | 0,89 |
| 57 | Лантан | La | 1,10 |
| 58 | Церий | Ce | 1,12 |
| 59 | Празеодим | Pr | 1,13 |
| 60 | Неодим | Nd | 1,14 |
| 61 | Прометий | Pm | 1,1 |
| 62 | Самарий | Sm | 1,17 |
| 63 | Европий | Eu | 1,2 |
| 64 | Гадолиний | Gd | 1,20 |
| 65 | Тербий | Tb | 1,20 |
| 66 | Диспрозий | Dy | 1,22 |
| 67 | Гольмий | Ho | 1,23 |
| 68 | Эрбий | Er | 1,24 |
| 69 | Тулий | Tm | 1,25 |
| 70 | Иттербий | Yb | 1,1 |
Таблица электроотрицательности химических элементов (3 часть):
| 71 | Лютеций | Lu | 1,27 |
| 72 | Гафний | Hf | 1,3 |
| 73 | Тантал | Ta | 1,5 |
| 74 | Вольфрам | W | 2,3 |
| 75 | Рений | Re | 1,9 |
| 76 | Осмий | Os | 2,2 |
| 77 | Иридий | Ir | 2,2 |
| 78 | Платина | Pt | 2,28 |
| 79 | Золото | Au | 2,64 |
| 80 | Ртуть | Hg | 2,0 |
| 81 | Таллий | Tl | 1,62 |
| 82 | Свинец | Pb | 2,33 |
| 83 | Висмут | Bi | 2,02 |
| 84 | Полоний | Po | 2,0 |
| 85 | Астат | At | 2,2 |
| 86 | Радон | Rn | 2,2 |
| 87 | Франций | Fr | 0,7 |
| 88 | Радий | Ra | 0,9 |
| 89 | Актиний | Ac | 1,1 |
| 90 | Торий | Th | 1,3 |
| 91 | Протактиний | Pa | 1,5 |
| 92 | Уран | U | 1,38 |
| 93 | Нептуний | Np | 1,36 |
| 94 | Плутоний | Pu | 1,28 |
| 95 | Америций | Am | 1,3 |
| 96 | Кюрий | Cm | 1,3 |
| 97 | Берклий | Bk | 1,3 |
| 98 | Калифорний | Cf | 1,3 |
| 99 | Эйнштейний | Es | 1,3 |
| 100 | Фермий | Fm | 1,3 |
| 101 | Менделевий | Md | 1,3 |
| 102 | Нобелий | No | 1,3 |
| 103 | Лоуренсий | Lr | 1,3 |
| 104 | Резерфордий (Курчатовий) | Rf | |
| 105 | Дубний (Нильсборий) | Db | |
| 106 | Сиборгий | Sg | |
| 107 | Борий | Bh | |
| 108 | Хассий | Hs | |
| 109 | Мейтнерий | Mt | |
| 110 | Дармштадтий | Ds |
Коэффициент востребованности
18 452
Таблицы на ЕГЭ и ОГЭ по химии
На сдаче ЕГЭ и ОГЭ по химии можно использовать три таблицы:
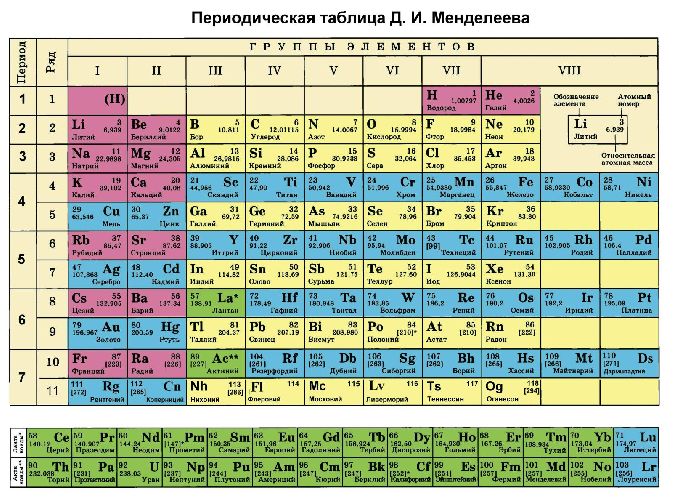
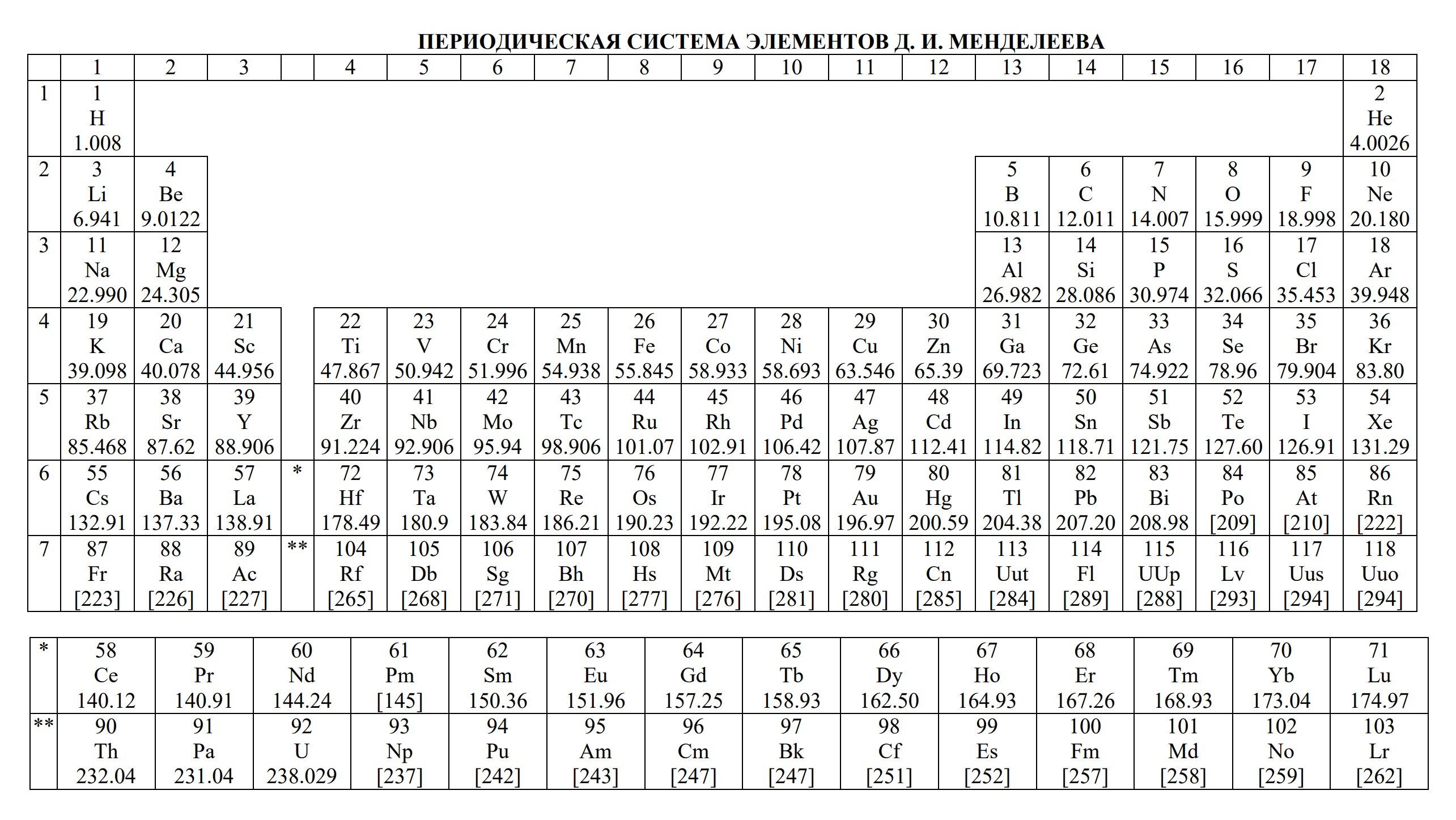
- периодическая система химических элементов Д.И. Менделеева
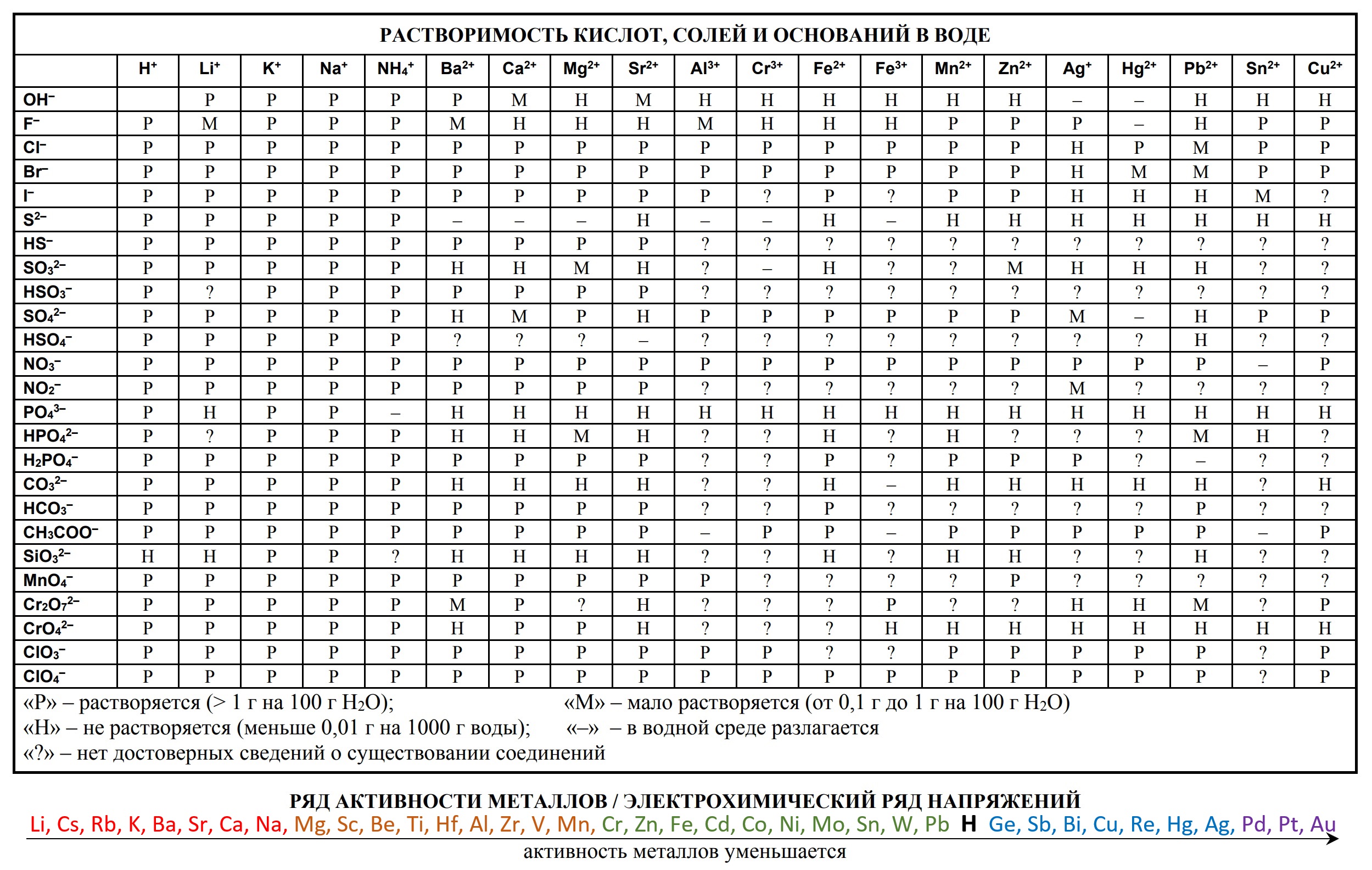
- таблица растворимости
- ряд активности металлов.
Они содержат в себе 80% информации, необходимой для решения большинства заданий.
Однако таблицы на форзацах разных учебников, продаваемые в книжных магазинах, располагающиеся на просторах интернета отличаются не только оформлением, но и содержанием. Что бы они оказались надёжно шпаргалкой, а не приятной неожиданностью, лучше с самого начала начинать работать с тем форматом, который официально разрешен на ЕГЭ твоего года.
Скачать эти таблицы можно ниже. А как сделать эти безликие таблицы наиболее информационными для тебя я расскажу на уроке.
- Таблица Д.И. Менделеева для ОГЭ и ЕГЭ
- Таблица растворимости и ряд активности для ОГЭ и ЕГЭ
- Таблица растворимости с расширенным рядом активности
- Таблица Д.И. Менделеева длиннопериодная для олимпиады
Относительная электроотрицательность химических элементов (Таблица)
Относительноя электроотрицательность химических элементов (классический вариант)
|
I |
II |
III b |
IV b |
V b |
VI b |
VII b |
VIII b |
VIII b |
VIII b |
I b |
II b |
III |
IV |
V |
VI |
VII |
VIII |
|
H 2,1 |
He |
||||||||||||||||
|
Li 0,97 |
Be 1,47 |
B 2,02 |
C 2,50 |
N 3,07 |
O 3,50 |
F 4,10 |
Ne |
||||||||||
|
Na 1,01 |
Mg 1,23 |
Al 1,47 |
Si 1,74 |
P 2,10 |
S 2,60 |
Cl 2,83 |
Ar |
||||||||||
|
K 0,91 |
Ca 1,04 |
Sc 1,20 |
Ti 1,32 |
V 1,45 |
Сr 1,56 |
Mn 1,60 |
Fe 1,64 |
Co 1,75 |
Ni 1,75 |
Cu 1,76 |
Zn 1,66 |
Ga 1,82 |
Ge 2,02 |
As 2,20 |
Se 2,48 |
Br 2,74 |
Kr 3,00 |
|
Rb 0,89 |
Sr 0,99 |
Y 1,11 |
Zr 1,22 |
Nb 1,23 |
Mo 1,30 |
Tc 1,36 |
Ru 1,42 |
Rh 1,45 |
Pd 1,35 |
Ag 1,42 |
Cd 1,46 |
In 1,49 |
Sn 1,72 |
Sb 1,82 |
Te 2,01 |
I 2,21 |
Xe 2,60 |
|
Cs 0,86 |
Ba 0,97 |
La 1,08 |
Hf 1,23 |
Ta 1,33 |
W 1,40 |
Re 1,46 |
Os 1,52 |
Ir 1,55 |
Pt 1,44 |
Au 1,42 |
Hg 1,44 |
Tl 1,44 |
Pb 1,55 |
Bi 1,67 |
Po 1,76 |
At 1,96 |
Rn 2,20 |
|
Fr 0,86 |
Ra 0,97 |
Ac 1,00 |
Лантаноиды имеют значения относительных электроотрицательностей в области 1,08 – 1,14;
Актиноиды имеют значения относительных электроотрицательностей в области 1,11 – 1,20;
Элементы VIII группы периодической системы (благородные газы) имеют нулевую электроотрицательность;
Условной границей между металлами и неметаллами считается значение относительно электроотрицательности равное 2
Относительная электроотрицательности химических элементов (таблица)
|
Элемент |
Электроотрицательность |
Элемент |
Электроотрицательность |
|
Ac |
1,00 |
F |
4,10 |
|
Ag |
1,42 |
Fe |
1,64 |
|
Al |
1,47 |
Fr |
0,86 |
|
Ar |
3,20 |
Ga |
1,82 |
|
As |
2,11 |
Ge |
2,02 |
|
At |
1,90 |
H |
2,10 |
|
Au |
1,42 |
He |
5,50 |
|
B |
2,01 |
Hf |
1,23 |
|
Ba |
0,97 |
Hg |
1,44 |
|
Be |
1,47 |
I |
2,21 |
|
Bi |
1,67 |
In |
1,49 |
|
Br |
2,74 |
Ir |
1,55 |
|
C |
2,50 |
K |
0,91 |
|
Ca |
1,04 |
Kr |
2,94 |
|
Cd |
1,46 |
La |
1,08 |
|
Cl |
2,83 |
Li |
0,97 |
|
Co |
1,70 |
Mg |
1,23 |
|
Cr |
1,56 |
Mn |
1,60 |
|
Cs |
0,86 |
Rn |
2,06 |
|
Cu |
1,75 |
Ru |
1,42 |
|
Mo |
1,30 |
S |
2,60 |
|
N |
3,07 |
Si |
2,25 |
|
Na |
0,93 |
Sb |
1,82 |
Электроотрицательность
Электроотрицательность — способность атома какого-либо химического элемента в соединении оттягивать на себя электроны связанных с ним атомов других химических элементов.
Электроотрицательность, как и прочие свойства атомов химических элементов, изменяется с увеличением порядкового номера элемента периодически:
График выше демонстрирует периодичность изменения электроотрицательности элементов главных подгрупп в зависимости от порядкового номера элемента.
При движении вниз по подгруппе таблицы Менделеева электроотрицательность химических элементов уменьшается, при движении вправо по периоду возрастает.
Электроотрицательность отражает неметалличность элементов: чем выше значение электроотрицательности, тем более у элемента выражены неметаллические свойства.
Степень окисления
Степень окисления – условный заряд атома химического элемента в соединении, рассчитанный исходя из предположения, что все связи в его молекуле ионные, т.е. все связывающие электронные пары смещены к атомам с большей электроотрицательностью.
Как рассчитать степень окисления элемента в соединении?
1) Степень окисления химических элементов в простых веществах всегда равна нулю.
2) Существуют элементы, проявляющие в сложных веществах постоянную степень окисления:
Элементы, проявляющие постоянную СО |
Значение постоянной СО этого элемента |
| Щелочные металлы, т.е. все металлы IA группы — Li, Na, K, Rb, Cs, Fr |
+1 |
| Все элементы II группы, кроме ртути: Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd |
+2 |
| Алюминий Al | +3 |
| Фтор F | -1 |
3) Существуют химические элементы, которые проявляют в подавляющем большинстве соединений постоянную степень окисления. К таким элементам относятся:
4) Алгебраическая сумма степеней окисления всех атомов в молекуле всегда равна нулю. Алгебраическая сумма степеней окисления всех атомов в ионе равна заряду иона.
5) Высшая (максимальная) степень окисления равна номеру группы. Исключения, которые не попадают под это правило, — элементы побочной подгруппы I группы, элементы побочной подгруппы VIII группы, а также кислород и фтор.
Химические элементы, номер группы которых не совпадает с их высшей степенью окисления (обязательные к запоминанию)
Химический элемент |
Номер группы |
Высшая степень окисления |
| Кислород | VI | +2 (в OF2) |
| Фтор | VII | 0 |
| Медь | I | +2 |
| Железо | VIII | +6 (например K2FeO4) |
6) Низшая степень окисления металлов всегда равна нулю, а низшая степень окисления неметаллов рассчитывается по формуле:
низшая степень окисления неметалла = №группы − 8
Отталкиваясь от представленных выше правил, можно установить степень окисления химического элемента в любом веществе.
Нахождение степеней окисления элементов в различных соединениях
Пример 1
Определите степени окисления всех элементов в серной кислоте.
Решение:
Запишем формулу серной кислоты:
Степень окисления водорода во всех сложных веществах +1 (кроме гидридов металлов).
Степень окисления кислорода во всех сложных веществах равна -2 (кроме пероксидов и фторида кислорода OF2). Расставим известные степени окисления:
Обозначим степень окисления серы как x:
Молекула серной кислоты, как и молекула любого вещества, в целом электронейтральна, т.к. сумма степеней окисления всех атомов в молекуле равна нулю. Схематически это можно изобразить следующим образом:
Т.е. мы получили следующее уравнение:
Решим его:
Таким образом, степень окисления серы в серной кислоте равна +6.
Пример 2
Определите степень окисления всех элементов в дихромате аммония.
Решение:
Запишем формулу дихромата аммония:
Как и в предыдущем случае, мы можем расставить степени окисления водорода и кислорода:
Однако мы видим, что неизвестны степени окисления сразу у двух химических элементов — азота и хрома. Поэтому найти степени окисления аналогично предыдущему примеру мы не можем (одно уравнение с двумя переменными не имеет единственного решения).
Обратим внимание на то, что указанное вещество относится к классу солей и, соответственно, имеет ионное строение. Тогда справедливо можно сказать, что в состав дихромата аммония входят катионы NH4+ (заряд данного катиона можно посмотреть в таблице растворимости). Следовательно, так как в формульной единице дихромата аммония два положительных однозарядных катиона NH4+ , заряд дихромат-иона равен -2, поскольку вещество в целом электронейтрально. Т.е. вещество образовано катионами NH4+ и анионами Cr2O72-.
Мы знаем степени окисления водорода и кислорода. Зная, что сумма степеней окисления атомов всех элементов в ионе равна заряду, и обозначив степени окисления азота и хрома как x и y соответственно, мы можем записать:
Т.е. мы получаем два независимых уравнения:
Решая которые, находим x и y:
Таким образом, в дихромате аммония степени окисления азота -3, водорода +1, хрома +6, а кислорода -2.
Как определять степени окисления элементов в органических веществах можно почитать здесь.
Валентность
Валентность — число химических связей, которые образует атом элемента в химическом соединении.
Валентность атомов обозначается римскими цифрами: I, II, III и т.д.
Валентные возможности атома зависят от количества:
1) неспаренных электронов
2) неподеленных электронных пар на орбиталях валентных уровней
3) пустых электронных орбиталей валентного уровня
Валентные возможности атома водорода
Изобразим электронно-графическую формулу атома водорода:
Было сказано, что на валентные возможности могут влиять три фактора — наличие неспаренных электронов, наличие неподеленных электронных пар на внешнем уровне, а также наличие вакантных (пустых) орбиталей внешнего уровня. Мы видим на внешнем (и единственном) энергетическом уровне один неспаренный электрон. Исходя из этого, водород может точно иметь валентность, равную I. Однако на первом энергетическом уровне есть только один подуровень — s, т.е. атом водорода на внешнем уровне не имеет как неподеленных электронных пар, так и пустых орбиталей.
Таким образом, единственная валентность, которую может проявлять атом водорода, равна I.
Валентные возможности атома углерода
Рассмотрим электронное строение атома углерода. В основном состоянии электронная конфигурация его внешнего уровня выглядит следующим образом:
Т.е. в основном состоянии на внешнем энергетическом уровне невозбужденного атома углерода находится 2 неспаренных электрона. В таком состоянии он может проявлять валентность, равную II. Однако атом углерода очень легко переходит в возбужденное состояние при сообщении ему энергии, и электронная конфигурация внешнего слоя в этом случае принимает вид:
Несмотря на то что на процесс возбуждения атома углерода тратится некоторое количество энергии, траты с избытком компенсируются при образовании четырех ковалентных связей. По этой причине валентность IV намного более характерна для атома углерода. Так, например, валентность IV углерод имеет в молекулах углекислого газа, угольной кислоты и абсолютно всех органических веществ.
Помимо неспаренных электронов и неподеленных электронных пар на валентные возможности также влияет наличие вакантных ( ) орбиталей валентного уровня. Наличие таких орбиталей на заполняемом уровне приводит к тому, что атом может выполнять роль акцептора электронной пары, т.е. образовывать дополнительные ковалентные связи по донорно-акцепторному механизму. Так, например, вопреки ожиданиям, в молекуле угарного газа CO связь не двойная, а тройная, что наглядно показано на следующей иллюстрации:
Резюмируя информацию по валентным возможностям атома углерода:
1) Для углерода возможны валентности II, III, IV
2) Наиболее распространенная валентность углерода в соединениях IV
3) В молекуле угарного газа CO связь тройная (!), при этом одна из трех связей образована по донорно-акцепторному механизму
Валентные возможности атома азота
Запишем электронно-графическую формулу внешнего энергетического уровня атома азота:
Как видно из иллюстрации выше, атом азота в своем обычном состоянии имеет 3 неспаренных электрона, в связи с чем логично предположить о его способности проявлять валентность, равную III. Действительно, валентность, равная трём, наблюдается в молекулах аммиака (NH3), азотистой кислоты (HNO2), треххлористого азота (NCl3) и т.д.
Выше было сказано, что валентность атома химического элемента зависит не только от количества неспаренных электронов, но также и от наличия неподеленных электронных пар. Связано это с тем, что ковалентная химическая связь может образоваться не только, когда два атома предоставляют друг другу по одному электрону, но также и тогда, когда один атом, имеющий неподеленную пару электронов — донор( ) предоставляет ее другому атому с вакантной (
) орбиталью валентного уровня (акцептору). Т.е. для атома азота возможна также валентность IV за счет дополнительной ковалентной связи, образованной по донорно-акцепторному механизму. Так, например, четыре ковалентных связи, одна из которых образована по донорно-акцепторному механизму, наблюдается при образовании катиона аммония:
Несмотря на то что одна из ковалентных связей образуется по донорно-акцепторному механизму, все связи N-H в катионе аммония абсолютно идентичны и ничем друг от друга не отличаются.
Валентность, равную V, атом азота проявлять не способен. Связано это с тем, что для атома азота невозможен переход в возбужденное состояние, при котором происходит распаривание двух электронов с переходом одного из них на свободную орбиталь, наиболее близкую по уровню энергии. Атом азота не имеет d-подуровня, а переход на 3s-орбиталь энергетически настолько затратен, что затраты энергии не покрываются образованием новых связей. Многие могут задаться вопросом, а какая же тогда валентность у азота, например, в молекулах азотной кислоты HNO3 или оксида азота N2O5? Как ни странно, валентность там тоже IV, что видно из нижеследующих структурных формул:
Пунктирной линией на иллюстрации изображена так называемая делокализованная π-связь. По этой причине концевые связи NO можно назвать «полуторными». Аналогичные полуторные связи имеются также в молекуле озона O3, бензола C6H6 и т.д.
em>Резюмируя информацию по валентным возможностям атома азота:
1) Для азота возможны валентности I, II, III и IV
2) Валентности V у азота не бывает!
3) В молекулах азотной кислоты и оксида азота N2O5 азот имеет валентность IV, а степень окисления +5 (!).
4) В соединениях, в которых атом азота четырехвалентен, одна из ковалентных связей образована по донорно-акцепторному механизму (соли аммония NH4+, азотная кислота и д.р).
Валентные возможности фосфора
Изобразим электронно-графическую формулу внешнего энергетического уровня атома фосфора:
Как мы видим, строение внешнего слоя у атома фосфора в основном состоянии и атома азота одинаково, в связи с чем логично ожидать для атома фосфора так же, как и для атома азота, возможных валентностей, равных I, II, III и IV, что и наблюдается на практике.
Однако в отличие от азота, атом фосфора имеет на внешнем энергетическом уровне еще и d-подуровень с 5-ю вакантными орбиталями.
В связи с этим он способен переходить в возбужденное состояние, распаривая электроны 3s-орбитали:
Таким образом, недоступная для азота валентность V для атома фосфора возможна. Так, например, валентность, равную пяти, атом фосфора имеет в молекулах таких соединений, как фосфорная кислота, галогениды фосфора (V), оксид фосфора (V) и т.д.
Валентные возможности атома кислорода
Электронно-графическая формула внешнего энергетического уровня атома кислорода имеет вид:
Мы видим на 2-м уровне два неспаренных электрона, в связи с чем для кислорода возможна валентность II. Следует отметить, что данная валентность атома кислорода наблюдается практически во всех соединениях. Выше при рассмотрении валентных возможностей атома углерода мы обсудили образование молекулы угарного газа. Связь в молекуле CO тройная, следовательно, кислород там трехвалентен (кислород — донор электронной пары).
Из-за того что атом кислорода не имеет на внешнем уровне d-подуровня, распаривание электронов s и p-орбиталей невозможно, из-за чего валентные возможности атома кислорода ограничены по сравнению с другими элементами его подгруппы, например, серой.
Таким образом, кислород практически всегда имеет валентность, равную II, однако в некоторых частицах он трехвалентен, в частности, в молекуле угарного газа C≡O. В случае, когда кислород имеет валентность III, одна из ковалентных связей образована по донорно-акцепторному механизму.
Валентные возможности атома серы
Внешний энергетический уровень атома серы в невозбужденном состоянии:
У атома серы, как и у атома кислорода, в обычном состоянии два неспаренных электрона, поэтому мы можем сделать вывод о том, что для серы возможна валентность, равная двум. И действительно, валентность II сера имеет, например, в молекуле сероводорода H2S.
Как мы видим, у атома серы на внешнем уровне появляется d-подуровень с вакантными орбиталями. По этой причине атом серы способен расширять свои валентные возможности в отличие от кислорода за счет перехода в возбужденные состояния. Так, при распаривании неподеленной электронной пары 3p-подуровня атом серы приобретает электронную конфигурацию внешнего уровня следующего вида:
В таком состоянии атом серы имеет 4 неспаренных электрона, что говорит нам о возможности проявления атомами серы валентности, равной IV. Действительно, валентность IV сера имеет в молекулах SO2, SF4, SOCl2 и т.д.
При распаривании второй неподеленной электронной пары, расположенной на 3s-подуровне, внешний энергетический уровень приобретает конфигурацию:
В таком состоянии уже становится возможным проявление валентности VI. Примером соединений с VI-валентной серой являются SO3, H2SO4, SO2Cl2 и т.д.
Аналогично можно рассмотреть валентные возможности остальных химических элементов.
Автор: С.И. Широкопояс https://scienceforyou.ru/