12 сентября 2022
В закладки
Обсудить
Жалоба
Памятка по органической химии
Таблица.
pm-h.doc
pm-h.pdf
Класс | Химические свойства | Способы получения
Алканы
Алкены
Алкины
Алкадиены
Арены
Предельные одноатомные спирты
Многоатомные спирты
Альдегиды
Предельные одноосновные карбоновые кислоты
Моносахариды
Дисахариды
Полисахариды
Амины
Аминокислоты
Белки
Автор: Столярова В.А.
Таблицы качественных реакций
21-Дек-2013 | комментариев 9 | Лолита Окольнова
Вопросы части С объединяют знание всех тем химии. В случае Задания С2 ЕГЭ по химии — знание всех классов неорганических веществ и их качественных реакции.
Дается конкретный химический эксперимент, ход которого нужно описать химическими реакциями.
Для таких реакции обычно предлагаются какие-то внешние проявления — выделения газа, выпадение осадка или изменение окраски раствора.
Таблица качественных реакций для газов
| Описание | Формула |
Реакции |
| Бурый газ |
NO2 |
1) N2 + 2O2 = 2NO2 2) взаимодействие металлов с азотной кислотой (концентрированной) 3) разложение нитратов |
| Запах тухлых яиц |
H2S |
Взаимодействие активных металлов с концентрированной серной кислотой: |
|
Газ с резким запахом. Растворимый в воде |
SO2 |
1) взаимодействие серасодежащих веществ с кислородом
2) взаимодействие некоторых металлов с концентрированной серной кислотой |
| Газ с резким характерным запахом, растворимый в воде |
NH3 |
1) N2 + 3H2 = 2NH3 2) обменные реакции солей аммония |
| Газ, не поддерживающий горение, малорастворимый в воде, не ядовитый |
N2 |
1) горение азотсодержащих веществ; NH4NO2 = N2 + 2H2O |
|
Газы, поддерживающие горение: (для NO2 – бурый цвет) |
O2 O3 NO2 |
3C + 2O3 = 3CO2 С + 2NO2 = CO2 + 2NO |
Таблица качественных реакций для щелочных металлов:
Т.к. все соединения щелочных металлов хорошо растворимы в воде, то их определяют по цвету пламени:
(указан так же цвет пламени некоторых щелочно-земельных металлов)
|
желто-зеленое |
фиолетовое |
кирпично-красное |
ярко-красное |
желтое |
карминово-красное |
|
Ba2+ |
K+ |
Са2+ |
Li+ |
Na+ |
Sr2+ |
Таблица качественных реакций
— цвета осадков
|
Осадки белого цвета |
Качественная реакция |
|
Белый творожистый нерастворимый в воде; нерастворимый в HNO3 |
Ag+ + Cl— → AgCl↓ качественная реакция на соли серебра; качественная реакция на хлорид-ионы; |
|
Белый осадок нерастворимый в кислотах |
Ba2+ + SO4 -2 → BaSO4↓ качественная реакция на соли бария; качественная реакция на сульфат-ионы; |
|
Белый осадок образуется при пропускании газа без цвета с резким запахом через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах |
Сa(OH)2 + SO2 = CaSO3↓ + H2O
|
|
Белый осадок образуется при добавлении щелочи; растворяется в избытке щелочи |
Al3+ + 3OH— = Al(OH)3↓ Zn2+ + 2OH— = Zn(OH)2↓
|
|
Белый осадок образуется при пропускании газа без цвета и запаха через известковую воду; растворяется при пропускании избытка газа; растворяется в кислотах |
Сa(OH)2 + CO2 = CaCO3↓ + H2O
CaCO3 + 2H+ → CO2↑ + H2O + Ca2+ |
|
Осадок светло-желтого цвета (осадок кремового цвета) образуется при приливании AgNO3; нерастворим в HNO3; |
Ag+ + Br— → AgBr↓ качественная реакция на бромид-ионы; (качественная реакция на соли серебра); |
|
Осадок желтого цвета образуется при приливании AgNO3; нерастворим в HNO3; |
Ag+ + I— → AgJ↓ качественная реакция на иодид-ионы; (качественная реакция на соли серебра); |
|
Осадок желтого цвета образуется при приливании AgNO3; растворим в кислотах; |
3Ag+ + PO43- → Ag3PO4↓ |
|
Осадки коричневых цветов |
Качественная реакция |
|
Осадок бурого цвета образуется при взаимодействии с растворами щелочей; |
Fe3+ +3OH— → Fe(OH)3↓ качественная реакция на соли железа |
|
Осадки синих и зеленых цветов |
Качественная реакция |
|
Осадки зеленого цвета |
Fe2+ +2OH— → Fe(OH)2↓ |
|
Осадок голубого цвета (осадок синего цвета) образуется при взаимодействии с растворами щелочей |
Cu2+ +2OH— → Cu(OH)2↓ качественная реакция на соли меди (II) |
|
Осадок синего цвета образуется при взаимодействии с раствором красной кровяной и желтой кровяной соли |
3Fe2+ + 2[Fe(CN)6]3- → Fe3[Fe(CN)6]2↓ качественная реакция на соли железа (II) — с красной кровяной солью; 4Fe3+ + 3[Fe(CN)6]-4 → Fe4[Fe(CN)6]3↓ качественная реакция на соли железа (III) — с желтой кровяной солью; |
|
Осадки черного цвета |
Качественная реакция |
|
Осадок черного цвета Образуется при взаимодействии с сульфидами или с H2S |
Fe2+ + S2- → FeS↓ Ni2+ + S2- → NiS↓ Cu2+ + S2- → CuS↓ Pb2+ + S2- → PbS↓ Hg2+ + S2- → HgS↓ Ag+ + S2- → Ag2S↓ качественная реакция на сульфид-ионы |
Обсуждение: «Таблицы качественных реакций»
(Правила комментирования)
1.4.1. Классификация химических реакций в неорганической и органической химии.
Классификация химических реакций на основании их признаков.
Классификационный признак |
Тип реакции |
Число и состав реагентов и продуктов |
соединенияв результате таких реакций из двух или более исходных веществ образуется только один продукт, например: С + O2 = CO2 4NO2 + O2 + 2H2O = 4HNO3 |
разложенияв таких реакциях из одного вещества образуется два или больше других веществ: 2KMnO4 = K2MnO4 + MnO2 + O2 CaCO3 = CaO + CO2 |
|
замещенияВсе реакции, в результате которых из простого и сложного веществ образуется другое простое и другое сложное вещества. Например: Zn + CuSO4 = ZnSO4 + Cu
|
|
обменаРеакциями обмена называют такие реакции, в результате которых вещества меняются своими составными частями. Например: 2NaOH + CuCl2 = 2NaCl + Cu(OH)2 Частный случай реакции обмена между кислотой и основанием носит также название реакции нейтрализации: NaOH + HCl = NaCl + H2O
|
|
Изменение степеней окисления химических элементов |
окислительно-восстановительныев результате таких реакций изменяются степени окисления одного или более химических элемента. Например: |
Реакции, протекающие с сохранением степеней окисления атомов всех химических элементов |
|
Обратимость |
обратимыетакие реакции обладают способностью протекать как в прямом, так и обратном направлении. Реакции, про которые обязательно нужно знать, что они обратимые: |
необратимыеТакие реакции протекают только в прямом направлении. Если речь идет о реакциях между электролитами, то необратимой реакция является в том случае, если образуется осадок, газ или малодиссоциирующее вещество. Например: Na2CO3 + 2HCl = 2NaCl + H2O + CO2 В качестве малодиссоциирующих веществ в реакциях ионного обмена могут образоваться вода, слабые кислоты, гидроксид аммония. |
|
Тепловой эффект |
экзотермическиеВ результате таких реакций выделяется энергия в виде теплоты. Обозначают такие реакции, добавляя «+Q» к уравнению реакции, например: |
эндотермическиеПри протекании таких реакций поглощается тепло. Для обозначения таких реакций пишут «-Q» в уравнении реакции. Практически все реакции разложения являются эндотермическими: Исключения: реакции разложения HI и NO являются экзотермическими. |
|
Количество фаз |
гомогенныеГомогенными реакциями называют такие реакции, реагенты в которых находятся в одной фазе. Примерами таких реакций могут быть многие реакции протекающие в растворах, реакции между газообразными веществами: NaOH (р-р) + HCl(р-р) = NaCl + H2O 2CO + O2 = 2CO2 В гомогенных реакциях не наблюдаются границы раздела между реагентами |
гетерогенныегетерогенными реакциями называют такие реакции, в которых реагирующие вещества находятся в разных фазах. Примерами таких реакций являются, взаимодействие цинка с раствором соляной кислоты, взаимодействие углекислого газа с известковой водой, и т.д.: |
|
По участию катализатора |
каталитическиереакции, протекающие в присутствии катализатора:
|
некаталитическиереакции, протекающие без катализатора: |
Классификация химических реакций в органической химии:
Реакции присоединения |
В зависимости от того, какое соединение присоединяется органическим веществом различают:
Гидрирование — присоединение водорода:Гидратация — присоединение воды:Гидрогалогенирование — присоединение галогеноводорода:
|
Реакции замещения |
Под реакциями замещения в органической химии подразумевают такие реакции, в результате протекания которых происходит замена одного заместителя (или атома водорода) непосредственно прикрепленного к углеродному скелету на другой заместитель. Так, например, реакциями замещения являются: Галогенирование алканов:Нитрование углеводородов:Реакция спиртов с галогеноводородными кислотами:C2H5OH + HBr = C2H5Br + H2O и т.д. |
Реакции отщепления (элиминирования) |
Все реакции, в названии которых присутствует приставка «де-«: дегидрирование:дегидратация:дегидрогалогенирование:(от исходной молекулы бромэтана отщепляется бромоводород, который нейтрализуется щелочью) дегалогенирование:Также к реакциям отщепления (элиминирования) относят крекинг — процесс термического превращения углеводородов в соединения с меньшей длинной углеродного скелета. Например, крекинг алканов, уравнение которого в общем виде можно записать как: |
Окислительно-восстановительные реакции |
Реакции, при которых изменяется степень окисления одного или нескольких атомов углерода углеродного скелета. Окисление органического соединенияВ таких реакциях отдельные атомы углерода повышают свою степень окисления. Например: Восстановление органического соединенияЧаще всего под восстановлением органических веществ понимают их взаимодействие с водородом. Например: CH3-CH=O + H2 => CH3-CH2-OH |
Реакции с сохранением качественного и количественного состава веществ |
Изомеризация |
Реакции протекающие по тем или иным механизмам |
Реакции протекающие по ионному механизмуВ таких реакциях активными действующими частицами являются ионы. Следует помнить, что по ионному механизму протекают такие реакции как:
|
Реакции протекающие по радикальному механизмуВ таких реакциях активными действующими частицами являются свободные радикалы:
|
Муниципальное автономное общеобразовательное учреждение
средняя общеобразовательная школа №9
Таблицы и схемы по химии
при подготовке к ЕГЭ.
учитель химии МАОУ СОШ №9
Моргунов Н.М.
ст. Темиргоевская 2018г.
Используемая литература:
-
Н.Е.Кузьменко, В.В.Ерёмин, В.А.Попков «Начала химии». Со-временный курс для поступающих в ВУЗы. – М.: «Экзамен», 2001г.
-
А.И.Артёменко «Органическая химия». Учебник для строит. спец. вузов. – М.: «Высшая школа», 1994г.
-
А.С.Егоров, Г.Х.Аминова «Экспресс-курс неорганической и органической химии. Для поступающих в ВУЗы.» — Ростов-на-Дону: «Феникс», 2002г.
-
А.С.Егоров «Химия в 400-х вопросах и ответах». (Пособие для учащихся и абитуриентов). Ростов-на-Дону: «Феникс», 2001 г.
-
А.С.Егоров «Как сдать ЕГЭ по химии на 100 баллов». – Ростов-на-Дону: «Феникс», 2003г.
-
И.А.Фрейфельд «Общая химия». Пособие для абитуриентов и старшеклассников. М.: «Московский лицей», 1996г.
-
И.И.Новошинский, Н.С.Новошинская «Переходные элементы и их соединения». Пособие для старшеклассников и абитуриентов. – Краснодар: «Советская Кубань», 2006г.
-
И.И.Новошинский, Н.С.Новошинская «Органическая химия 11 класс». Учебник для общеобразовательных учреждений. – М.: «Образование», 2005г.
-
И.И.Новошинский, Н.С.Новошинская «Химия. 10 класс». Учебник для общеобразовательных учреждений. – М.: «Оникс» «Мир и Образование», 2006г.
Тепловой эффект растворения веществ:
газы CO2
кислоты H2SO4
щёлочи NaOH
соли:
CuSO4
FeSO4
ZnSO4
Na2SO4
Na2CO3
AlCl3
AgNO3
NaCl
NaNO3
KNO2
NH4NO3
CuSO4 . 5H2O FeSO4 . 7H2O } купоросы
ZnSO4 . 7H2O
Na2SO4 . 10H2O кристаллическая сода
Na2СO3 . 10H2O Глауберова соль
AlCl3. 6H2O
Тепловой эффект химических реакций:
экзотермические (+Q)
эндотермические (-Q)
а) соединения искл. N2 + O2 = 2NO — Q
б) нейтрализации
в) замещения
г) овр
а) разложения
искл. 2H2O2 = 2H2O + O2 + Q
(NH4)2Cr2O7 = Cr2O3 + N2 +4H2O + Q
б) гидролиз
Механизмы органических реакций:
радикальный
( hv, t, H2O2 )
ионный
1) Замещение:
а) предельных у/в
hv
CH4 + Cl2 → CH3Cl + HCl
б) непредельных у/в ( у α-атома) – р-ция Львова.
hv
CH2=CH-CH3 + Cl2 → CH2=CH-CH3 + HCl
в) ароматических у/в ( в боковой цепи)
t, hv
С6Н5-СН2-СН3 + Cl2 → C6H5—CHCl—CH3 + HCl
2) Присоединение : a) непредельных у/в против правила Марковникова:
H2 O 2
CH3 –CH =CH2 + HCl → CH3-CH2-CH2Cl
б) ароматических у/в
hv
C6H6 + Cl2 → C6H6Cl6
3) Полимеризация:
n СН2=СН2 → (-СН2-СН2— )n
4) Горение, окисление:
t
CH4 + 2O2 → CO2 + 2H2O
1) Замещение в бензольном кольце:
FeCl3 , t
С6Н6 + Cl2 → C6H5Cl + HCl
H2SO4k, t
C6H6 + HNO3 → C6H5-NO2 + H2O
2) Присоединение непредельных у/в ( кроме гидрирования):
CH3-CH=CH2 + HCl → CH3-CHCl-CH3
3) Полимеризация ( в присутствии катализатора)
O2
n CH2=CH2 → (-CH2-CH2)n
H2SO4
n CH2=C-CH=CH2 → (-CH2-C=CH-CH2-)n
| |
CH3 CH3
Периодический закон и периодическая система.
№ периода = числу электронных слоёв
№ группы = числу (внешних) валентных электронов (для главных подгрупп)

электроотрицательность радиус атомов ув.
ув.
Fr

неметаллические и металлические и
окислительные свойства восстановительные свойства
ув.
ув.
Fr

HClO4 – самая сильная кислородсодержащая кислота
FrOH HI – самая сильная бескислородная кислота
самое сильное основание
внешние

валентные внешние S и предвнешние d ( кроме Zn, Cd, Hg ) d — элементы
э

Химическое равновесие.
υ прям.= υ обратн. ( при данных условиях )
υ пр [HI]2
H

ющих веществ )

C
[CO2]
Факторы смещения хим. равновесия ( принцип Ле-Шателье) :
1) Изменение концентрации ( кроме тв. веществ) : ув. исх.
ув. продукты
2) Изменение температуры : ув. t — Q


ум. Р ув. Р

2 моль 2 моль
Катализатор на смещение равновесия не влияет.
Смещение равновесия при диссоциации:
разбавление , связывание одного из ионов → (н: NaOH )
C
← ув. концентрации, введение одноимённых ионов (н: CH3COONa, HCl)
Смещение равновесия гидролиза:
Разбавление, нагревание, связывание одного из ионов → ( н: NH4Cl => H+ )
N
C
← ув. концентрации, охлаждение, введение одноимённых ионов (н: K2S => OH— )
Скорость химической реакции.
нет поверхности раздела гомогенные υ = +_ Δν / v . Δτ

υср. = +_ Δ С / Δ τ ; [ моль/ л . сек ]
Реакции –

т + ж, т + г, т + т гетерогенные υ = +_ Δ ν / s . Δτ
Факторы, влияющие на скорость:
1) Концентрация : чем > С , тем > υ
ув.Р ( для газов) ум. V
N2 + 3H2 = 2NH3υ = k [ N2 ] . [ H2 ] 3 — кинетическое уравнение закона действующих масс
4Al (тв.)+ 3O2(г) = 2Al2O3υ = k [ O2 ] 3 — твёрдые не входят ( для гетерогенных реакций)
Fe порошок + CuSO4 10% > Fe порошок + CuSO4 4% > Fe гвоздь + CuSO4 4%
2) Температура: при повышении t на каждые 100υ ув. в 2-4 раза ( правило Вант-Гоффа ) , т.к.
ув. число активных частиц (способных преодолеть Еакт. )
t2 — t 1

υ t2 = γ

3) Природа реагирующих веществ:
а) υ в-в с ионной и полярной ков. связью > υ в-в с неполярной или малополярной связью
н/о Zn + HCl = > органические Zn + CH3COOH =
б) активность металлов Mg + HCl > Fe + HCl неметаллов F2 + H2 > I2 + H2
K + H2O > Li + H2O (взрыв)
4) Площадь поверхности (для твёрдых в-в) : чем > S поверн. , тем > υ
Al порошок горит, Al ложка нет

— ↑
NO(г)

гетерогенный (в разных) N2 (Г) + 3H2 (Г) = 2NH3

В
промоторы
Разрушение комплексных солей и солей анионного типа:
1) Na2[ Zn(OH)4 ] + 2HCl нед. = Zn(OH)2 ↓ + 2NaCl + 2H2O
Na2[ Zn(OH)4 ] + 4HCl изб. = 2ZnCl2 +2NaCl + 4H2O
2) Na3[ Al(OH)6 ] + 3H2CO3 = Al(OH)3↓ + 3NaHCO3 + 3H2O
Na3[ Al(OH)6 ] + 3H2S = Al(OH)3↓ + 3NaHS + 3H2O
3) Na[ Al(OH)4 ] + CO2 = Al(OH)3 ↓ + NaHCO3
Na3[ Cr(OH)6 ] + 3SO2 = Cr(OH)3↓ + 3NaHSO3
4) Na3[ Cr(OH)6 ] + FeCl3 = Cr(OH)3↓ + Fe(OH)3 + 3NaCl
3Na[Al(OH)4 ] + AlCl3 = 4Al(OH)3↓ + 3NaCl
5) 2Na3[ Cr(OH)6 ] + 3H2O2 = 2Na2CrO4 + 2NaOH + 8H2O
t
6) Na[ Al(OH)4 ] = NaAlO2 + 2H2O
t
Na2[ Zn(OH)4 ] = ZnO + H2O + NaOH
7) 2Na[ Cr(OH)4 ] + 3Br2 + 8NaOH = 2Na2CrO4 + 6NaBr + 8H2O
Na2ZnO2 + 2HCl нед.= Zn(OH)2↓ + 2NaCl
Na2ZnO2 + 4HCl изб.= ZnCl2 + 2NaCl + 2H2O
NaAlO2 + HCl нед.+ H2O = Al(OH)3↓ + NaCl
NaAlO2 + 4HCl изб.= AlCl3 + NaCl + 2H2O
Образование комплексных солей и солей анионного типа:
а) в растворах:
1) NaOH + Al(OH)3 = Na[ Al(OH)4 ] или 3NaOH + Al(OH)3 = Na3[ Al(OH)6 ]
OH— + Al(OH)3 = [ Al(OH)4 ] — 3OH— + Al(OH)3 = [ Al(OH)6 ]3-
2) 2NaOH + Al2O3 + 3H2O = 2Na[ Al(OH)4 ] — тетрагидроксоалюминат
3) 2NaOH + 2Al + 6H2O = 2Na[ Al(OH)4 ] + 3H2↑
4) 4NaOH + AlCl3 = Na[ Al(OH)4 ] + 3NaCl
Na[ Cr(OH)4 ] ; Na3[ Cr(OH)6 ] ; Na[ Fe(OH)4 ] ; Na3[ Fe(OH)6 ]
тетрагидроксохромат гексагидроксохромат тетрагидроксоферрат гексагидроксоферрат
1) 2NaOH + Zn(OH)2 = Na2[ Zn(OH)4 ] — тетрагидроксоцинкат
2OH— + Zn(OH)2 = [ Zn(OH)4 ]2-
2) 2NaOH + ZnO + H2O = Na2[ Zn(OH)4 ]
3) 2NaOH + Zn + 2H2O = Na2[ Zn(OH)4 ] + H2↑
4) 4NaOH + ZnCl2 = Na2[ Zn(OH)4 ] + 2NaCl
Na2[ Be(OH)4 ] ; Na2[ Sn(OH)4 ] ; Na2[ Pb(OH)4 ]
тетрагидроксобериллат тетрагидроксостаннит тетрагидроксоплюмбит
t t
слабоамфотерные : Fe(OH)3 + NaOHконц = Na[ Fe(OH)4 ] ; Cu(OH)2 + 2NaOHконц >40% = Na2[ Cu(OH)4 ]
б) в расплавах:
Zn(OH)2 <=> H2ZnO2 ; Al(OH)3 <=> H3AlO3 – ортоалюминиевая кислота
HAlO2 – метаалюминиевая кислота
t
2NaOH + Zn(OH)2 = Na2ZnO2 + H2O
цинкат
tt
NaOH + Al(OH)3 = NaAlO2 + 2H2O 3NaOH + Al(OH)3 = Na3AlO3 + 3H2O
метаалюминат ортоалюминат
Na2BeO2 ; Na2SnO2 ; Na2PbO2 ; Na2CuO2
бериллат станнит плюмбит купрат (II)
NaCrO2 ; NaFeO2 ; Na2FeO4
метахромат феррат (III ) феррат ( VI )
Именные реакции:
t
1) Коновалова (нитрование): CH4 + HO—NO2 разб → CH3—NO2 + H2O
t
2) Вюрца: CH3-Br + 2Na + Br-CH3 → CH3-CH3 + 2NaBr
Cl CH3


эфир t
4) Гриньяра: CH3Cl + Mg → CH3-Mg-Cl ; CH3-Mg-Cl + Cl-CH2-CH3 → CH3-CH2-CH3 + MgCl2
t
5) Дюма (декарбоксилирование): CH3-COONa + NaOH → CH4 + Na2CO3
KMnO4
6) Вагнера: CH2=CH2 + [O] + H2O → CH2-CH2
| |
OH OH
3CH2=CH2 + 2KMnO4 + 4H2O → 3 CH2-CH2 + 2MnO2↓ + 2KOH
| |
OH OH

7) Лебедева: 2C2H5OH t CH2=CH-CH=CH2 + 2H2O + H2↑
t, Cr2O3, Al2O3




H





или C6H5NO2 + 3(NH4)2S + 7HCl → [C6H5NH3]Cl + 3S + 6NH4Cl + 2H2O
H+, t
13) Кирхгофа: (C6H10O5)n + nH2O → nC6H12O6
14) Кольбе (электролиз р-ра солей карбоновых кислот):
эл. ток
2CH3COONa + 2H2O → H2↑ + 2NaOH + CH3-CH3↑ + 2CO2↑
(K) (A)
hv α
15) Львова: CH3-CH=CH2 + Cl2 → Cl-CH2-CH=CH2 + HCl
|
Химическая связь и типы кристаллических решёток. |
|||
|
К |
н (одинаковые) . неМе – неМе полярная (разные) |
||
|
Атомная B, C (алмаз, графит), Si, Ge, As, Se,Te (SiO2-кварц, SiC-карбид). Молекулярная N2 . P4 . O2 , S8, H2 , F2 , Cl2, Br2 , I2 , благородные газы (искл. Rn), CO2 –«сухой лёд», NH3 ,H2 O, C6 H6 и т.д. |
Очень твёрдые, тугоплавкие, нераство-римые, не проводят ток и тепло (искл. Si и Ge – п/п). |
||
|
Малая твёрдость, летучие, низкая Тпл. и кип., многие не растворимы и не про-водят ток. |
|||
|
Ионная |
Ме – неМЕ |
Ионная NaCl, Li2 SO4 , KOH, Na 2 O, [CH3 –NH3] Cl |
Твёрдые, хрупкие, тугоплавкие, тепло-стойкие, растворы и расплавы прово-дят ток. |
|
Металлическая |
Ме |
Металлическая Fe, Cu и т.п. |
Ковкие, пластичные, с металлическим блеском, проводят ток и тепло. |
|
Водородная (между молекулами) |
H…(O,N,F) в разных молекулах |
между молекулами (H2 O)n , (HF)n H – O … H – O … ; H – F … H – F … H H |
ДНК внутримолекулярная |
|
Донорно- акцепторная (ковалентная связь) |
+ + _ NH4 , H3O , BF4 и комплексные соединения O3, CO |
H H H:N: + __ H+ → [ H—N—H ]+ ; H:O: + __ H → [ H:O:H ]+ H H H H B= IV B= III Na2 [ Zn(OH)4 ] |
F F F:B: __ + :F: → [F:B:F ]— F F |
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
- Соединения
- Разложения
- Замещения
- Обмена
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно
сложное вещество. Примеры:
4Na + O2 = 2Na2O
P2O5 + 3H2O = 2H3PO4
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
2KMnO4 = K2MnO4 + MnO2 + 2O2
Сa(OH)2 = CaO + H2O
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
CuSO4 + Fe = FeSO4 + Cu
2KI + Cl2 = 2KCl + I2
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами.
Часто обмен происходит анионами/катионами:
2KOH + MgCl2 = Mg(OH)2↓ + 2KCl
AgF + NaCl = AgCl↓ + NaF
Реакция нейтрализации — реакция обмена между основанием и кислотой, в ходе которой получаются соль и вода:
KOH + H2SO4 = K2SO4 + H2O

Окислительно-восстановительные реакции (ОВР)
Это те химические реакции, в процессе которых происходит изменение степеней окисления химических элементов, входящих в состав
исходных веществ. ОВР подразделяются на:
- Межмолекулярные — атомы окислителя и восстановителя входят в состав разных молекул. Примеры:
- Внутримолекулярные — атомы окислителя и восстановителя в составе одного сложного вещества. Примеры:
- Диспропорционирование — один и тот же атом является и окислителем, и восстановителем
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
K2SO3 + K2Cr2O7 + H2SO4 → K2SO4
+ Cr2(SO4)3 + H2O
KMnO4 → K2MnO4 + MnO2 + O2
KClO3 → KCl + O2
KOH + Cl2 → (t) KCl + KClO3 + H2O
KOH + Cl2 → KCl + KClO + H2O

Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО,
принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
От обилия информации можно запутаться. Я рекомендую сформулировать четко: «Окислитель — понижает СО, восстановитель — повышает СО». Запомнив
эту информацию таким образом, вы не будете путаться.

ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Обратимые реакции — такие химические реакции, которые протекают одновременно в двух противоположных направлениях: прямом и обратном.
При записи реакции в таких случаях вместо знака «=» ставят знак обратимости «⇆».
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
N2 + 3H2 ⇆ 2NH3
CH3COOH + C2H5OH ⇆ CH3COOC2H5 + H2O
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от
обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Иногда сложно бывает отличить обратимую реакцию от необратимой, однако я дам несколько советов, которые советую взять на вооружение.
В результате необратимых реакций:
- Образуются малодиссоциирующие вещества (например — вода, однако есть исключения — реакция этерификации)
- Реакция сопровождается выделение большого количества тепла
- В ходе реакции образуется газ или выпадает осадок
Примеры необратимых реакций:
BaCl2 + H2SO4 = BaSO4↓ + 2HCl (выпадает осадок)
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)

Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому
составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой,
твердой и газообразной.
Все реакции можно разделить на гетеро- и гомогенные. Гетерогенные реакции (греч. heterogenes — разнородный) — реакции, протекающие на
границе раздела фаз, в неоднородной среде. Скорость таких реакций зависит от площади соприкосновения реагирующих веществ.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество,
твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
Zn(тв.) + 2HCl(р-р.) = ZnCl2(р-р.) + H2(газ.)↑

Гомогенные реакции (греч. homogenes — однородный) — реакции, протекающие между веществами, находящимися в одной фазе.
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером
такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
NaOH(р-р.) + CH3COOH(р-р.) = CH3COONa(р-р.) + H2O(р-р.)

Реакции и их тепловой эффект
Все реакции можно разделить на те, в ходе которых тепло поглощается, или, наоборот, тепло выделяется. Представьте пробирку, охлаждающуюся
или нагревающуюся в вашей руке — это и есть тот самый тепловой эффект. Иногда тепла выделяется так много, что реакции сопровождаются
воспламенением или взрывом (натрий с водой).
- Экзотермические реакции
- Эндотермические реакции
Экзотермические реакции (греч. exo — вне) — химические реакции, сопровождающиеся потерей энергии системой и выделением тепла (той самой
энергии) во внешнюю среду. При написании химических реакций в конце экзотермических ставят «+ Q» (Q — тепло), иногда бывает указано точное
количество выделяющегося тепла. Например:
2Mg + O2 = 2MgO + Q
Большинство реакций нейтрализации относятся к экзотермическим:
NaOH + HCl = NaCl + H2O + 56 кДж

К экзотермическим реакциям часто относятся реакции горения, соединения.
4NH3 + 5O2 = 4NO + 6H2O + Q
Исключением является взаимодействие азота и кислорода, при
котором тепло поглощается:
N2 + O2 ⇄ 2NO — Q
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому
не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания»
в реакции вместо явного +Q при экзотермической реакции могут написать ΔH < 0. Например:
2Na + 2H2O = 2NaOH + H2; ΔH < 0 (это значит, что тепло выделяется — реакция экзотермическая)

Эндотермические реакции (греч. ἔνδον — внутри) — химические реакции, сопровождающиеся поглощением тепла, в результате которых образуются
вещества с более высоким энергетическим уровнем (их внутренняя энергия увеличивается).
К таким реакциям наиболее часто относятся реакции разложения. При написании эндотермических реакций в конце ставят «-Q», либо указывают точное
количество поглощенной энергии. Примеры таких реакций:
2HgO = Hg + O2 — Q
CaCO3 = CaO + CO2↑ — Q
С целью «запутывания» может быть дана энтальпия, она при таких реакциях всегда: ΔH > 0, так как внутренняя
энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)

Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик»)
является примером экзотермического разложения, при котором тепло выделяется.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Качественные реакции на неорганические вещества и ионы
Таблица. Качественные реакции на анионы
| Анион | Реактив | Наблюдаемая реакция |
| SO42- | соли Ва2+ | Выпадение белого осадка BaSO4 |
| NO3— | добавить конц. H2SO4 и Сu, нагреть | Образование голубого раствора (ионы Сu2+), выделение газа бурого (NO2) |
| РО43- | ионы Ag+ | Выпадение светло-желтого осадка в нейтральной среде:
ЗАg+ + РO43- = Аg3РO4 |
| СrO42- | ионы Ва2+ | Выпадение желтого осадка:
Ва2+ + СrO42- = BaCrO4 |
| S2- | ионы Рb2+ | Выпадение черного осадка:
Pb2+ + S2- = PbS |
| СО32- | ионы Са2+ | выпадение белого осадка СаСО3 |
| CO2 | известковая вода Са(ОН)2 | Выпадение белого осадка и его растворение при пропускании СO2:
Са(ОН)2 + СO2 = СаСО3+Н2O СаСО3 + СO2 + Н2O = Са(НСO3)2 |
| SO32- | ионы Н+ | Появление запаха SO2:
2Н+ + SO32- = Н2O + SO2 Сернистый газ обесцвечивает бромную воду. |
| F— | ионы Са2+ | Выпадение белого осадка:
Са2+ + 2F— = CaF2 |
| Cl— | ионы Аg+ | Выпадение белого творожистого осадка:
Аg+ + Cl— = AgCl |
| Br— | ионы Аg+ | Выпадение светло-желтого осадка:
Ag+ + Br— = AgBr осадок темнеет на свету |
| I— | ионы Аg+ | Выпадение желтого осадка:
Аg+ + I— = АgI осадок темнеет на свету |
| ОН— | индикаторы: лакмус
фенолфталеин |
синее окрашивание
малиновое окрашивание |
Таблица. Качественные реакции на катионы
| Катион | Реактив | Наблюдаемая реакция |
| Li+ | Пламя | Карминово-красное окрашивание |
| Na+ | Пламя | Желтое окрашивание |
| K+ | Пламя | Фиолетовое окрашивание |
| Ca2+ | Пламя | Кирпично-красное окрашивание |
| Sr2+ | Пламя | Карминово-красное окрашивание |
| Ba2+ | 1) Пламя
2) Ион SO42- |
1) Желто-зеленое окрашивание
2) Выпадение белого осадка BaSO4 |
| Cu2+ | 1) Вода
2) Ионы ОН— |
1) Растворы солей Сu2+ имеют голубую окраску
2) Голубой осадок Cu(OH)2 |
| Pb2+ | Ион S2- | Выпадение черного осадка: PbS |
| Ag+ | Ион Cl— | Выпадение белого осадка:
Аg+ + Cl— = AgCl |
| Fe2+ | Красная кровяная соль, K3[Fe(CN)6] | Выпадение синего осадка KFe[Fe(CN)6] |
| Fe3+ | 1) Желтая кровяная соль, K4[Fe(CN)6] 2) Роданид-ион SCN— |
1) Выпадение синего осадка: KFe[Fe(CN)6]
2) Появление ярко-красного окрашивания |
| Al3+ | Щелочь (амфотерные свойства гидроксида) | Выпадение белого осадка гидроксида алюминия при добавлении первых порций щелочи и его растворение при дальнейшем добавлении. |
| NH4+ | Щелочь при нагревании | Запах аммиака NH3 и окрашивание влажного лакмуса в синий цвет |
| H+ | Индикаторы: лакмус, метилоранж | Красное окрашивание (кислая среда) |
Таблица. Качественные реакции на газы
| Газ | Качественная реакция |
| Водород, H2 | Хлопок при поднесении горящей лучинки к источнику водорода |
| Азот, N2 | Горящая лучинка тухнет в атмосфере азота. При пропускании через раствор Ca(OH)2 осадок не выпадает |
| Кислород, O2 | Тлеющая лучинка ярко загорается в атмосфере кислорода |
| Озон, O3 | Взаимодействие озона с раствором иодидов с выпадением кристаллического иода I2 в осадок:
2KI + O3 + H2O = 2KOH + I2↓ + O2↑ |
| Хлор, Сl2 | При взаимодействии хлора с растворами иодидов в осадок выпадает желтый осадок йода I2:
2KI + Cl2 = 2KCl + I2↓ |
| Аммиак, NH3 | Резкий запах; влажный лакмус синеет. Реакция аммиака с хлороводородом («дым» без огня):
NH3 + HCl = NH4Cl |
| Углекислый газ, CO2 | Тлеющая лучинка гаснет в атмосфере углекислого газа. Пропускание углекислого газа через известковую воду Ca(OH)2: Ca(OH)2 + CO2 = CaCO3↓ + H2O Дальнейшее пропускание приведет к растворению осадка: CaCO3 + CO2 + H2O = Ca(HCO3)2 |
| Оксид азота (II), NO | Оксид азота (II) очень чувствителен к кислороду воздуха, потому на воздухе буреет, окисляясь до оксида азота (IV) NO2:
2NO+ O2 = 2NO2 |
| Сернистый газ, SO2 | Обесцвечивание бромной воды и раствора перманганата калия |
| Сероводород, H2S | Чёрный осадок сульфида при пропускании через раствор соли меди или свинца |

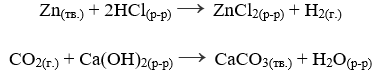



















 овалентная
овалентная еполярная
еполярная