Муниципальное автономное общеобразовательное учреждение
средняя общеобразовательная школа №9
Таблицы и схемы по химии
при подготовке к ЕГЭ.
учитель химии МАОУ СОШ №9
Моргунов Н.М.
ст. Темиргоевская 2018г.
Используемая литература:
-
Н.Е.Кузьменко, В.В.Ерёмин, В.А.Попков «Начала химии». Со-временный курс для поступающих в ВУЗы. – М.: «Экзамен», 2001г.
-
А.И.Артёменко «Органическая химия». Учебник для строит. спец. вузов. – М.: «Высшая школа», 1994г.
-
А.С.Егоров, Г.Х.Аминова «Экспресс-курс неорганической и органической химии. Для поступающих в ВУЗы.» — Ростов-на-Дону: «Феникс», 2002г.
-
А.С.Егоров «Химия в 400-х вопросах и ответах». (Пособие для учащихся и абитуриентов). Ростов-на-Дону: «Феникс», 2001 г.
-
А.С.Егоров «Как сдать ЕГЭ по химии на 100 баллов». – Ростов-на-Дону: «Феникс», 2003г.
-
И.А.Фрейфельд «Общая химия». Пособие для абитуриентов и старшеклассников. М.: «Московский лицей», 1996г.
-
И.И.Новошинский, Н.С.Новошинская «Переходные элементы и их соединения». Пособие для старшеклассников и абитуриентов. – Краснодар: «Советская Кубань», 2006г.
-
И.И.Новошинский, Н.С.Новошинская «Органическая химия 11 класс». Учебник для общеобразовательных учреждений. – М.: «Образование», 2005г.
-
И.И.Новошинский, Н.С.Новошинская «Химия. 10 класс». Учебник для общеобразовательных учреждений. – М.: «Оникс» «Мир и Образование», 2006г.
Тепловой эффект растворения веществ:
газы CO2
кислоты H2SO4
щёлочи NaOH
соли:
CuSO4
FeSO4
ZnSO4
Na2SO4
Na2CO3
AlCl3
AgNO3
NaCl
NaNO3
KNO2
NH4NO3
CuSO4 . 5H2O FeSO4 . 7H2O } купоросы
ZnSO4 . 7H2O
Na2SO4 . 10H2O кристаллическая сода
Na2СO3 . 10H2O Глауберова соль
AlCl3. 6H2O
Тепловой эффект химических реакций:
экзотермические (+Q)
эндотермические (-Q)
а) соединения искл. N2 + O2 = 2NO — Q
б) нейтрализации
в) замещения
г) овр
а) разложения
искл. 2H2O2 = 2H2O + O2 + Q
(NH4)2Cr2O7 = Cr2O3 + N2 +4H2O + Q
б) гидролиз
Механизмы органических реакций:
радикальный
( hv, t, H2O2 )
ионный
1) Замещение:
а) предельных у/в
hv
CH4 + Cl2 → CH3Cl + HCl
б) непредельных у/в ( у α-атома) – р-ция Львова.
hv
CH2=CH-CH3 + Cl2 → CH2=CH-CH3 + HCl
в) ароматических у/в ( в боковой цепи)
t, hv
С6Н5-СН2-СН3 + Cl2 → C6H5—CHCl—CH3 + HCl
2) Присоединение : a) непредельных у/в против правила Марковникова:
H2 O 2
CH3 –CH =CH2 + HCl → CH3-CH2-CH2Cl
б) ароматических у/в
hv
C6H6 + Cl2 → C6H6Cl6
3) Полимеризация:
n СН2=СН2 → (-СН2-СН2— )n
4) Горение, окисление:
t
CH4 + 2O2 → CO2 + 2H2O
1) Замещение в бензольном кольце:
FeCl3 , t
С6Н6 + Cl2 → C6H5Cl + HCl
H2SO4k, t
C6H6 + HNO3 → C6H5-NO2 + H2O
2) Присоединение непредельных у/в ( кроме гидрирования):
CH3-CH=CH2 + HCl → CH3-CHCl-CH3
3) Полимеризация ( в присутствии катализатора)
O2
n CH2=CH2 → (-CH2-CH2)n
H2SO4
n CH2=C-CH=CH2 → (-CH2-C=CH-CH2-)n
| |
CH3 CH3
Периодический закон и периодическая система.
№ периода = числу электронных слоёв
№ группы = числу (внешних) валентных электронов (для главных подгрупп)

электроотрицательность радиус атомов ув.
ув.
Fr

неметаллические и металлические и
окислительные свойства восстановительные свойства
ув.
ув.
Fr

HClO4 – самая сильная кислородсодержащая кислота
FrOH HI – самая сильная бескислородная кислота
самое сильное основание
внешние

валентные внешние S и предвнешние d ( кроме Zn, Cd, Hg ) d — элементы
э

Химическое равновесие.
υ прям.= υ обратн. ( при данных условиях )
υ пр [HI]2
H

ющих веществ )

C
[CO2]
Факторы смещения хим. равновесия ( принцип Ле-Шателье) :
1) Изменение концентрации ( кроме тв. веществ) : ув. исх.
ув. продукты
2) Изменение температуры : ув. t — Q


ум. Р ув. Р

2 моль 2 моль
Катализатор на смещение равновесия не влияет.
Смещение равновесия при диссоциации:
разбавление , связывание одного из ионов → (н: NaOH )
C
← ув. концентрации, введение одноимённых ионов (н: CH3COONa, HCl)
Смещение равновесия гидролиза:
Разбавление, нагревание, связывание одного из ионов → ( н: NH4Cl => H+ )
N
C
← ув. концентрации, охлаждение, введение одноимённых ионов (н: K2S => OH— )
Скорость химической реакции.
нет поверхности раздела гомогенные υ = +_ Δν / v . Δτ

υср. = +_ Δ С / Δ τ ; [ моль/ л . сек ]
Реакции –

т + ж, т + г, т + т гетерогенные υ = +_ Δ ν / s . Δτ
Факторы, влияющие на скорость:
1) Концентрация : чем > С , тем > υ
ув.Р ( для газов) ум. V
N2 + 3H2 = 2NH3υ = k [ N2 ] . [ H2 ] 3 — кинетическое уравнение закона действующих масс
4Al (тв.)+ 3O2(г) = 2Al2O3υ = k [ O2 ] 3 — твёрдые не входят ( для гетерогенных реакций)
Fe порошок + CuSO4 10% > Fe порошок + CuSO4 4% > Fe гвоздь + CuSO4 4%
2) Температура: при повышении t на каждые 100υ ув. в 2-4 раза ( правило Вант-Гоффа ) , т.к.
ув. число активных частиц (способных преодолеть Еакт. )
t2 — t 1

υ t2 = γ

3) Природа реагирующих веществ:
а) υ в-в с ионной и полярной ков. связью > υ в-в с неполярной или малополярной связью
н/о Zn + HCl = > органические Zn + CH3COOH =
б) активность металлов Mg + HCl > Fe + HCl неметаллов F2 + H2 > I2 + H2
K + H2O > Li + H2O (взрыв)
4) Площадь поверхности (для твёрдых в-в) : чем > S поверн. , тем > υ
Al порошок горит, Al ложка нет

— ↑
NO(г)

гетерогенный (в разных) N2 (Г) + 3H2 (Г) = 2NH3

В
промоторы
Разрушение комплексных солей и солей анионного типа:
1) Na2[ Zn(OH)4 ] + 2HCl нед. = Zn(OH)2 ↓ + 2NaCl + 2H2O
Na2[ Zn(OH)4 ] + 4HCl изб. = 2ZnCl2 +2NaCl + 4H2O
2) Na3[ Al(OH)6 ] + 3H2CO3 = Al(OH)3↓ + 3NaHCO3 + 3H2O
Na3[ Al(OH)6 ] + 3H2S = Al(OH)3↓ + 3NaHS + 3H2O
3) Na[ Al(OH)4 ] + CO2 = Al(OH)3 ↓ + NaHCO3
Na3[ Cr(OH)6 ] + 3SO2 = Cr(OH)3↓ + 3NaHSO3
4) Na3[ Cr(OH)6 ] + FeCl3 = Cr(OH)3↓ + Fe(OH)3 + 3NaCl
3Na[Al(OH)4 ] + AlCl3 = 4Al(OH)3↓ + 3NaCl
5) 2Na3[ Cr(OH)6 ] + 3H2O2 = 2Na2CrO4 + 2NaOH + 8H2O
t
6) Na[ Al(OH)4 ] = NaAlO2 + 2H2O
t
Na2[ Zn(OH)4 ] = ZnO + H2O + NaOH
7) 2Na[ Cr(OH)4 ] + 3Br2 + 8NaOH = 2Na2CrO4 + 6NaBr + 8H2O
Na2ZnO2 + 2HCl нед.= Zn(OH)2↓ + 2NaCl
Na2ZnO2 + 4HCl изб.= ZnCl2 + 2NaCl + 2H2O
NaAlO2 + HCl нед.+ H2O = Al(OH)3↓ + NaCl
NaAlO2 + 4HCl изб.= AlCl3 + NaCl + 2H2O
Образование комплексных солей и солей анионного типа:
а) в растворах:
1) NaOH + Al(OH)3 = Na[ Al(OH)4 ] или 3NaOH + Al(OH)3 = Na3[ Al(OH)6 ]
OH— + Al(OH)3 = [ Al(OH)4 ] — 3OH— + Al(OH)3 = [ Al(OH)6 ]3-
2) 2NaOH + Al2O3 + 3H2O = 2Na[ Al(OH)4 ] — тетрагидроксоалюминат
3) 2NaOH + 2Al + 6H2O = 2Na[ Al(OH)4 ] + 3H2↑
4) 4NaOH + AlCl3 = Na[ Al(OH)4 ] + 3NaCl
Na[ Cr(OH)4 ] ; Na3[ Cr(OH)6 ] ; Na[ Fe(OH)4 ] ; Na3[ Fe(OH)6 ]
тетрагидроксохромат гексагидроксохромат тетрагидроксоферрат гексагидроксоферрат
1) 2NaOH + Zn(OH)2 = Na2[ Zn(OH)4 ] — тетрагидроксоцинкат
2OH— + Zn(OH)2 = [ Zn(OH)4 ]2-
2) 2NaOH + ZnO + H2O = Na2[ Zn(OH)4 ]
3) 2NaOH + Zn + 2H2O = Na2[ Zn(OH)4 ] + H2↑
4) 4NaOH + ZnCl2 = Na2[ Zn(OH)4 ] + 2NaCl
Na2[ Be(OH)4 ] ; Na2[ Sn(OH)4 ] ; Na2[ Pb(OH)4 ]
тетрагидроксобериллат тетрагидроксостаннит тетрагидроксоплюмбит
t t
слабоамфотерные : Fe(OH)3 + NaOHконц = Na[ Fe(OH)4 ] ; Cu(OH)2 + 2NaOHконц >40% = Na2[ Cu(OH)4 ]
б) в расплавах:
Zn(OH)2 <=> H2ZnO2 ; Al(OH)3 <=> H3AlO3 – ортоалюминиевая кислота
HAlO2 – метаалюминиевая кислота
t
2NaOH + Zn(OH)2 = Na2ZnO2 + H2O
цинкат
tt
NaOH + Al(OH)3 = NaAlO2 + 2H2O 3NaOH + Al(OH)3 = Na3AlO3 + 3H2O
метаалюминат ортоалюминат
Na2BeO2 ; Na2SnO2 ; Na2PbO2 ; Na2CuO2
бериллат станнит плюмбит купрат (II)
NaCrO2 ; NaFeO2 ; Na2FeO4
метахромат феррат (III ) феррат ( VI )
Именные реакции:
t
1) Коновалова (нитрование): CH4 + HO—NO2 разб → CH3—NO2 + H2O
t
2) Вюрца: CH3-Br + 2Na + Br-CH3 → CH3-CH3 + 2NaBr
Cl CH3


эфир t
4) Гриньяра: CH3Cl + Mg → CH3-Mg-Cl ; CH3-Mg-Cl + Cl-CH2-CH3 → CH3-CH2-CH3 + MgCl2
t
5) Дюма (декарбоксилирование): CH3-COONa + NaOH → CH4 + Na2CO3
KMnO4
6) Вагнера: CH2=CH2 + [O] + H2O → CH2-CH2
| |
OH OH
3CH2=CH2 + 2KMnO4 + 4H2O → 3 CH2-CH2 + 2MnO2↓ + 2KOH
| |
OH OH

7) Лебедева: 2C2H5OH t CH2=CH-CH=CH2 + 2H2O + H2↑
t, Cr2O3, Al2O3




H





или C6H5NO2 + 3(NH4)2S + 7HCl → [C6H5NH3]Cl + 3S + 6NH4Cl + 2H2O
H+, t
13) Кирхгофа: (C6H10O5)n + nH2O → nC6H12O6
14) Кольбе (электролиз р-ра солей карбоновых кислот):
эл. ток
2CH3COONa + 2H2O → H2↑ + 2NaOH + CH3-CH3↑ + 2CO2↑
(K) (A)
hv α
15) Львова: CH3-CH=CH2 + Cl2 → Cl-CH2-CH=CH2 + HCl
|
Химическая связь и типы кристаллических решёток. |
|||
|
К |
н (одинаковые) . неМе – неМе полярная (разные) |
||
|
Атомная B, C (алмаз, графит), Si, Ge, As, Se,Te (SiO2-кварц, SiC-карбид). Молекулярная N2 . P4 . O2 , S8, H2 , F2 , Cl2, Br2 , I2 , благородные газы (искл. Rn), CO2 –«сухой лёд», NH3 ,H2 O, C6 H6 и т.д. |
Очень твёрдые, тугоплавкие, нераство-римые, не проводят ток и тепло (искл. Si и Ge – п/п). |
||
|
Малая твёрдость, летучие, низкая Тпл. и кип., многие не растворимы и не про-водят ток. |
|||
|
Ионная |
Ме – неМЕ |
Ионная NaCl, Li2 SO4 , KOH, Na 2 O, [CH3 –NH3] Cl |
Твёрдые, хрупкие, тугоплавкие, тепло-стойкие, растворы и расплавы прово-дят ток. |
|
Металлическая |
Ме |
Металлическая Fe, Cu и т.п. |
Ковкие, пластичные, с металлическим блеском, проводят ток и тепло. |
|
Водородная (между молекулами) |
H…(O,N,F) в разных молекулах |
между молекулами (H2 O)n , (HF)n H – O … H – O … ; H – F … H – F … H H |
ДНК внутримолекулярная |
|
Донорно- акцепторная (ковалентная связь) |
+ + _ NH4 , H3O , BF4 и комплексные соединения O3, CO |
H H H:N: + __ H+ → [ H—N—H ]+ ; H:O: + __ H → [ H:O:H ]+ H H H H B= IV B= III Na2 [ Zn(OH)4 ] |
F F F:B: __ + :F: → [F:B:F ]— F F |
6 августа 2021
В закладки
Обсудить
Жалоба
ЕГЭ по химии: справочные материалы
Предложенный материал адресован абитуриентам, преподавателям химии и ученикам 8-11 классов.
Материал содержит справочные таблицы, тривиальные названия неорганических и органических соединений, краткие теоретические сведения о гидролизе, электролизе, тренажёр для повторения большого количества неорганических реакций.
spr-himiya.docx
spr-himiya.pdf
Автор: Аветисян Сатеник Вагеевна.
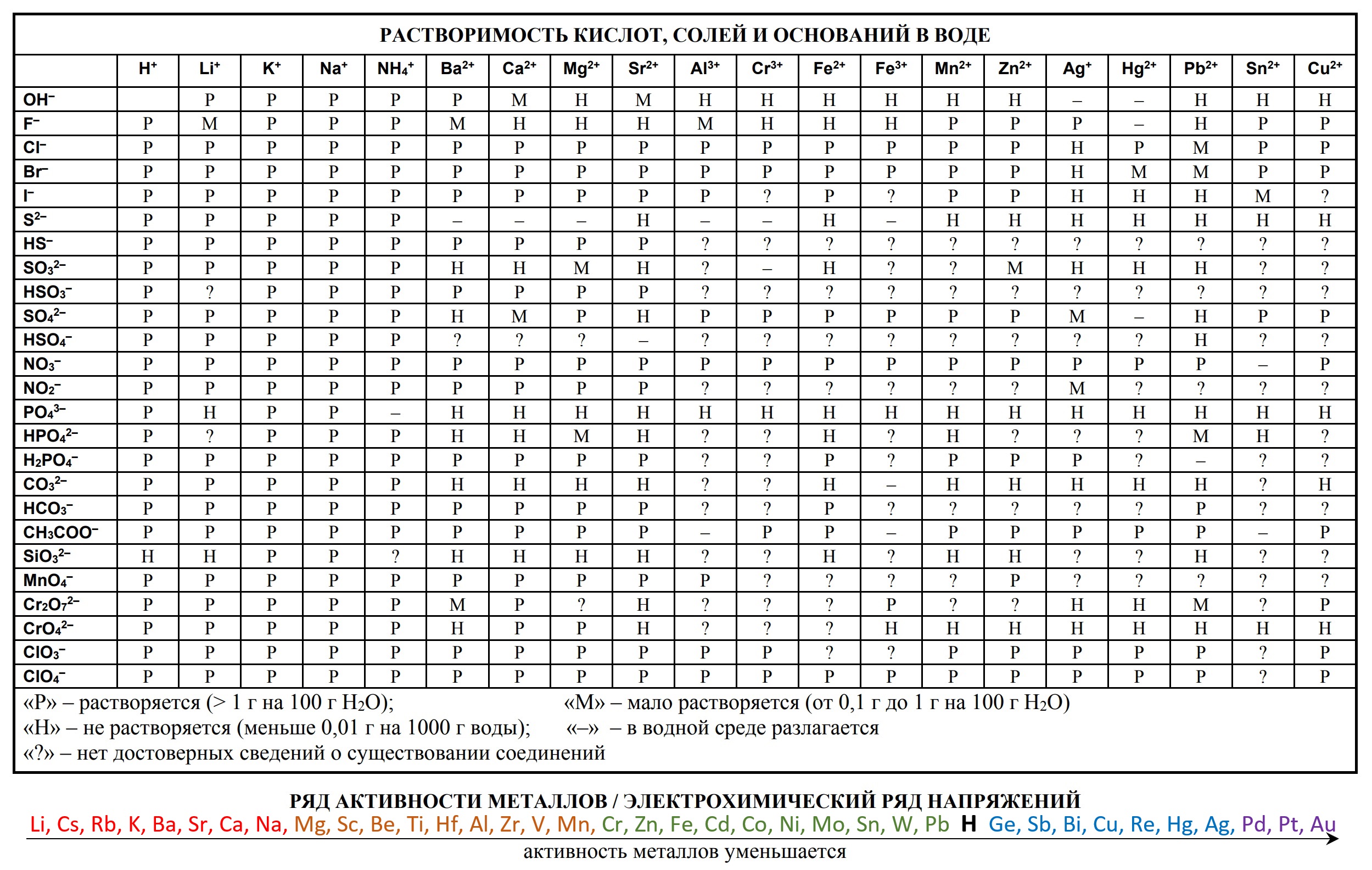
Таблицы на ЕГЭ и ОГЭ по химии
На сдаче ЕГЭ и ОГЭ по химии можно использовать три таблицы:
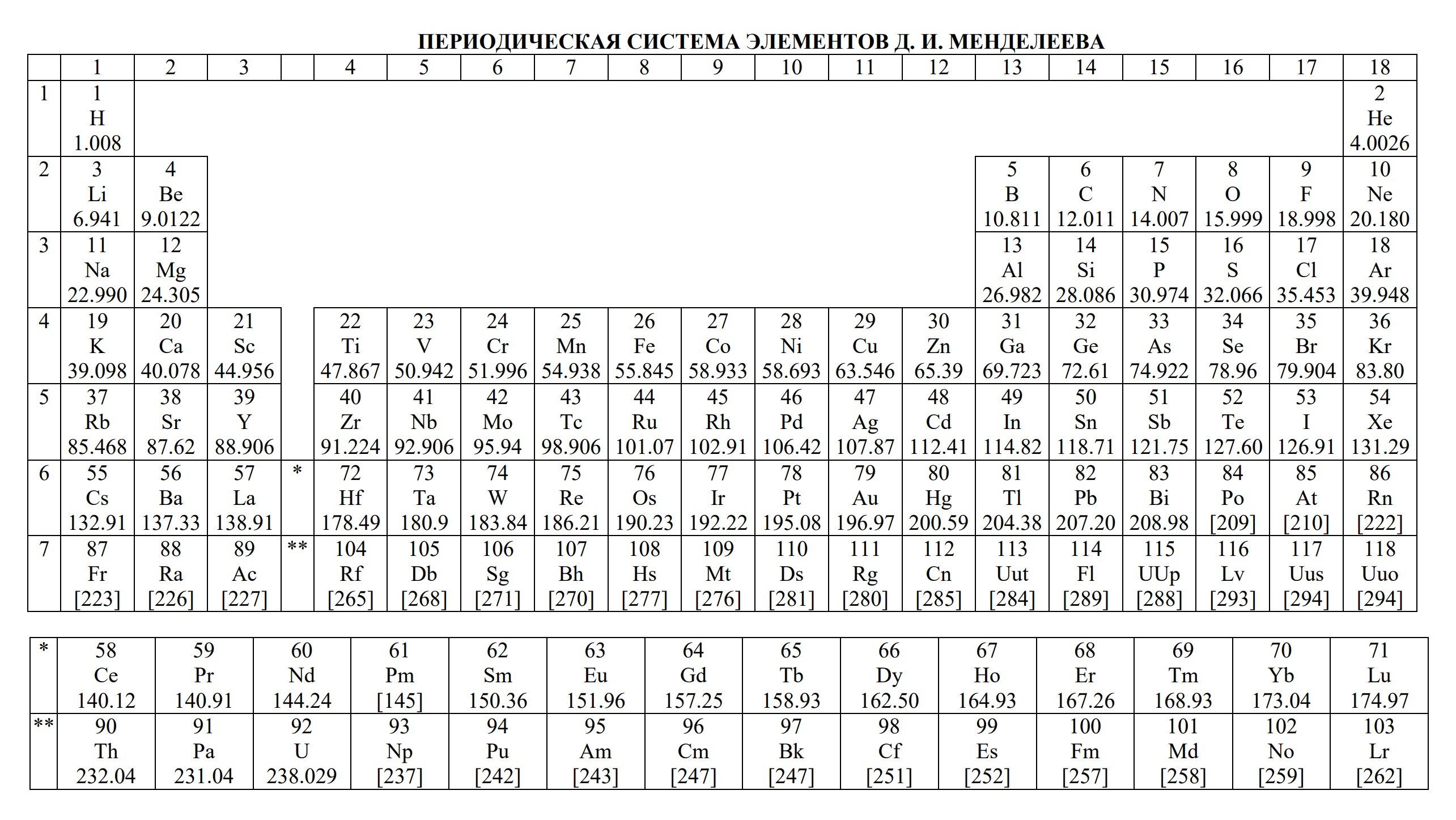
- периодическая система химических элементов Д.И. Менделеева
- таблица растворимости
- ряд активности металлов.
Они содержат в себе 80% информации, необходимой для решения большинства заданий.
Однако таблицы на форзацах разных учебников, продаваемые в книжных магазинах, располагающиеся на просторах интернета отличаются не только оформлением, но и содержанием. Что бы они оказались надёжно шпаргалкой, а не приятной неожиданностью, лучше с самого начала начинать работать с тем форматом, который официально разрешен на ЕГЭ твоего года.
Скачать эти таблицы можно ниже. А как сделать эти безликие таблицы наиболее информационными для тебя я расскажу на уроке.
- Таблица Д.И. Менделеева для ОГЭ и ЕГЭ
- Таблица растворимости и ряд активности для ОГЭ и ЕГЭ
- Таблица растворимости с расширенным рядом активности
- Таблица Д.И. Менделеева длиннопериодная для олимпиады
Качественные реакции на неорганические вещества и ионы
Таблица. Качественные реакции на анионы
| Анион | Реактив | Наблюдаемая реакция |
| SO42- | соли Ва2+ | Выпадение белого осадка BaSO4 |
| NO3— | добавить конц. H2SO4 и Сu, нагреть | Образование голубого раствора (ионы Сu2+), выделение газа бурого (NO2) |
| РО43- | ионы Ag+ | Выпадение светло-желтого осадка в нейтральной среде:
ЗАg+ + РO43- = Аg3РO4 |
| СrO42- | ионы Ва2+ | Выпадение желтого осадка:
Ва2+ + СrO42- = BaCrO4 |
| S2- | ионы Рb2+ | Выпадение черного осадка:
Pb2+ + S2- = PbS |
| СО32- | ионы Са2+ | выпадение белого осадка СаСО3 |
| CO2 | известковая вода Са(ОН)2 | Выпадение белого осадка и его растворение при пропускании СO2:
Са(ОН)2 + СO2 = СаСО3+Н2O СаСО3 + СO2 + Н2O = Са(НСO3)2 |
| SO32- | ионы Н+ | Появление запаха SO2:
2Н+ + SO32- = Н2O + SO2 Сернистый газ обесцвечивает бромную воду. |
| F— | ионы Са2+ | Выпадение белого осадка:
Са2+ + 2F— = CaF2 |
| Cl— | ионы Аg+ | Выпадение белого творожистого осадка:
Аg+ + Cl— = AgCl |
| Br— | ионы Аg+ | Выпадение светло-желтого осадка:
Ag+ + Br— = AgBr осадок темнеет на свету |
| I— | ионы Аg+ | Выпадение желтого осадка:
Аg+ + I— = АgI осадок темнеет на свету |
| ОН— | индикаторы: лакмус
фенолфталеин |
синее окрашивание
малиновое окрашивание |
Таблица. Качественные реакции на катионы
| Катион | Реактив | Наблюдаемая реакция |
| Li+ | Пламя | Карминово-красное окрашивание |
| Na+ | Пламя | Желтое окрашивание |
| K+ | Пламя | Фиолетовое окрашивание |
| Ca2+ | Пламя | Кирпично-красное окрашивание |
| Sr2+ | Пламя | Карминово-красное окрашивание |
| Ba2+ | 1) Пламя
2) Ион SO42- |
1) Желто-зеленое окрашивание
2) Выпадение белого осадка BaSO4 |
| Cu2+ | 1) Вода
2) Ионы ОН— |
1) Растворы солей Сu2+ имеют голубую окраску
2) Голубой осадок Cu(OH)2 |
| Pb2+ | Ион S2- | Выпадение черного осадка: PbS |
| Ag+ | Ион Cl— | Выпадение белого осадка:
Аg+ + Cl— = AgCl |
| Fe2+ | Красная кровяная соль, K3[Fe(CN)6] | Выпадение синего осадка KFe[Fe(CN)6] |
| Fe3+ | 1) Желтая кровяная соль, K4[Fe(CN)6] 2) Роданид-ион SCN— |
1) Выпадение синего осадка: KFe[Fe(CN)6]
2) Появление ярко-красного окрашивания |
| Al3+ | Щелочь (амфотерные свойства гидроксида) | Выпадение белого осадка гидроксида алюминия при добавлении первых порций щелочи и его растворение при дальнейшем добавлении. |
| NH4+ | Щелочь при нагревании | Запах аммиака NH3 и окрашивание влажного лакмуса в синий цвет |
| H+ | Индикаторы: лакмус, метилоранж | Красное окрашивание (кислая среда) |
Таблица. Качественные реакции на газы
| Газ | Качественная реакция |
| Водород, H2 | Хлопок при поднесении горящей лучинки к источнику водорода |
| Азот, N2 | Горящая лучинка тухнет в атмосфере азота. При пропускании через раствор Ca(OH)2 осадок не выпадает |
| Кислород, O2 | Тлеющая лучинка ярко загорается в атмосфере кислорода |
| Озон, O3 | Взаимодействие озона с раствором иодидов с выпадением кристаллического иода I2 в осадок:
2KI + O3 + H2O = 2KOH + I2↓ + O2↑ |
| Хлор, Сl2 | При взаимодействии хлора с растворами иодидов в осадок выпадает желтый осадок йода I2:
2KI + Cl2 = 2KCl + I2↓ |
| Аммиак, NH3 | Резкий запах; влажный лакмус синеет. Реакция аммиака с хлороводородом («дым» без огня):
NH3 + HCl = NH4Cl |
| Углекислый газ, CO2 | Тлеющая лучинка гаснет в атмосфере углекислого газа. Пропускание углекислого газа через известковую воду Ca(OH)2: Ca(OH)2 + CO2 = CaCO3↓ + H2O Дальнейшее пропускание приведет к растворению осадка: CaCO3 + CO2 + H2O = Ca(HCO3)2 |
| Оксид азота (II), NO | Оксид азота (II) очень чувствителен к кислороду воздуха, потому на воздухе буреет, окисляясь до оксида азота (IV) NO2:
2NO+ O2 = 2NO2 |
| Сернистый газ, SO2 | Обесцвечивание бромной воды и раствора перманганата калия |
| Сероводород, H2S | Чёрный осадок сульфида при пропускании через раствор соли меди или свинца |

Подготовка к ЕГЭ начинается с
психологического настроя на успех, обязательную сдачу ЕГЭ.
Поэтому не
лишними будут помощь психолога, советы родителей и учителей.
Теория к ЕГЭ. Методика самостоятельной подготовки к ЕГЭ
ТЕОРИЯ ДЛЯ СДАЮЩИХ ЕГЭ
Дopoнькин ЕГЭ. Химия. Большой справочник
Adobe Acrobat Document
7.6 MB
РАСПЕЧАТАТЬ И ИСПОЛЬЗОВАТЬ
Методические рекомендации по подготовке
Adobe Acrobat Document
375.5 KB
ПРОРАБОТАТЬ И ПРИНЯТЬ К СВЕДЕНИЮ
анализ типичных ошибок ЕГЭ-2019 г.pdf
Adobe Acrobat Document
771.7 KB
ПРОГРАММА ПОДГОТОВКИ К ЕГЭ ПО ХИМИИ.doc
Microsoft Word Document
129.5 KB
ВНИМАНИЕ
Тривиальные названия органических вещест
Adobe Acrobat Document
340.1 KB
Теория и тест для самостоятельной проработки.
Основные способы получения металлов.pptx
Microsoft Power Point Presentation
920.7 KB
Все свойства органических веществ.
Реакции к основным темам курса 10 класса
Microsoft Word Document
158.0 KB
Общие формулы. УЧИТЬ!!!
Общие формулы классов органических вещес
Adobe Acrobat Document
188.4 KB
Металлы. Соединения металлов. УЧИТЬ!!!
Свойства металлов и их соединений.docx
Microsoft Word Document
2.5 MB
Цепочки превращений.
Задание С3. Цепочки превращений..docx
Microsoft Word Document
674.8 KB
Теория по основным классам неорганических соединений.
Основные классы и их свойства.doc
Microsoft Word Document
880.0 KB
Нужно разобраться и выучить.
Ряд активности металлов.pdf
Adobe Acrobat Document
315.0 KB

Документация и подготовка к ЕГЭ
таблица ПСХЭ.doc
Microsoft Word Document
396.5 KB
Таблица растворимости некоторых веществ
Microsoft Word Document
578.5 KB

Дополнительная информация, теория к ЕГЭ
Адреса сайтов подготовки.
Материалы для подготовки к ОГЭ и ЕГЭ.doc
Microsoft Word Document
15.2 KB
Таблица. Качественные признаки веществ.d
Microsoft Word Document
44.8 KB
Ряд ЭО. Названия кислот и остатков. Степ
Microsoft Word Document
518.7 KB
Таблица ПСХЭ . С обозначением классов со
Microsoft Word Document
498.4 KB
цвета оксидов.doc
Microsoft Word Document
24.0 KB
Номенклатура неорганических веществ.doc
Microsoft Word Document
135.5 KB
Определение ионов. Качественные реакции.
Microsoft Word Document
51.0 KB
Часть представленных здесь материалов взята с
сайта учителя химии Сикорской О.Э.
2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная).
Классификация неорганических веществ с примерами соединений
Теперь проанализируем представленную выше классификационную схему более детально.
Как мы видим, прежде всего все неорганические вещества делятся на простые и сложные:
Простыми веществами называют такие вещества, которые образованы атомами только одного химического элемента. Например, простыми веществами являются водород H2, кислород O2, железо Fe, углерод С и т.д.
Среди простых веществ различают металлы, неметаллы и благородные газы:
Металлы образованы химическими элементами, расположенными ниже диагонали бор-астат, а также всеми элементами, находящимися в побочных группах.
Благородные газы образованы химическими элементами VIIIA группы.
Неметаллы образованы соответственно химическими элементами, расположенными выше диагонали бор-астат, за исключением всех элементов побочных подгрупп и благородных газов, расположенных в VIIIA группе:
Названия простых веществ чаще всего совпадают с названиями химических элементов, атомами которых они образованы. Однако для многих химических элементов широко распространено такое явление, как аллотропия. Аллотропией называют явление, когда один химический элемент способен образовывать несколько простых веществ. Например, в случае химического элемента кислорода возможно существование молекулярных соединений с формулами O2 и O3. Первое вещество принято называть кислородом так же, как и химический элемент, атомами которого оно образовано, а второе вещество (O3) принято называть озоном. Под простым веществом углеродом может подразумеваться любая из его аллотропных модификаций, например, алмаз, графит или фуллерены. Под простым веществом фосфором могут пониматься такие его аллотропные модификации, как белый фосфор, красный фосфор, черный фосфор.
Сложные вещества
Сложными веществами называют вещества, образованные атомами двух или более химических элементов.
Так, например, сложными веществами являются аммиак NH3, серная кислота H2SO4, гашеная известь Ca(OH)2 и бесчисленное множество других.
Среди сложных неорганических веществ выделяют 5 основных классов, а именно оксиды, основания, амфотерные гидроксиды, кислоты и соли:
Оксиды — сложные вещества, образованные двумя химическими элементами, один из которых кислород в степени окисления -2.
Общая формула оксидов может быть записана как ЭxOy, где Э — символ какого-либо химического элемента.
Номенклатура оксидов
Название оксида химического элемента строится по принципу:
Например:
Fe2O3 — оксид железа (III); CuO — оксид меди (II); N2O5 — оксид азота (V)
Нередко можно встретить информацию о том, что в скобках указывается валентность элемента, однако же это не так. Так, например, степень окисления азота N2O5 равна +5, а валентность, как это ни странно, равна четырем.
В случае, если химический элемент имеет единственную положительную степень окисления в соединениях, в таком случае степень окисления не указывается. Например:
Na2O — оксид натрия; H2O — оксид водорода; ZnO — оксид цинка.
Классификация оксидов
Оксиды по их способности образовывать соли при взаимодействии с кислотами или основаниями подразделяют соответственно на солеобразующие и несолеобразующие.
Несолеобразующих оксидов немного, все они образованы неметаллами в степени окисления +1 и +2. Список несолеобразующих оксидов следует запомнить: CO, SiO, N2O, NO.
Солеобразующие оксиды в свою очередь подразделяются на основные, кислотные и амфотерные.
Основными оксидами называют такие оксиды, которые при взаимодействии с кислотами (или кислотными оксидами) образуют соли. К основным оксидам относят оксиды металлов в степени окисления +1 и +2, за исключением оксидов BeO, ZnO, SnO, PbO.
Кислотными оксидами называют такие оксиды, которые при взаимодействии с основаниями (или основными оксидами) образуют соли. Кислотными оксидами являются практически все оксиды неметаллов за исключением несолеобразующих CO, NO, N2O, SiO, а также все оксиды металлов в высоких степенях окисления (+5, +6 и +7).
Амфотерными оксидами называют оксиды, которые могут реагировать как с кислотами, так и основаниями, и в результате этих реакций образуют соли. Такие оксиды проявляют двойственную кислотно-основную природу, то есть могут проявлять свойства как кислотных, так и основных оксидов. К амфотерным оксидам относятся оксиды металлов в степенях окисления +3, +4, а также в качестве исключений оксиды BeO, ZnO, SnO, PbO.
Некоторые металлы могут образовывать все три вида солеобразующих оксидов. Например, хром образует основный оксид CrO, амфотерный оксид Cr2O3 и кислотный оксид CrO3.
Как можно видеть, кислотно-основные свойства оксидов металлов напрямую зависят от степени окисления металла в оксиде: чем больше степень окисления, тем сильнее выражены кислотные свойства.
Основания
Основания — соединения с формулой вида Me(OH)x, где x чаще всего равен 1 или 2.
Исключения: Be(OH)2, Zn(OH)2, Sn(OH)2 и Pb(OH)2 не относятся к основаниям, несмотря на степень окисления металла +2. Данные соединения являются амфотерными гидроксидами, которые еще будут рассмотрены в этой главе более подробно.
Классификация оснований
Основания классифицируют по количеству гидроксогрупп в одной структурной единице.
Основания с одной гидроксогруппой, т.е. вида MeOH, называют однокислотными основаниями, с двумя гидроксогруппами, т.е. вида Me(OH)2, соответственно, двухкислотными и т.д.
Также основания подразделяют на растворимые (щелочи) и нерастворимые.
К щелочам относятся исключительно гидроксиды щелочных и щелочно-земельных металлов, а также гидроксид таллия TlOH.
Номенклатура оснований
Название основания строится по нижеследующему принципу:
Например:
Fe(OH)2 — гидроксид железа (II),
Cu(OH)2 — гидроксид меди (II).
В тех случаях, когда металл в сложных веществах имеет постоянную степень окисления, указывать её не требуется. Например:
NaOH — гидроксид натрия,
Ca(OH)2 — гидроксид кальция и т.д.
Кислоты
Кислоты — сложные вещества, молекулы которых содержат атомы водорода, способные замещаться на металл.
Общая формула кислот может быть записана как HxA, где H — атомы водорода, способные замещаться на металл, а A — кислотный остаток.
Например, к кислотам относятся такие соединения, как H2SO4, HCl, HNO3, HNO2 и т.д.
Классификация кислот
По количеству атомов водорода, способных замещаться на металл, кислоты делятся на:
— одноосновные кислоты: HF, HCl, HBr, HI, HNO3;
— двухосновные кислоты: H2SO4, H2SO3, H2CO3;
— трехосновные кислоты: H3PO4, H3AsO4.
Следует отметить, что количество атомов водорода в случае органических кислот чаще всего не отражает их основность. Например, уксусная кислота с формулой CH3COOH, несмотря на наличие 4-х атомов водорода в молекуле, является не четырех-, а одноосновной. Основность органических кислот определяется количеством карбоксильных групп (-COOH) в молекуле.
Также по наличию кислорода в молекулах кислоты подразделяют на бескислородные (HF, HCl, HBr и т.д.) и кислородсодержащие (H2SO4, HNO3, H3PO4 и т.д.). Кислородсодержащие кислоты называют также оксокислотами.
Более детально про классификацию кислот можно почитать здесь.
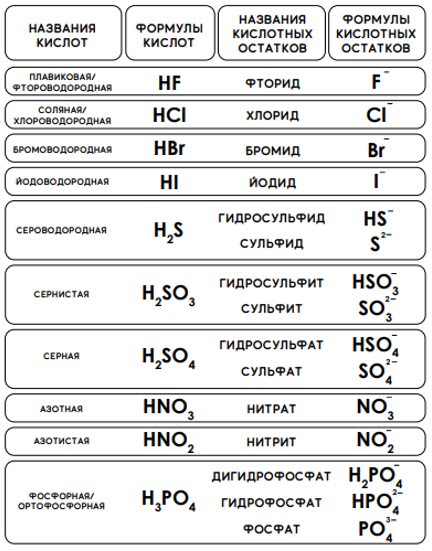
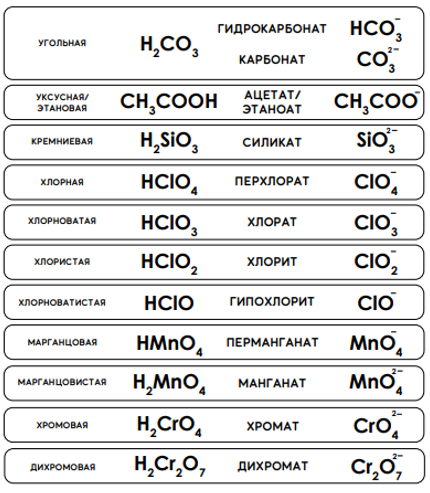
Номенклатура кислот и кислотных остатков
Нижеследующий список названий и формул кислот и кислотных остатков обязательно следует выучить.
В некоторых случаях облегчить запоминание может ряд следующих правил.
Как можно видеть из таблицы выше, построение систематических названий бескислородных кислот выглядит следующим образом:
Например:
HF — фтороводородная кислота;
HCl — хлороводородная кислота;
H2S — сероводородная кислота.
Названия кислотных остатков бескислородных кислот строятся по принципу:
Например, Cl— — хлорид, Br— — бромид.
Названия кислородсодержащих кислот получают добавлением к названию кислотообразующего элемента различных суффиксов и окончаний. Например, если кислотообразующий элемент в кислородсодержащей кислоте имеет высшую степень окисления, то название такой кислоты строится следующим образом:
Например, серная кислота H2S+6O4, хромовая кислота H2Cr+6O4.
Все кислородсодержащие кислоты могут быть также классифицированы как кислотные гидроксиды, поскольку в их молекулах обнаруживаются гидроксогруппы (OH). Например, это видно из нижеследующих графических формул некоторых кислородсодержащих кислот:
Таким образом, серная кислота иначе может быть названа как гидроксид серы (VI), азотная кислота — гидроксид азота (V), фосфорная кислота — гидроксид фосфора (V) и т.д. При этом число в скобках характеризует степень окисления кислотообразующего элемента. Такой вариант названий кислородсодержащих кислот многим может показаться крайне непривычным, однако же изредка такие названия можно встретить в реальных КИМах ЕГЭ по химии в заданиях на классификацию неорганических веществ.
Амфотерные гидроксиды
Амфотерные гидроксиды — гидроксиды металлов, проявляющие двойственную природу, т.е. способные проявлять как свойства кислот, так и свойства оснований.
Амфотерными являются гидроксиды металлов в степенях окисления +3 и +4 (как и оксиды).
Также в качестве исключений к амфотерным гидроксидам относят соединения Be(OH)2, Zn(OH)2, Sn(OH)2 и Pb(OH)2, несмотря на степень окисления металла в них +2.
Для амфотерных гидроксидов трех- и четырехвалентных металлов возможно существование орто- и мета-форм, отличающихся друг от друга на одну молекулу воды. Например, гидроксид алюминия (III) может существовать в орто-форме Al(OH)3 или мета-форме AlO(OH) (метагидроксид).
Поскольку, как уже было сказано, амфотерные гидроксиды проявляют как свойства кислот, так и свойства оснований, их формула и название также могут быть записаны по-разному: либо как у основания, либо как у кислоты. Например:
| Амфотерный гидроксид в форме основания | Амфотерный гидроксид в форме кислоты | «Кислотный» остаток |
| Zn(OH)2 гидроксид цинка | H2ZnO2 цинковая кислота | ZnO22- цинкат |
| Al(OH)3 (орто)гидроксид алюминия | H3AlO3 ортоалюминиевая кислота | AlO33- ортоалюминат |
| AlO(OH) метагидроксид алюминия | HAlO2 метаалюминиевая кислота | AlO2— метаалюминат |
Соли
Соли — это сложные вещества, в состав которых входят катионы металлов и анионы кислотных остатков.
Так, например, к солям относятся такие соединения как KCl, Ca(NO3)2, NaHCO3 и т.д.
Представленное выше определение описывает состав большинства солей, однако же существуют соли, не попадающие под него. Например, вместо катионов металлов в состав соли могут входить катионы аммония или его органические производные. Т.е. к солям относятся такие соединения, как, например, (NH4)2SO4 (сульфат аммония), [CH3NH3]+Cl— (хлорид метиламмония) и т.д.
Также противоречат определению солей выше класс так называемых комплексных солей, которые будут рассмотрены в конце данной темы.
Классификация солей
С другой стороны, соли можно рассматривать как продукты замещения катионов водорода H+ в кислоте на другие катионы или же как продукты замещения гидроксид-ионов в основаниях (или амфотерных гидроксидах) на другие анионы.
При полном замещении образуются так называемые средние или нормальные соли. Например, при полном замещении катионов водорода в серной кислоте на катионы натрия образуется средняя (нормальная) соль Na2SO4, а при полном замещении гидроксид-ионов в основании Ca(OH)2 на кислотные остатки нитрат-ионы образуется средняя (нормальная) соль Ca(NO3)2.
Соли, получаемые неполным замещением катионов водорода в двухосновной (или более) кислоте на катионы металла, называют кислыми. Так, при неполном замещении катионов водорода в серной кислоте на катионы натрия образуется кислая соль NaHSO4.
Соли, которые образуются при неполном замещении гидроксид-ионов в двухкислотных (или более) основаниях, называют основными солями. Например, при неполном замещении гидроксид-ионов в основании Ca(OH)2 на нитрат-ионы образуется основная соль Ca(OH)NO3.
Соли, состоящие из катионов двух разных металлов и анионов кислотных остатков только одной кислоты, называют двойными солями. Так, например, двойными солями являются KNaCO3, KMgCl3 и т.д.
Если соль образована одним типом катионов и двумя типами кислотных остатков, такие соли называют смешанными. Например, смешанными солями являются соединения Ca(OCl)Cl, CuBrCl и т.д.
Существуют соли, которые не попадают под определение солей как продуктов замещения катионов водорода в кислотах на катионы металлов или продуктов замещения гидроксид-ионов в основаниях на анионы кислотных остатков. Это — комплексные соли. Так, например, комплексными солями являются тетрагидроксоцинкат- и тетрагидроксоалюминат натрия с формулами Na2[Zn(OH)4] и Na[Al(OH)4] соответственно. Распознать комплексные соли среди прочих чаще всего можно по наличию квадратных скобок в формуле. Однако нужно понимать, что, чтобы вещество можно было отнести к классу солей, в его состав должны входить какие-либо катионы, кроме (или вместо) H+, а из анионов должны быть какие-либо анионы помимо (или вместо) OH—. Так, например, соединение H2[SiF6] не относится к классу комплексных солей, поскольку при его диссоциации из катионов в растворе присутствуют только катионы водорода H+. По типу диссоциации данное вещество следует скорее классифицировать как бескислородную комплексную кислоту. Аналогично, к солям не относится соединение [Ag(NH3)2]OH, т.к. данное соединение состоит из катионов [Ag(NH3)2]+ и гидроксид-ионов OH—, т.е. его следует считать комплексным основанием.
Номенклатура солей
Номенклатура средних и кислых солей
Название средних и кислых солей строится по принципу:
Если степень окисления металла в сложных веществах постоянная, то ее не указывают.
Названия кислотных остатков были даны выше при рассмотрении номенклатуры кислот.
Например,
Na2SO4 — сульфат натрия;
NaHSO4 — гидросульфат натрия;
CaCO3 — карбонат кальция;
Ca(HCO3)2 — гидрокарбонат кальция и т.д.
Номенклатура основных солей
Названия основных солей строятся по принципу:
Например:
(CuOH)2CO3 — гидроксокарбонат меди (II);
Fe(OH)2NO3 — дигидроксонитрат железа (III).
Номенклатура комплексных солей
Номенклатура комплексных соединений значительно сложнее, и для сдачи ЕГЭ многого знать из номенклатуры комплексных солей не нужно.
Следует уметь называть комплексные соли, получаемые взаимодействием растворов щелочей с амфотерными гидроксидами. Например:
*Одинаковыми цветами в формуле и названии обозначены соответствующие друг другу элементы формулы и названия.
Тривиальные названия неорганических веществ
Под тривиальными названиями понимают названия веществ не связанные, либо слабо связанные с их составом и строением. Тривиальные названия обусловлены, как правило, либо историческими причинами либо физическими или химическими свойствами данных соединений.
Список тривиальных названий неорганических веществ, которые необходимо знать:
| Na3[AlF6] | криолит |
| SiO2 | кварц, кремнезем |
| FeS2 | пирит, железный колчедан |
| CaSO4∙2H2O | гипс |
| CaC2 | карбид кальция |
| Al4C3 | карбид алюминия |
| KOH | едкое кали |
| NaOH | едкий натр, каустическая сода |
| H2O2 | перекись водорода |
| CuSO4∙5H2O | медный купорос |
| NH4Cl | нашатырь |
| CaCO3 | мел, мрамор, известняк |
| N2O | веселящий газ |
| NO2 | бурый газ |
| NaHCO3 | пищевая (питьевая) сода |
| Fe3O4 | железная окалина |
| NH3∙H2O (NH4OH) | нашатырный спирт |
| CO | угарный газ |
| CO2 | углекислый газ |
| SiC | карборунд (карбид кремния) |
| PH3 | фосфин |
| NH3 | аммиак |
| KClO3 | бертолетова соль (хлорат калия) |
| (CuOH)2CO3 | малахит |
| CaO | негашеная известь |
| Ca(OH)2 | гашеная известь |
| прозрачный водный раствор Ca(OH)2 | известковая вода |
| взвесь твердого Ca(OH)2 в его водном растворе | известковое молоко |
| K2CO3 | поташ |
| Na2CO3 | кальцинированная сода |
| Na2CO3∙10H2O | кристаллическая сода |
| MgO | жженая магнезия |




















 овалентная
овалентная еполярная
еполярная