Краткое описание документа:
Тест по теме «Углеводороды»
Часть 1.
1. Вещества с общей формулой СnH2n относятся к классу:
а) алканов
б) алкенов
в) алкинов
г) аренов
2. Гомологами являются:
а) метан и хлорметан
б) этен и пропен
в) этилен и ацетилен
г) бензол и гексан
3. Пи-связь отсутствует в молекуле
а) этана
б) этена
в) этина
г) бутадиена-1,3
4. Формула алкана:
а) C2H4
б) C8H16
в) C12H26
г) C6H6
5. Вещество, из которого получают ацетилен:
а) карбид кальция
б) карбонат кальция
в) углерод
г) гидроксид кальция
6. Для алканов характерна изомерия:
а) положения функциональной группы
б) углеродного скелета
в) положения кратной связи
г) геометрическая
7. Допишите уравнение реакции и определите ее тип СH2== CH — CH3 + HCl →
а) галогенирование
б) гидрогалогенирование
в) гидрирование
г) дегидрогалогенирование
8. Четыре атома углерода в молекуле содержит
а) пентан
б) пропин
в) бутадиен-1,3
г) циклогексан
9. Природный газ содержит главным образом
а) водород
б) пропан
в) бутан
г) метан
10. Для полного сгорания 10 литров этана потребуется кислород (О2) объемом
а) 25 л
б) 30 л
в) 35 л
г) 40 л
Часть 2
В1. Третичный атом углерода имеется в молекуле
а) этана
б) 2,2-диметилпропана
в) 2-метилпропана
г) пропана
В2. Слабые кислотные свойства проявляют
а) алканы
б) алкены
в) алкины
г) алкадиены
В3. По реакции Лебедева можно получить:
а) бутан
б) бутадиен-1,3
в) уксусный альдегид
г) бензол
В4. Допишите уравнение реакции и определите ее тип
CH2==CH2 + [O] + H2O
Часть 3
С1. При сжигании углеводорода, плотность паров которого по водороду равна 28, образовалось 8,96 л углекислого газа и 7,2 г воды. Определите формулу углеводорода и постройте все его изомеры.
Предложите, как улучшить StudyLib
(Для жалоб на нарушения авторских прав, используйте
другую форму
)
Ваш е-мэйл
Заполните, если хотите получить ответ
Оцените наш проект
1
2
3
4
5
Официальная демоверсия ЕГЭ 2022 от ФИПИ по химии.
В демонстрационном варианте представлено по несколько примеров заданий на некоторые позиции экзаменационной работы. В реальных вариантах экзаменационной работы на каждую позицию будет предложено только одно задание.
Экзаменационная работа состоит из двух частей, включающих в себя 34 задания. Часть 1 содержит 28 заданий с кратким ответом, часть 2 содержит 6 заданий с развёрнутым ответом.
На выполнение экзаменационной работы по химии отводится 3,5 часа.
Обновлено 10 ноября. Демоверсия утверждена.
→ Демоверсия: him-demo2022-v2.pdf
→ Кодификатор: him-k2022-v2.pdf
→ Спецификация: him-s2022-v2.pdf
→ Скачать одним архивом: him-demo2022-v2.zip
Изменения в КИМ 2022 года в сравнении с КИМ 2021 года
В экзаменационной работе 2022 г. по сравнению с работой 2021 г. приняты следующие изменения.
1. В экзаменационном варианте уменьшено с 35 до 34 общее количество заданий. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
− Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
− Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8.
2. Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
3. Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
4. Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
5. Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).
В целом принятые изменения в экзаменационной работе 2022 г. ориентированы на повышение объективности проверки сформированности ряда важных общеучебных умений, в первую очередь таких, как анализ текста условия задания, представленного в различной форме (таблица, схема, график), комбинирование аналитической и расчётной деятельности, анализ состава веществ и прогноз возможности протекания реакций между ними, моделирование химических процессов и описание признаков их протекания и др.
Обобщённый план варианта КИМ ЕГЭ 2022 года по химии
| Номер | Проверяемые элементы содержания |
Уровень сложности задания | Макс. балл за выпол нение задания | Примерное время выполнения задания (мин.) |
| Часть 1 | ||||
| 1 | Строение электронных оболочек атомов элементов первых четырёх периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояния атомов |
Б | 1 | 2–3 |
| 2 | Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов. Общая характеристика неметаллов IVА– VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | Б | 1 | 2–3 |
| 3 | Электроотрицательность. Степень окисления и валентность химических элементов | Б | 1 | 2–3 |
| 4 | Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения |
Б | 1 | 2–3 |
| 5 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная) |
Б | 1 | 2–3 |
| 6 | Характерные химические свойства простых веществ – металлов: щелочных, щёлочноземельных, магния, алюминия; переходных металлов: меди, цинка, хрома, железа. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния. Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот. Характерные химические свойства солей: средних, кислых, оснóвных; комплексных (на примере гидроксосоединений алюминия и цинка). Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена | П | 2 | 5–7 |
| 7 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная). Характерные химические свойства неорганических веществ:
комплексных (на примере гидроксосоединений алюминия и цинка) |
П | 2 | 5–7 |
| 8 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная); Характерные химические свойства неорганических веществ:
|
П | 2 | 5–7 |
| 9 | Взаимосвязь неорганических веществ | Б | 1 | 2–3 |
| 10 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) |
Б | 1 | 2–3 |
| 11 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа |
Б | 1 | 2–3 |
| 12 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Основные способы получения углеводородов (в лаборатории). Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Основные способы получения кислородсодержащих органических соединений (в лаборатории) |
Б | 1 | 2–3 |
| 13 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки |
Б | 1 | 2–3 |
| 14 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Важнейшие способы получения углеводородов. Ионный (правило В.В. Марковникова) и радикальные механизмы реакций в органической химии |
П | 2 | 5–7 |
| 15 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, карбоновых кислот, сложных эфиров. Важнейшие способы получения кислородсодержащих органических соединений |
П | 2 | 5–7 |
| 16 | Взаимосвязь углеводородов, кислородсодержащих и азотсодержащих органических соединений |
Б | 1 | 2–3 |
| 17 | Классификация химических реакций в неорганической и органической химии |
Б | 1 | 2–3 |
| 18 | Скорость реакции, её зависимость от различных факторов |
Б | 1 | 2–3 |
| 19 | Реакции окислительно-восстановительные | Б | 1 | 2–3 |
| 20 | Электролиз расплавов и растворов (солей, щелочей, кислот) |
Б | 1 | 2–3 |
| 21 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная |
Б | 1 | 2–3 |
| 22 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов |
П | 2 | 5–7 |
| 23 | Обратимые и необратимые химические реакции. Химическое равновесие. Расчёты количества вещества, массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ |
П | 2 | 5–7 |
| 24 | Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений |
П | 2 | 5–7 |
| 25 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ. Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки |
Б | 1 | 2–3 |
| 26 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе» |
Б | 1 | 3–4 |
| 27 | Расчёты теплового эффекта (по термохимическим уравнениям) |
Б | 1 | 3–4 |
| 28 | Расчёты массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ. Расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного. Расчёты массовой доли (массы) химического соединения в смеси |
Б | 1 | 3–4 |
| Часть 2 | ||||
| 29 | Окислитель и восстановитель. Реакции окислительно-восстановительные | В | 2 | 10–15 |
| 30 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена |
В | 2 | 10–15 |
| 31 | Реакции, подтверждающие взаимосвязь различных классов неорганических веществ |
В | 4 | 10-15 |
| 32 | Реакции, подтверждающие взаимосвязь органических соединений |
В | 5 | 10–15 |
| 33 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе». Расчёты массы (объёма, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси). Расчёты массы (объёма, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определённой массовой долей растворённого вещества. Расчёты массовой доли (массы) химического соединения в смеси |
В | 4 | 20–25 |
| 34 | Установление молекулярной и структурной формул вещества |
В | 3 | 10–15 |
| Всего заданий – 34; из них по уровню сложности: Б – 20; П – 8; В – 6. Максимальный первичный балл за работу – 56. Общее время выполнения работы – 210 мин. |
Об экзамене
Химию нельзя сдать на высокий балл, просто выучив теорию. Химию надо любить. И любить всем сердцем, чтобы тот безграничный объем информации ровным слоем уложился в голове. А когда мы говорим о будущем, о профессиях, которые будут востребованы долгие годы, то практически все направления, которые связаны с химией, с рынка труда никуда не уйдут. Потребность в “химических мозгах” стабильно растет. Поэтому если вы чувствуете, что есть хоть какая-то предрасположенность к данной науке, не поленитесь и попробуйте себя. И если все получится, то вам откроется безграничное поле для новых открытий и свершений. Меняйте себя и мир вокруг!
Структура
Часть 1 содержит 29 заданий с кратким ответом, часть 2 содержит 5 заданий высокого уровня сложности, с развернутым ответом (порядковые номера этих заданий: 30, 31, 32, 33, 34). На выполнение всех заданий отводится 3,5 часа.
Дополнительные материалы и оборудование
К каждому варианту экзаменационной работы прилагаются следующие материалы:
− Периодическая система химических элементов Д.И. Менделеева;
− таблица растворимости солей, кислот и оснований в воде;
− электрохимический ряд напряжений металлов.
Во время выполнения экзаменационной работы разрешается использовать непрограммируемый калькулятор.
Пояснения к оцениванию заданий
За правильный ответ на каждое из заданий 1–8, 12–16, 20, 21, 27–29 ставится 1 балл. Задание считается выполненным верно, если экзаменуемый дал правильный ответ в виде последовательности цифр или числа с заданной степенью точности.
Задания 9–11, 17–19, 22–26 считаются выполненными верно, если правильно указана последовательность цифр. За полный правильный ответ в заданиях 9–11, 17–19, 22–26 ставится 2 балла; если допущена одна ошибка, – 1 балл; за неверный ответ (более одной ошибки) или его отсутствие – 0 баллов.
Задания части 2 (с развёрнутым ответом) предусматривают проверку от трёх до пяти элементов ответа. Задания с развёрнутым ответом могут быть выполнены выпускниками различными способами. Наличие каждого требуемого элемента ответа оценивается 1 баллом, поэтому максимальная оценка верно выполненного задания составляет от 3 до 5 баллов в зависимости от степени сложности задания: задание 30 – 3 балла; 31 – 4 балла; 32 – 5 баллов; 33 – 4 балла; 34 – 4 балла. Проверка заданий части 2 осуществляется на основе сравнения ответа выпускника с поэлементным анализом приведённого образца ответа.
Любой учитель или репетитор может отслеживать результаты своих учеников по всей группе или классу.
Для этого нажмите ниже на кнопку «Создать класс», а затем отправьте приглашение всем заинтересованным.
Ознакомьтесь с подробной видеоинструкцией по использованию модуля.
Контрольный тест по теме «Углеводороды»
I вариант
1. Длина связи С — С в молекуле этана, нм:
а) 0,154 б) 0,140 в) 0,120 г) 0,134
2. Гомологом пропана является:
а) фенол б) пентан в) этилен г) этин
3. Гомологом С7H16 является
а) 2- метилгексан б) 3- метилоктен в) 3- метилгексан г) октан
4. Объём кислорода, необходимый для сжигания 3 литров этана, л:
а) 10,31 б) 10,5 в) 10,12 г) 10,25
5. При гидролизе карбида алюминия получают:
а) оксид алюминия б) метан в) ацетилен г) гидроксид алюминия
6. При нагревании хлорметана и хлорэтана с металлическим натрием образуется:
а) С2Н6; б) С4Н10 в) С3Н8 г) СН4
а) 5; б) 4; в) 3; г) 2.

Н2С СН ─СН3
а) циклопентан; б) 1,2 -диметилциклопропан; в) пентан; г) диметилпропан.
8. По реакции Лебедева из этилового спирта получают:
а) бутадиен-1,3; б) уксусную кислоту; в) бензол; г) этанол..
9. Определите гомологи гексена -2:
а) пропен; б) пентан; в) бутен -1; г) бутен-2
10.Характерные для алкенов реакции, обусловленные наличием π- связи в молекулах, относятся к типу реакции:
а) замещения; б) разложения; в) обмена; г) присоединения.
11При гидратации этилена образуется:
а) этан; б) этиловый спирт; в) пропан; г) пропилен.
12.По систематической номенклатуре алкен строения:СН3 = С–СН2 –СH- СН2 – СН3
│ │
СН3 СН2 – СН3
а) 2-метил-4-этиллгексен-1 ; б) 2-метил-4-этиллгексен-4;
в) 5-метил-3-этилпентен-3; г) 5-метил-3-этилпентен-2.
13. В результате реакции бутена-2 с бромом образуется;
а) 1,4-дибромбутан; б) 1,2-дибромбутан; в) 2,3-дибромбутан; г) 1,3-дибромбутан.
14. Общая формула веществ класса алкадиенов такая же, как у:
а) алкенов; б) циклопарафинов; в) алкинов; г) алканов.
15. Бутадиен и бутин – это:
а) гомологи; б) изомеры; в) радикалы; г) аллотропные видоизменения..
16.Укажите алкадиены с кумулированными связями:
а) СН2 = СН2 – СН2 –СН2 – СН2 = СН2; б) СН2 = СН — СН2 – СН = СН2 ;
в) СН2 = СН – СН = СН2; г) СН3 – СН = С = СН – СН3
17. Реакция гидратации возможна для:
а) декана; б) бензола; в) этина; г) циклопентана.
18. Тип гибридизации атомов С в этине:
а) sp б) sp2 в) sp3 г) sp3d2
19. Гомологом пропина является:
а) пропан б) ацетилен в) этен г) дивинил
20. При дегидратации этилового спирта образуется:
а) бутан; б) этен; в) этин; г) пропен.
21. Щавелевую кислоту из неорганических соединений впервые (1824) получил:
а) Ф.Велер; б) Д.И.Менделеев; в) А.М.Бутлеров; г) Н.Н.Зинин.
22. Масса карбида кальция, содержащего 20 % примесей, необходимого для получения 28 л ацетилена:
а) 64 г; б) 12 г; в) 100 г; г) 35 г.
23. Главным продуктом крекинг-процесса является
а) парафин; б) керосин; в) гудрон; г) бензин
24. Каменноугольная смола является источником:
а) циклоалканов; б) алканов; в) аренов; г) непредельных углеводородов.
25. Какая из реакций отражает крекинг нефтепродукции:
а) С4Н10 = С4Н8 + Н2 б) С6Н12 + Н2 = С6Н14 в) С4Н8 + Н2= С6Н12 г) С20Н42 = С10Н22 + С10Н20.
II вариант
1.Углеводород С7Н16 относится к классу:
а) алкены б) алкины в) алканы г) арены.
2. Углеводород 2-метилбутан имеет молярную массу, г/моль:
а) 68 б) 70 в) 72 г) 74
3. Углеводород, содержащий только σ — связи:
а) С4Н8 б) С3Н6 в) С3Н4 г) С3Н8
4. Тип гибридизации атомов С в этане:
а) sp3 б) sp2 в) sp г) sp3d2
5. Объём кислорода, необходимый для сжигания 2 литров пропана, л:
а) 1 б) 2 в) 5 г) 10
6. Изопентан получают при:
а) нагревании пентана; б) нагревании пентана в присутствии катализатора AlCl3;
в) крекинге декана; г) дегидрировании пентана.
7. Какой вид изомерии не может быть у циклопарафинов?
а) положения двойной связи. б) пространственной
в) углеродного скелета. г) межклассовой.
8. Вещество: СН3 – СН2 – СН2 ─ СН2
│ │
СН2 ─ СН2 называется:
а) этилциклобутан; б) циклобутан; в) циклогексан; г) гексан.
9. Какая из перечисленных формул принадлежит непредельному углеводороду ряда алкенов
а) С6Н12 б) С6Н5ОН в) С4Н10 г) С6Н14
10. Изомером гексена является:
а) пентан; б) гексан; в) метилциклопентан; г) гексин.
11. Гомологами являютя:
а) метилпропан и метилпропен; б) бутен-1 и пентен -1; в) метан и этен; г) этин и этен..
12. В молекуле этилена имеются:
а) две σ – и две π- связи; б) три σ – и одна π- связь;
в) четыре σ – и одна π- связь; г) пять σ – и одна π- связь.
13. Вещество не реагирующее с алкенами:
а) HCl; б) СО2; в) раствор KMnO4; г) НОН
14. Превращение ацетилена в бензол – это реакция …
а) тримеризации; б) дегидрирования; в) восстановления; г) окисления.
15. В промышленности этилен не используют для получения:
а) полипропилена; б) органических растворителей;
в) этилового спирта; г) полиэтилена.
16. Первый представитель ряда алкадиенов называется:
а) пентадиен; б) бутадиен; в) этин; г) пропадиен.
17. Пропадиен и пентадиен – это:
а) гомологи; б) изомеры; в) радикалы; г) аллотропные видоизменения.
18. Две π – связи имеются в молекуле:
а) этена; б) бутана; в) бутена; г) этина.
19. Наличием тройной связи обусловлена возможность алкинов вступать в реакции:
а) горения; б) замещения; в) дегидрирования; г) полимеризации.
20. Валентный угол в молекуле этина:
а) 10928 б) 120 в) 180 г) 90
21. Сахаристое вещество в 1861 году удалось синтезировать русскому химику:
а) М. Ломоносову; б) В. Шухову; в) И. Каблукову; г) А. Бутлерову.
22. Масса карбида кальция в образце технического карбида кальция ,если при обработке его массой 10 кг избытком воды выделилось 2,24 м3ацетилена:
а) 36 %; б) 64 %; в) 100 %; г) 22,4 %.
23. Процесс термического разделения нефти на фракции называется:
а) крекинг; б) отгонка; в) риформинг г) перегонка;
24. Смесь углеводородов, содержащих 6-10 атомов углерода, образует:
а) мазут; б) гудрон; в) бензин г) газойль
25. Какая из реакций отражает крекинг нефтепродукции:
а) С4Н8 + Н2О= С4Н9ОН б) С20Н42 + С20Н40= С40Н82
в) С40Н82 = С20Н42 + С20Н40 г) С6Н6 + 3Н2 = С6Н12
Углеводороды
Классификация органических веществ
А 1. Общая форула алкенов:
1) C
n
H
2n+2
2) C
n
H
2n
3) C
n
H
2n-2
4) C
n
H
2n-6
А 2. Вещества с общей формулой C
n
H
2n
могут относиться к классам
1) алкинов и алкенов 2) алкинов и алкодиенов
3) алкенов и алкодиенов 4) алкенов и циклопарафинов
А 3. Ароматическим углеводородам соответствует общая формула
1) С
ņ
Н
2ņ-2
3) С
ņ
Н
2ņ+2
2) С
ņ
Н
2ņ-6
4) С
ņ
Н
2ņ
Гомологи
А 4. Гомологом этилена не является
1) СН
2
=СН—СН
2
—СН
3
2) СН
2
=СН—СН
2
—СН
2
—СН
3
3) СН
2
=СН—СН
3
4) СН
3
—СН
2
—СН
3
А 5. Гомолог вещества, формула которого СН
2
=СН—СН—СН
2
—СН
3
ﺍ
СН
3
1) 2 – метилгексан 2) гептан
3) гекан 4) 3 — метилгекен
А 6. Гомологами являются
1) пентин—1 и пентин-2 2) бутин—1 и бутен-1
3) 2-метилгексен—2 и 3—метилгексан 4)2,3-диметилпентин—1 и 2,3—диметилгексин-1
А 7. Гомологом ацетилена не является
1) СН
≡ С – СН
2
– СН
3
2) СН
3
– С ≡ СН
3) СН
2
= СН – СН
3
4) СН ≡ С – СН
2
– СН
2
– СН
3
Изомеры и их названия
А 8. Изомером вещества, формула которого СН
2
=СН—СН
2
—СН
3
, является:
1) 2-метилбутен-2 2) бутен-2
3) бутан 4) пентин-1
А 9. Число нециклических изомеров углеводорода С
4
Н
8
равно
1) 1 2) 3
3) 2 4) 4
А 10. Структурным изомером пентена – 1 является
1) циклопентан 2) пентен – 2
3) 2 – метилбутен 4) 2 – метилпентен 1
А 11. Как называется углеводород:
СН
3
– СН –СН — С ≡ С – СН – СН
3
│ │ │
СН
3
СН
3
С
2
Н
5
1) 2 – этил— 5,6 –диметилгептин – 3 2) 2,4 – диметил— 6 – этилгептин – 4
3) 1,4,5 – триметил – 1 – этилгексин – 2 4) 2,3,6 – триметилоктин – 4
Строение
А 12. Число σ связей в молекуле этилена равно
1) 1 2) 3
3) 5 4) 4
А 13. Номера атом, находящихся в состоянии sp
2
— гибридизации в молекуле бутена – 2
1) 1 и 2 2) 2 и 3
3) 3 и 4 4) 1 и 4
А 14. Вещество, являющееся исходным в реакции полимеризации, называется:
1) мономер 2) полимер
3) димер 4) тример
А 15. Только σ — связи имеются в молекуле
1) бутена 2) пропилена
3) этилена 4) пентана
А 16. Число σ связей в молекуле ацетилена равно
1) 1 2) 3
3) 5 4) 4
А 17. Число π—связей в молекуле пропина равно
1) 1 2) 3
3) 2 4) 4
Химические свойства
А 18. Вещество, для которого характерна реакция гидрирования:
1) пропан 2) пропен
3) этан 4) 2- метилпропан
А 19. Для получения углеводорода с более длинной углеродной цепью применяют
реакцию:
1) Вюрца 2) Зайцева
3) Кучерова 4) Марковникова
А 20. Условия проведения реакции Кучерова – это:
1) H
2
,(Ni) 2) Сl
2
,(h )
3) Pt, 5атм 4) р—р HgSO
4
А 21. Катализатором тримеризации ацетилена в бензол служит:
1) СuСl 2) С (актив)
3) АlСl
3
4) Рt.
А 22. Формулы веществ, вступающих в реакцию друг с другом:
1) С
2
Н
4
и СН
4
2) С
3
Н
8
и Н
2
3) С
6
Н
14
и Н
2
О 4) С
2
Н
4
и Н
2
А 23. В результате реакции Вюрца из 2 – иодбутана получается:
1) н — октан 2) н — гексан
2) 2,5 – диметилгексан 4) 3,4 – диметилгексан
А 24. Отличить 2—метилпентен-2 от 2—метилпентана можно с помощью:
1) бромоводорода 2) бромной воды
3) раствора серной кислоты 4) лакмуса
А 25. Какая из реакций бензола относится к реакциям замещения?
1) нитрование 2) горение
3) гидрирование 4) взаимодействие с хлором при действии УФ —
облучения.
А 26. Органическим веществом, при пропускании которого через бромную воду раствор
обесцвечивается, является:
1) метан 2) пропилен
3) хлорметан 4) этан
А 27. Бензол не взаимодействует с
1) азотной кислотой 2) бромоводородом
3) бромом 4) хлором
А 28. При взаимодействии бутена—1 c хлороводородом атом хлора присоединяется к атому
углерода:
1) первому 2) второму
3) третьему 4) четвертому
А 29. С водородом при определенных условиях реагируют оба вещества пары:
1) бутан и бутен 2) пропен и циклопропан
3) этилен и этан 4) гексан и изобутан
А 30. И бутан и бутилен реагируют с
1) бромной водой 2) раствором KMnO
4
3) водородом 4) хлором
А 31. Продуктом реакции бутена-1 с хлором является
1) 2-хлрбутен-1 2) 1,2-дихлорбутан
3) 1,1-дихлорбутан 4) 1,2-дихлорбутен-1
А 32. При полимеризации какого углеводорода образуется полимер, структурная формула
которого
1) пропана 2) 2- метилпропана
3) 2 – метилпрпена 4) пропена
А 33. Какой тип реакции характерен для ацетилена
1) разложения 2) замещения
3) присоединения 4) обмена
А 34. Гексахлорциклогексан образуется в результате взаимодействия
1) бензола и хлора при облучении 2) бензола и хлорметана в присутствии AlCl
3
3) бензола и хлора в присутствии FeCl
3
4)бензола и хлороводорода
Получение
А 35. Формула вещества Х в цепочке превращений
t
0
+ H
2
, Ni
СН
4
→ Х → С
2
Н
4
1) СО
2
2) С
2
Н
2
3)С
3
Н
8
4) С
2
Н
6
А 36. Тип реакции С
2
Н
5
ОН → С
2
Н
4
+ Н
2
О
1) замещение 2) присоединение
3) гидрирование 4) разложение
А 37. Бензол и его гомологи выделяют из:
1) мазута 2) попутного нефтяного газа;
3) кокса 4) каменноугольной смолы
Часть В
В 1. К способам получения алкенов относят:
А) дегидрирование алканов
Б) гидрирование бензола
В) дегидратацию спиртов
Г) отщепление галогенводородов от галогеналканов
Д) ароматизацию предельных углеводородов
Е) гидратацию алкинов
Ответ: _____________________
В 2. И для метана, и для пропена характерны:
А) реакции бромирования
Б) жидкое агрегатное состояние при н.у.
В) наличие π—связи в молекулах
Г) реакции гидрирования
Д) горение на воздухе
Е) малая растворимость в воде
Ответ: _____________________
В 3. К способам получения ацетилена относят:
А) дегидратацией этилового спирта
Б) гидратацией этилена
В) дегидрирование этилена
Г) сжиганием этана
Д) гидратацией карбида кальция
Е) термическим разложением метана
Ответ: _____________________
В 4. С каким из перечисленных веществ, при соответствующих условиях реагирует
пропин:
А) водород
Б) бром
В) этен
Г) метан
Д) углекислый газ
Е) хлороводород
Ответ: _____________________
В 5. С каким из перечисленных веществ, при соответствующих условиях реагирует
бензол:
А) хлор
Б) вода
В) азотная кислота
Г) бром
Д) р—р KMnO
4
Е) хлороводород
Ответ: _____________________
В 6. Выберите признаки, характерные для этана:
А) газообразное вещество
Б) горит бледным синеватым пламенем
В) имеет резкий запах
Г) в 1,5 раз тяжелее водорода
Д) растворим в воде
Е) вступает в реакции присоединения
Ответ: _____________________
В 7. Какие углеводороды можно получить реакцией дегидрирования
А) этан
Б) бутадиен
В) пропен
Г) ацетилен
Д) бутан
Е) пентан
Ответ: _____________________
В 8. Этилен не взаимодействует с веществами:
А) HNO
3
Б) О
2
В) C
2
H
2
Г) Н
2
Д) Cl
2
Е) CH
4
Ответ: _____________________
В 9. С каким из перечисленных веществ бензол не взаимодействует:
А) H
2
Б) C
2
H
2
В) НNO
3
Г) CH
4
Д) Н
2
О
Е) Cl
2
Ответ: _____________________
В 10. Какие пары углеводородов вступают в реакции гидрирования
А) пропан и пропилен
Б) бутадиен и бензол
В) пропен и этин
Г) метан и этан
Д) пентан и пентен
Е) бензол и ацетилен
Ответ: _____________________
В 11. Для этилена характерно
А) наличие в молекулах двойной связи
Б) хорошая растворимость в воде
В) обесцвечивание бромной воды
Г) наличие в молекулах только одинарных связей
Д) реакция полимеризации
Е) наличие тройной связи
Ответ: _____________________
В 12. С раствором бромной воды реагирует
А) метан
Б) циклогексан
В) этилен
Г) ацетилен
Д) бензол
Е) пентен-2
Ответ: _____________________
В 13. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) бутан А) алкены
2) бензол Б) алкины
3) бутен В) алканы
4) метан Г) арены
Д) циклоалканы
Е) алкадиены
В 14. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) бутадиен А) алканы
2) этан Б) алкины
3) пропен В) алкены
4) ацетилен Г) алкадиены
Д) циклоалканы
Е) арены
В 15. Установите соответствие между формулой вещества и степенью окисления углерода
в нем:
1) СН
4
А) +2
2) СН
3
Сl
Б) -3
3) ССl
4
В) -4
4) Al
4
С
3
Г) +1
Д) +4
Е) -2
В 16. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
3
Н
8
+ О
2
→
СО
2
+ Н
2
О
1) С
3
Н
8
А) 3
2) О
2
Б) 2
3) СО
2
В) 8
4) Н
2
О Г) 4
Д) 1
Е) 5
В 17. Установите соответствие между названием органического соединения и числом σ— и
π— связей.
Название органического соединения Число — σ— и π —связей
1) пропен А) 12 и 2
2) этин Б) 11 и 1
3) метан В) 3 и 2
4) бутадиен-1,3 Г) 8 и 1
Д) 10 и 3
Е) 4 и 0
В 18. Установите соответствие между названием органического соединения и числом σ— и
π— связей.
Название органического соединения Число σ— и π— связей
1) этан А) 3 и 2
2) этилен Б) 6 и 2
3) бутен-1 В) 11 и 1
4) ацетилен Г) 7 и 0
Е) 5 и 1
В 19. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
6
Н
6
+ О
2
→
СО
2
+ Н
2
О
1) С
6
Н
6
А) 6
2) О
2
Б) 2
3) СО
2
В) 3
4) Н
2
О Г) 12
Д) 15
Е) 1
В 20. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
5
Н
12
+ О
2
→
СО
2
+ Н
2
О
1) С
5
Н
12
А) 8
2) О
2
Б) 6
3) СО
2
В) 2
4) Н
2
О Г) 4
Д) 1
Е) 5
В 21. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
4
Н
8
+ О
2
→
СО
2
+ Н
2
О
1) С
4
Н
8
а) 1
2) О
2
б) 2
3) СО
2
в) 4
4) Н
2
О г) 5
д) 6
е) 8
В 22. Установите соответствие между названием органического соединения и структурной
формулой
Название вещества Структурная формула
1) транс-5-метилгептен—2 А) СН
3
– СН
2
– С = СН – СН
2
– СН
3
|
2) 2,5-диметилгексен—1 СН
2
– СН
3
3) 2-метил-3,6-диэтилоктен-4 СН
3
Н
4) 3-этилгексен—3 Б) С=С
Н СН
2
– СН – СН
2
– СН
3
|
СН
3
В) СН
2
= С – СН
2
– СН
2
– СН – СН
2
– СН
3
| |
СН
3
СН
3
Н Н
Г) С=С
СН
3
СН
2
– СН – СН
2
– СН
3
|
СН
3
СН
3
|
Д) СН
3
– СН – СН – СН = СН – СН – СН
2
– СН
3
| |
СН
2
– СН
3
СН
2
– СН
3
В 23. Установите соответствие между структурной формулой органического соединения и
его названием
Структурная формула вещества Название вещества
1) А) 1,3,5-триметилбензол
Б) пара—метилэтилбензол
2)
В) 1-пропил-5-метил-2-этилбензол
3) Г) 1-метил-4-этилбензол
Д) пропилбензол
4)
Е) 1-метил-3-этил-4-пропилбензол
В 24. Установите соответствие между структурной формулой вещества и названием
гомологического ряда, к которому оно принадлежит
1) С
6
Н
5
— СН
2
—СН
3
2) СН
3
—С(СН
3
)
2
—СН
2
—СН
3
3) СН
2
=С=СН—СН
3
4) СН
3
—С≡С—СН
3
А) алкодиены
Б) алканы
В) арены
Г) алкены
Д) алкины
В 25. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) гексен А) алкены
2) этан Б) алкины
3) циклобутан В) алканы
4) этилен Г) спирты
Д) циклоалканы
Е) алкадиены
В 26. Установите соответствие между структурной формулой вещества и названием
гомологического ряда, к которому оно принадлежит
1) С
6
Н
5
—СН
3
2) СН
3
—СН
2
—СН
2
— СН = СН—СН
3
3) СН
2
=СН—СН
2
—СН
3
4) СН
3
—С≡С—СН
2
—СН
3
А) алкодиены
Б) алканы
В) алкины
Г) алкены
Д) арены
В 27. Установите соответствие между исходными веществами и продуктами реакции
Вещества, вступившие в реакцию Основной продукт реакции
H
2
SO
4
(конц.)
1) + HNO
3
А) Б)
hν
2) + С1
2
В) Г)
3) AlCl
3
+ С
2
Н
5
С1
FeCl
3
4) + Cl
2
Д) Е)
В 28. Установите соответствие между названием вещества и формулой его
изомера
Название вещества Формула изомера
1) 2-метилбутен—2 А) СН
2
= СН – СН
2
– СН
2
– СН
3
2) цис-3-метилпентен-1 Н СН
3
3) бутен-1 Б) С=С
4) 2,3-диметилбутен-1 СН
3
СН
2
– СН
3
СН
3
|
В) СН
3
– С = С – СН
3
|
СН
3
СН
3
СН
3
Г) С=С
Н СН
2
– СН
3
Д) СН
3
– СН = СН – СН
3
Е) СН
3
– СН = С – СН
2
– СН
3
|
СН
2
– СН
3
В 29. Установите соответствие между исходными веществами и продуктами реакции
Вещества вступившие в реакцию Продукты реакции
1) СН
3
– С ≡ С – СН
3
+ Н
2
А) СН
3
СН
2
ОН
Б) СН
3
– СВr = СН
2
2) СН
3
– С ≡ СН + НВr В) СН
3
– СН = СН – СН
3
Г) СН
3
– СН = СНВr
3) СН ≡ СН + НОН Д) СН
3
– СНВr= СНВr- СН
3
4) СН
3
– С ≡ С – СН
3
+ Вr
2
Е) СН
3
СОН
В 30. Установите соответствие между исходными веществами и продуктами реакции
Вещества вступившие в реакцию Продукты реакции
1) СН
3
– С ≡ СН + Н
2
А) СН
2
=СН
2
Б) СН
3
– СН= СН
2
2) СН
3
– СН = СН
2
+ НВr В) СН
3
– СНВr-СН
3
Г) СН
3
– СН
2
—СНВr
3) СН ≡ СН + 2Н
2
Д) СН
3
– СНВr= СНВr- СН
3
4) СН
3
– С ≡ С – СН
3
+ Вr
2
Е) СН
3
—СН
3
Часть С
С 1. Определите формулу алкена, если известно, что 4,2 г этого алкена присоединяет 8,0 г
брома.
С 2. Осуществите следующие превращения. Запишите уравнения реакций.
+ Cl
2
+Na + Br
2
+ NaOH(спирт.) + Н
2
О
СН
3
– СН
3
→ Х
1
→ Х
2
→
Х
3
→ Х
4
→ Х
5
С 3. Осуществите следующие превращения. Запишите уравнения реакций.
С 4. Осуществите следующие превращения. Запишите уравнения реакций.
+Н
2
О, HgSO
4
С → СН
4
→ С
2
Н
2
→ Х
3
С 5. Напишите уравнения реакций, при помощи которых можно осуществить следующие
превращения, указав вещество X , и условия проведения реакций
+НNO
3
C
2
H
6
→ C
2
H
4
→ C
2
H
2
→ C
6
H
6
→
X
С 6. Осуществите следующие превращения. Запишите уравнения реакций.
+H
2
O +1мольCl
2
+Nа,t
Al
4
C
3
→X
1
→ X
2
→ X
3
С 7. Осуществите следующие превращения. Запишите уравнения реакций.
300
0
+ Cl
2
(FeCl
3
)
Гексен Гексан Х
1
Х
2
С 8. Напишите уравнения реакций, при помощи которых можно осуществить следующие
превращения, указав условия проведения реакций:
CH
4
→ C
2
H
2
→ C
2
H
4
→ C
2
H
2
→ C
6
H
6
С 9. Согласно термохимическому уравнению реакции
CH
4
+ 2O
2
→ CO
2
+ 2H
2
O + 900 кДж вычислите количество теплоты, которое
выделиться при сжигании 3,2 г метана.
С 10. Согласно термохимическому уравнению реакции
CH
4
+ 2O
2
→ CO
2
+ 2H
2
O + 900 кДж вычислите количество теплоты, которое
выделиться при сжигании 8 г метана.
С 11. Определите формулу углеводорода, массовая доля углерода в котором 85,7%, а
плотность паров по водороду 28.
С 12. Из 92 г этанола получили 33,6 л (н.у.) этилена. Вычислите выход продукта в
процентах от теоретически возможного.
С 13. Определите формулу углеводорода, массовая доля водорода в котором равна 20%.
Относительная плотность углеводорода по водороду равна 15.
С 14. Определите формулу углеводорода, при сжигании которого образовалось 1, 792л
(н.у) оксида углерода (IV ) и 1,44г воды. Относительная плотность вещества по водороду
равна 28.
С 15. Определите формулу углеводорода, при сжигании которого образовалось 4,48л
оксида углерода (IV) (н.у) и 1,8г воды. Масса 10л этого газа составляет 12,5г.
С 16. Найдите простейшую формулу углеводорода, содержащего 92,31% углерода по
массе.
С 17. Вычислите массовую долю углерода и водорода в молекуле пропана.
С 18. При нагревании иодметана массой 2,84 с избытком металлического
натрия получили 179,2 мл этана (н.у). Определите выход продукта реакции.
С 19. Определите алкан, 1 л которого при н.у. весит 2,59 г. Составьте его структурную
формулу.
С 20. Определите простейшую формулу углеводорода, при сжигании которого
образовалось 2,24л оксида углерода (IV) (н.у) и 3,6г воды.
С 21. Вычислите массу бромбензола, которую можно получить при бромировании
117 г бензола бромом массой 316 г.
С 22. Углеводород, плотность паров которого по водороду равна 15, содержит 80 %
углерода. Найдите его молекулярную формулу.
С 23. Из 7,8 г бензола получено 8,61 г нитробензола. Определите выход продукта реакции.
С 24. Технический карбид кальция массой 20 г обработали избытком воды. Какой объем
ацетилена получили, если массовая доля примесей техническом карбиде составляла 20 %.
С 25. Какая масса бромбензола образуется при взаимодействии 7,8 г бензола с избытком
брома в присутствии FeBr
3
, выход продукта реакции равен 90%?
С 26. При сжигании 29 г углеводорода образовалось 88 г оксида углерода (IV) и 45 г воды.
Выведите молекулярную формулу углеводорода.
С 27. Из 44,8 л метана получили 40 л хлорметана. Определите сколько это составляет в %
от теоретически возможного выхода.
С 28. Вычислите объем углекислого газа, выделившегося при сгорании 56 л метана в 48 л
кислорода
С 29. Из 92 г этанола получили 33,6 л (н.у.) этилена. Определите выход продукта в
процентах от теоретически возможного.
С. 30. Найдите объем этилена, необходимый для обесцвечивания 50 г 2%—ного раствора
бромной воды.
Пройти тестирование по этим заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Из предложенного перечня выберите все вещества, при взаимодействии которых с раствором перманганата калия будет наблюдаться изменение окраски раствора.
1) циклогексан
2) бензол
3) толуол
4) пропан
5) пропилен
Запишите в поле ответа номера выбранных веществ.
Источник: Демонстрационная версия ЕГЭ—2017 по химии
2
Из предложенного перечня выберите два ряда веществ, с каждым из которых может реагировать бутен-1.
1)
2)
3)
4)
5)
Запишите в поле ответа номера выбранных рядов веществ.
Источник: РЕШУ ЕГЭ, Яндекс: Тренировочная работа ЕГЭ по химии. Вариант 1.
3
Из предложенного перечня выберите все вещества, из которых можно получить бутан в одну стадию.
1) бутанол-1
2) бутановая кислота
3) бутен-1
4) бутен-2
5) бутанол-2
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
4
Из предложенного перечня выберите все вещества, с которыми взаимодействует пентан.
1) хлор на свету
2) раствор
3) бром на свету
4) бромная вода
5) раствор
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
5
Из предложенного перечня выберите все вещества, которые могут реагировать с каждым из веществ: водой, бромоводородом, водородом.
1) пропан
2) этилен
3) бутен-1
4) этан
5) хлорметан
Запишите в поле ответа номера выбранных веществ.
Источник: РЕШУ ЕГЭ
Пройти тестирование по этим заданиям
Углеводороды
I вариант
Часть А
А1. Какие из перечисленных веществ являются гомологами метана
- C2H2
- C3H6
- C4H10
- C5H10
А2. Геометрические (цис-транс-) изомеры имеет
- 2-метилбутен-1
- пентен-2
- пропин
- бутан
А3. Длина связи углерод – углерод в алканах равна
- 0,154 нм
- 0,140 нм
- 0,132 нм
- 0,120 нм
А4. Назовите соединения
CH3-C(C2H5)=C(C2H5)-CH2-CH3
- 3-этил-4метилгексен-3
- 2,3-диэтилпентен-2
- 3-метил-4-этилгексен-3
- 2,3-диэтилпентен-3
А5. При взаимодействии пропилена с водой образуется
- пропанол-1
- пропанол-2
- пропаналь
- 2-метилпропанол
А6. Межклассовыми изомерами являются
- алканы и алкены
- алкены и циклоалканы
- алкадиены и алкены
- алканы и алкины
А7. Является гомологом этина
- C4H6
- C5H10
- C3H8
- C2H4
А8. Реакциями замещения и присоединения соответственно являются:
- CH4+Cl2
и C2H2+Cl2→
- CH3COONa+HCl → и C6H6+Br2
- H2SO4+Zn → и H2SO4 + CuO →
- C8H18
и C2H6 + Cl2
А9. С бромной водой взаимодействует каждое из двух веществ:
- этилен и бензол
- бутадиен-1,3 и бутан
- этан и этен
- бутин-1 и пентадиен-1,3
А10. Определите вещество В в следующей цепочке превращений:
CH2-CH=CH2 A
Б
B.
- 1,2-дипромпропан
- пропен
- пропан
- пропандиол-1,2
А11. В ходе реакции Лебедева бутадиен-1,3 получают из
- этанола
- этилена
- бутана
- бутена-1
А12. При гидратации пропина образуется
- пропанол-1
- пропанол-2
- пропанон
- пропаналь
А13. В соответствии с термохимическим уравнением реакции 2CH3OH+3O2=2CO2+4H2O+1452 кДж,
при сгорании 16 г метанола выделится:
- 181,5 кДж
- 363 кДж
- 726 кДж
- 1452 кДж
Часть В
В1. Для пропена характерны:
- наличие в молекуле сопряженной электронной системы
- sp2-гибридизация всех атомов углерода
- реакция замещения
- обесцвечивания раствора MnO4
- горючесть
- хорошая растворимость в воде
Ответ: ______________________
В2. Толуол вступает в реакцию с
- аммиаком
- хлороводородом
- хлором при освещении
- аммиачным раствором оксида серебра
- хлором в присутствии катализатора AlCl3
- хлорэтаном в присутствии катализатора AlCl3
Ответ:________________________
(Запишите соответствующие буквы в алфавитном порядке)
В3. И для этилена, и для ацетилена характерны:
- взаимодействие с оксидом меди (II)
- наличие σ и π-связей в молекулах
- sp2— гибридизации атомов углерода в молекуле
- реакция гидрирования
- горение на воздухе
- реакции замещения
Ответ:____________________________
(Запишите выбранные цифры в порядке возрастания).
В4. Установите соответствие между структурной формулой вещества и названием его гомологического ряда
|
ФОРМУЛА ВЕЩЕСТВА |
ГОМОЛОГИЧЕСКИЙ РЯД |
|
а) C6H5 — CH2-CH3 |
1. алкадиены |
|
б) C6H5-C(CH3)2-CH2-CH3 |
2. алканы |
|
в) CH2=C=CH-CH3 |
3. арены |
|
г) CH3-CC-CH3 |
4. алкены |
|
5. алкины |
Часть С
С1. При сжигании газообразного углеводорода с плотностью по кислороду 1,312 получено 16,8 л углекислого газа и 13,5 г воды.
Определите молекулярную формулу углеводорода.
С2. Осуществите превращения:
CaC2 →C2H2 →C2H3Br→C2H4Br2 →C2H2 →CH3-CH = O.
C3. Для нитрования 18,4 г толуола взято 50 г раствора азотной кислоты, содержащего 94,6% (по массе) кислоты. Определите массу полученного тринитротолуола, если выход продукта реакции составляет 75% от теоретически возможного.
Углеводороды
II вариант
Часть А
А1. Какие из перечисленных веществ являются гомологами этена
- C2H2
- C3H6
- C4H10
- C5H12
А2. Пентен-1 и гексен-1 являются
- одним и тем же веществом
- структурными изомерами
- геометрическими изомерами
- гомологами
А3. В каком углеводороде все атомы углерода находятся в состоянии sp2 –гибридизации?
- H2C=CH-CH=CH2
- H2C=C=CH-CH3
- H3C-CH2-CCH
- H3C-CC-СН3
А4. Назовите соединения CH3-C(C2H5)=CH-CH(CH3)2
- 2,4-диметилгексен-3
- 3,5-диметилгексен-3
- 5-метил-2-этилпентен-2
- 1,1-диметил-3-этилбутен-2
А5. При взаимодействии пропена с хлороводородом преимущественно образуется
- CH3-CHCl-CH3
- CH2Cl-CH2-CH3
- CH2Cl-CHCl-CH3
- CH2Cl-CH2-CH2Cl
А6. Структурный изомер нормального гексана имеет название
- 3-этилпентан
- 2-метилпропан
- 2,2-диметилпропан
- 2,2-диметилбутан
А7. В результате окисления продукта гидратации ацетилена получается
- муравьиная кислота
- масляная кислота
- пропионовый альдегид
- уксусный альдегид
А8. Две π-связи содержатся в молекуле:
- этена
- бутана
- бутена
- этина
А9. Сходства химических свойств бензола и предельных углеводородов в реакции:
- С6H6+3H2→C6H12
- C6H6+C2H4→C6H5-C2H5
- C6H6+3Cl2→C6H6Cl6
- C6H6+Br2→C6H5Br+HBr
А10. Определите вещество В в следующей цепочке превращений:
CH3-CH2-CH3 A Б
B.
- 1,2,3-трибромпропан
- 1,2-дибромпропан
- 1-бромпропан
- 2-бромпропан
А11. Вулканизация – процесс нагревания каучука с
- сажей
- фосфором
- бромом
- серой
А12. Бутанол-1 преимущественно образуется при
- гидратации бутена-1
- гидратации бутена-2
- действии водного раствора щелочи на 1-хлорбутан
- действии спиртового раствора щелочи на 1-хлорбутан
А13. Согласно термохимическому уравнению реакции
CH4(г) +2O2(г) =CO2(г) + 2H2O(г) + 802 кДж, количество теплоты, выделившейся при сжигании 24 г метана, равно
- 1604 кДж
- 1203 кДж
- 601,5 кДж
- 401 кДж
Часть В
В1. Для бутана характерны:
- наличие в молекуле сопряженной электронной системы
- sp2-гибридизация всех атомов углерода
- реакция замещения
- обесцвечивания раствора KMnO4
- горючесть
- хорошая растворимость в воде
Ответ: _______________________
В2.Алкены взаимодействуют с
- [Ag(NH3)2]OH
- Br2 (p-p)
- Cu(OH)2
- KMnO4(H+)
- H2O
- Ca(OH)2
Ответ:___________________________
(Запишите выбранные цифры в порядке возрастания).
В3. Для метана и для пропена характерны:
- реакция бромирования
- sp-гибридизация атомов углерода в молекуле
- наличие π-связи в молекулах
- реакция гидрирования
- горения на воздухе
- газообразные вещества
Ответ:____________________________
(Запишите выбранные цифры в порядке возрастания).
В4. Установите соответствие между структурной формулой углеводорода и общей формулой его гомологического ряда
|
ФОРМУЛА УГЛЕВОДОРОДА |
ОБЩАЯ ФОРМУЛА |
|
а) CH2=C(CH3)-CH=CH2 |
1. CnH2n+2 |
|
б) CH3-CC-CH2-CH3 |
2. CnH2n-2 |
|
в) C6H5-CH2-CH2-CH3 |
3. CnH2n-6 |
|
г) CH3-CH(CH3)-CH (CH3)-CH3 |
4. CnH2n |
Часть С
С1. В результате сжигания алкана образовалось 8,96 л (н.у.) углекислого газа и 9 г воды. Определите формулу алкана.
С2. Осуществите превращения:
C → Al4C3 → CH4 → C2H2 → C2H3Cl → полимер
С3. Из ацетилена объемом 61,6 л (н.у.) по реакции Кучерова было получено 72,6 г уксусного альдегида (этаналь). Определите выход продукта реакции в % от теоретически возможного.
29 апреля 2022
В закладки
Обсудить
Жалоба
Контрольная работа по теме «Углеводороды»
2 варианта по 14 заданий.
Часть А. Тестовые задания с выбором ответа. За задание 1 балл.
Часть Б. Задания со свободным ответом.
Часть С. Задача.
В контрольную работу были включены вопросы и задания по теме «Углеводороды»:
1. Общая формула классов углеводородов.
2. Номенклатура.
3. Гомологи и изомеры.
4. Химические реакции данных классов.
5. Генетическая связь между классами.
6. Основные области применения.
7. Задача на нахождение формулы.
uglv.doc
uglv.pdf
Автор: Ганеева Ирина Борисовна.
Чтобы поделиться, нажимайте
Тесты по теме Углеводороды.
Предлагаем вашему вниманию тесты по теме Углеводороды с подробными видео-объяснениями (даны сразу после условий задания) и ответами (приведены в конце страницы).
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
1. При взаимодействии вещества C3H6 с хлором при определённых условиях выделился хлороводород. Укажите класс исходного вещества и тип реакции соответственно:
-
алканы, замещения
-
алкены, замещения
-
алкены, присоединения
-
циклоалканы, присоединения
2. Укажите вещество, образующееся при взаимодействии 2-хлоргексана со спритовым раствором гидроксида натрия при нагревании, которое существует в виде цис-транс-изомеров:
-
гексен-1
-
гексен-2
-
3-метилпентен-2
-
пентадиен-1,3
3. Число изомерных углеводородов, имеющих относительную молекулярную массу 86, равно:
-
4
-
7
-
6
-
5
4. Гомологи образуются при действии избытка хлора в присутствии тетрахлористого углерода на УВ-ы пары:
-
пропен и пропадиен
-
пропин и этен
-
бутин-1 и бутадиен-1,3
-
бутин-1 и ацетилен
5. Для соединений с общей формулой CnH2n наиболее характерны реакции:
-
поликонденсации
-
замещения
-
присоединения
-
обмена
6. В молекуле неизвестного углеводорода содержатся атомы углерода только в sp3-гибридизации, а молярная масса 72 г/моль. Число структурных изомеров у этого углеводорода равно:
-
4
-
3
-
5
-
2
7. Гомологи образуются при взаимодействии водорода в мольном соотношении 1:1 с каждым из углеводородов пары:
-
бутен-1 и пентадиен-1,4
-
пропин и ацетилен
-
этен и пропан
-
ацетилен и бензол
8. Укажите пару веществ, которые при взаимодействии с избытком водорода образуют гомологи:
-
бутин-1 и пентадиен-1,3
-
бутадиен-1,3 и бутин-2
-
2-метилпропен и бутадиен-1,3
-
гексен-3 и 4-метилпентин-1
9. Укажите пару веществ, при полном гидрировании которых образуются изомеры:
10. Укажите число ВСЕХ изомеров ациклического и циклического строения (включая цис- и транс-изомеры) с относительной молекулярной массой 56:
-
7
-
4
-
5
-
6
11. Этен дегидрируют. При этом:
а) связь между атомами углерода укорачивается;
б) валентный угол между атомами углерода и соседним водородом увеличивается;
в) число пи-связей уменьшается;
г) протекает реакция присоединения.
-
а, б
-
а, г
-
б, в
-
в, г
12. Выберите верное утверждение:
1) уравнения СН3(СН2)4СН3 → С6Н6 + 4Н2 отражает процесс дегидроциклизации гексана
2) этан можно получить гидролизом карбида алюминия
3) продуктами полного сгорания углеводородов с общей формулой CnH2n являются угарный газ и вода
4) температура кипения изобутана выше температуры кипения бутана
13. Массовая доля водорода в газообразном при н.у. углеводороде составляет 7,69%. Этим углеводородом может быть:
1) С2H2
2) C6H6
3) C7H8
4) CH4
14. Из технического карбида алюминия, содержащего 14% примесей, с выходом 80% был получен ацетилен массой 2кг. Масса (кг) потраченного технического карбида алюминия равна:
1) 13,8
2) 16,1
3) 9,2
4) 10,7
15. Укажите число ациклических структурных изомеров состава C4H5Br, в молекулах которых присутствуют одинарные связи и одна тройная:
1) 3
2) 4
3) 5
4) 6
16. В отличие от пентена-2 бензол:
1) является предельным углеводородом
2) НЕ реагирует с раствором перманганата калия
3) имеет другой качественный состав
4) реагирует с кислородом
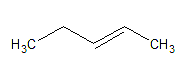
17. Структурным изомером соединения, формула которого , является :
:
1) пентен-2
2) 2-метилпентен-1
3) циклопентан
4) 2-метилбутадиен-1,3
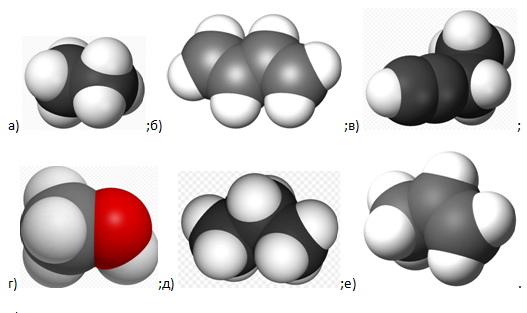
18. Укажите масштабные модели углеводородов, молекулы которых содержат π-связи:
1) а, в, е
2) а, г, д
3) б, в, е
4) б, в
5) в, г
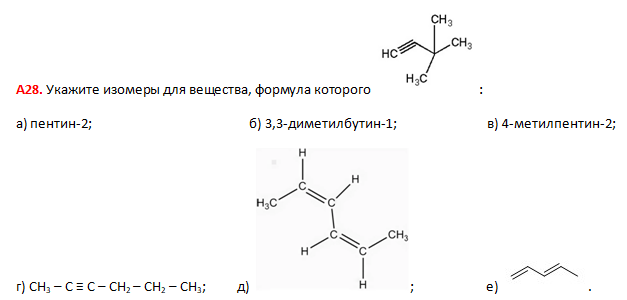
19.
 1) а, в, г
1) а, в, г
2) а, е
3) б, г, е
4) в, г, д
5) в, д, е
20. Как этен, так и пропин реагируют со всеми веществами пары:
1) бром, ацетат натрия
2) хлороводород, перманганат калия
3) азотная кислота, барий
4) бензиловый спирт, хлорид железа (III)
5) вода, оксид серебра (I)
Ответы:
1. 2
2. 2
3. 4
4. 4
5. 3
6. 2
7. 2
8. 1
9. 1
10. 4
11. 1
12. 1
13. 1
14. 4
15. 2
16. 2
17. 3
18. 3
19. 4
20. 2
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
Посмотреть видео-объяснения каждого задания ЦТ, РТ и ДРТ всех лет, а также получить условия всех пробных, тренеровочных и реальных вариантов ЕГЭ, вы можете получив полный доступ к сайту кликнув здесь «Получить все материалы сайта»
А также:
- Просмотреть все тесты по органической химии
- Просмотреть все тесты по неорганической химии
- Посмотреть пробные варианты ЦТ вы можете здесь, нажав на эту строку
- Посмотреть пробные и реальные варианты ЕГЭ вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Больше заданий РТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЦТ вы можете найти здесь, нажав на эту строку
- Больше заданий ЕГЭ вы можете найти здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку
Материалы сайта (тесты, задания, задачи, видео) разработаны автором самостоятельно и не являются копией каких-либо других заданий, в том числе заданий, разработанных РИКЗом (Республиканским институтом контроля знаний). При составлении заданий использованы идеи, которые были использованы составителями ЦТ и РТ, что не является нарушением авторского права. Все материалы сайта используются исключительно в образовательных целях.
В доказание вышесказанного, привожу выдержки из Закона Республики Беларусь «Об авторском праве и смежных правах»:
Статья 7. Произведения, не являющиеся объектами авторского права
Пункт 2. Авторское право не распространяется на собственно идеи, методы, процессы, системы, способы, концепции, принципы, открытия, факты, даже если они выражены, отображены, объяснены или воплощены в произведении.
Статья 32. Свободное использование объектов авторского права и смежных прав
Пункт 2. Допускается воспроизведение отрывков из правомерно обнародованных произведений (цитирование) в оригинале и переводе в исследовательских, образовательных, полемических, критических или информационных целях в том объеме, который оправдан целью цитирования.
Статья 36. Свободное использование произведений в образовательных и исследовательских целях
Пункт 2. Статьи и иные малообъемные произведения, правомерно опубликованные в сборниках, а также газетах, журналах и других печатных средствах массовой информации, отрывки из правомерно опубликованных литературных и иных произведений могут быть воспроизведены посредством репродуцирования и иного воспроизведения в образовательных и исследовательских целях.
В данном разделе представлена подборка заданий по отдельным темам курса химии. Задания составлены в формате ЕГЭ и направлены на помощь в подготовке к итоговой аттестации.
При возникновении вопросов по содержанию или решению заданий обращайтесь через поле «Оставьте отзыв».
Тематические тесты по химии элементов
Неметаллы
Тестовые задания по теме «Водород» (скачать).
Тестовые задания по теме «Галогены и их соединения» (скачать).
Металлы
Тестовые задания по теме «Элементы IA и IIA групп» (скачать).
Тестовые задания по теме «Алюминий» (скачать).
Тестовые задания по теме «Железо» (скачать).
Тестовые задания по теме «Марганец» (скачать).
Тестовые задания по теме «Медь» (скачать).
Тестовые задания по теме «Серебро» (скачать).
Тестовые задания по теме «Хром» (скачать).
Тестовые задания по теме «Цинк» (скачать).
Ответы на тестовую часть заданий по металлам (скачать).
Тематические тесты по органической химии
Тестовые задания по теме «Алканы» (скачать).
Тестовые задания по теме «Алкены» (скачать).
Тестовые задания по теме «Алкадиены» (скачать).
Тестовые задания по теме «Алкины» (скачать).
Тестовые задания по теме «Арены» (скачать).
Тестовые задания по теме «Спирты. Фенол» (скачать).
При обращении ответы на тесты высылаются по почте, с которой написан запрос.


 :
:
 1) а, в, г
1) а, в, г